© Borgis - Postępy Fitoterapii 4/2007, s. 194-201
Loretta Pobłocka-Olech, *Mirosława Krauze-Baranowska
Aktywność farmakologiczna chalkonów1
PHARMACOLOGICAL ACTIVITY OF CHALCONES
Katedra i Zakład Farmakognozji z Ogrodem Roślin Leczniczych Akademii Medycznej w Gdańsku
Kierownik Katedry i Zakładu: dr hab. prof. nadzw. Mirosława Krauze-Baranowska
Summary
Chalcones belong to the group of natural compounds, which rarely occur in the plant kingdom. Among the medicinal plants (herbal remedies) they are present in the willow bark, everlasting flower and liquorice root. Most of pharmacological researches were performed on semi-synthetic derivatives of chalcones, which posses protozoicide (1-(2,5-dichlorophenyl)-3-(4-chinoyl)-2-propen-1-on,4-chlorochalcone) and antibacterial (2´-hydroxychalcone,2,4,2´-trihydroxy-5´-methylchalcone) activity. For the structures isolated from plants different directions of pharmacological activities, such as: antineoplastic (isobavachalcone, 4-hydroxyderricin, isoliquiritigenin, pedicine), antiulcerogenic (2´,4´-dihydroxy-3´-methoxychalcone, xantoangelol, sophoradin), spasmolytic (isosalipurposide, isoliquiritoside) and antiphlogistic (2´,4´,6´-trimethoxychalcone) have been described.

Chalkony (1,3-diarylo-2-propen-1-on) (ryc. 1) są pochodnymi acetofenonu i stanowią produkt pośredni w biosyntezie flawonoidów (1-3). Są to związki o charakterze lipofilowym i żółtym zabarwieniu. Charakterystyczną cechą cząsteczki chalkonu jest otwarty pierścień heterocykliczny, którego zamknięcie przekształca chalkon w układ flawanonu. Chalkony są związkami nietrwałymi i znajdują się w dynamicznej równowadze z odpowiednimi flawanonami (1, 4).
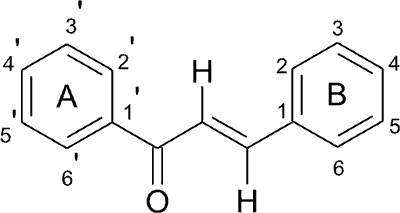
Ryc. 1. Wzór strukturalny chalkonu.
W przyrodzie występują jako aglikony oraz w postaci związanej glikozydowo lub estrowo. Ich obecność wykazano w 54 rodzinach, między innymi: Asteraceae (rodzaj Helichrysum i Dahlia), Fabaceae ( Glycyrrhiza), Salicaceae ( Salix) i Rubiaceae ( Citrus). W rodzinie Aristolochiaceae stanowią główną grupę związków czynnych (3). W przeciwieństwie do flawonoli chalkony są rzadko wskazywane jako związki decydujące o aktywności surowców leczniczych, pozyskiwanych z roślin umiarkowanej strefy klimatycznej (4). Dotychczas obecność chalkonów potwierdzono jedynie w czterech gatunkach, a mianowicie w lukrecji ( Glycyrrhiza glabra, Fabaceae – izolikwirytygenina oraz jej glikozyd izolikwirytozyd), chmielu ( Humulus lupulus, Cannabinaceae – ksantohumnol) oraz w kocankach ( Helichrysum arenarium, Asteraceae) i wierzbach ( Salix sp., Salicaceae – izosalipurpozyd) (4).
Chalkony oraz ich pochodne, zarówno naturalne jak i syntetyczne, wykazują różnorodną aktywność farmakologiczną. W wyniku badań przeprowadzonych w ostatnich latach opisano ich właściwości przeciwnowotworowe (5-13), przeciwbakteryjne (7, 14-19), przeciwgrzybicze (7), przeciwwirusowe (7), przeciwpierwotniakowe (7, 20-26), antyagregacyjne (27, 28), przeciwwrzodowe (7, 29) oraz przeciwzapalne (2, 7, 30).
Działanie przeciwpierwotniakowe
Zakażenia pierwotniakami z rodzaju: Plasmodium, Leishmania i Trypanosoma są przede wszystkim problemem krajów rozwijających się. Wzrost oporności pierwotniaków sprawia, że poszukiwane są związki o innym mechanizmie działania, niż np. chlorochina i bardziej skuteczne w leczeniu, m.in. malarii (7).
Wykazano, że naturalne i syntetyczne chalkony wykazują działanie przeciwmalaryczne o różnym mechanizmie.
Spośród syntetycznych chalkonów wysoką aktywność wobec szczepów Plasmodium falciparum, wrażliwych jak i opornych na chlorochinę, wykazuje 1-(2,5-dichlorofenylo)-3-(4-chinonylo)-2-propen-1-on (24). Przypuszcza się, że związek ten hamuje proteazę cysteinową, enzym produkowany przez trofozoity (postać zarodźca malarii znajdująca się w erytrocytach) i w ten sposób blokuje degradację hemoglobiny (7, 24) – źródła aminokwasów dla pierwotniaków (24). Chalkony są odwracalnymi inhibitorami enzymu, natomiast nie hamują katepsyny B, odpowiednika proteazy cysteinowej w komórkach ssaków (7, 24).
Syntetyczne chalkony o właściwościach przeciwmalarycznych działają przez blokowanie przepuszczalności kanałów w błonach erytrocytów (21). Błona erytrocytu w normalnych warunkach jest nieprzepuszczalna, ale kanały utworzone przez pasożyty w zainfekowanych krwinkach umożliwiają wnikanie szeregu substancji niezbędnych do ich rozwoju, np. aminokwasów, cukrów oraz jonów organicznych i nieorganicznych (21).
Wśród badanych chalkonów o właściwościach przeciwmalarycznych najsilniejsze działanie hamujące hemolizę, wywołaną przez sorbitol, mają pochodne dimetoksy- i metoksychalkonów. Hydroksychalkony wykazują około dwukrotnie niższą aktywność w porównaniu do chalkonów o właściwościach przeciwmalarycznych, natomiast są pozbawione wpływu na hemolizę indukowaną sorbitolem (21). Metoksy- i dimetoksychalkony mają dwie istotne właściwości: selektywną toksyczność przeciwko Plasmodium i nie wiążą się z białkami osocza, co wynika z nieanionowego charakteru cząsteczki (21).
Do naturalnych związków o działaniu przeciwpierwotniakowym należy likochalkon A (ryc. 2) znajdujący się w korzeniach lukrecji chińskiej Glycyrrhiza uralensis ( Fabaceae) (26).
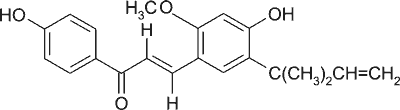
Ryc. 2. Wzór strukturalny likochalkonu A.
Chalkon jest aktywny wobec przedstawicieli rodzajów Plasmodium i Leishmania (23), powodując zmiany w strukturze i funkcji mitochondriów obydwu pasożytów (7, 26). Związek ten oraz jego pochodne hamują oddychanie pierwotniaków poprzez ograniczenie zużycia tlenu (7, 26), akumulację dwutlenku węgla, obniżanie pH (26) i hamowanie aktywności mitochondrialnych dehydrogenaz (7, 26). Obecnie uważa się, że enzymy łańcucha oddechowego pasożytów mogą być punktem uchwytu dla działania przeciwpierwotniakowego. Innym mechanizmem działania likochalkonu A jest hamowanie replikacji DNA (7). W badaniach prowadzonych na chomikach wykazano, że likochalkon A oraz utlenione chalkony hamują w wątrobie i śledzionie wzrost postaci promastigotów i amastigotów Leishmania major i L. donovani, przy czym działanie na amastigoty jest silniejsze. Efekt ten może być konsekwencją bezpośredniego wpływu na mechanizm obronny amastigotów przebywających w makrofagach lub aktywowania makrofagów do zabijania amastigotów. Ponadto likochalkon A hamuje in vitro wzrost wrażliwych i opornych na chlorochinę pierwotniaków Plasmodium falciparum (7, 20). Wykazano, że w stężeniu 0,6 μg/ml hamuje on rozwój pasożytów w około 50% (7). W przypadku P. yoelii związek podany myszom zarówno dootrzewnowo jak i doustnie w wyższej dawce, ogranicza rozwój choroby.
Szereg syntetycznych chalkonów, m.in. 4-chlorochalkon, wykazuje działanie przeciwpierwotniakowe przeciw Leishmania brasiliensis i Trypanosoma cruzi, jednocześnie nie wywołując efektu cytotoksycznego w stosunku do mysich makrofagów (25). Z kolei 2´4´-dihydroksy-4-metoksychalkon, 2´-hydroksy-3,4-dimetoksychalkon oraz 2-hydroksy-4,4´-dimetoksychalkon hamują przeżywalność Leishmania donovani, działając toksycznie na makrofagi (22). Chalkony, których pierścień A stanowił podstawnik nitrofenylowy, a pierścień B układ indolu z grupą metylową, wykazują aktywność przeciw Entamoeba histolityca i Trichomonas vaginalis (7).
Działanie przeciwzapalne
Niektóre chalkony, m.in. 2´-hydroksy- i 2´,5´-dihydroksychalkony, przez hamowanie aktywacji mastocytów, neutrofili i makrofagów, wykazują działanie przeciwzapalne (30). Podobnie, zależnie od dawki, hamują degranulację mastocytów 2´,3-dihydroksychalkon, 2´-hydroksy-3,4-dimetoksychalkon, 3´-hydroksy-3,4-dimetoksychalkon i 2´,5´-dihydroksy-3,4-dimetoksychalkon (2). Wykazano, że większość badanych hydroksychalkonów blokowała uwalnianie β-glukuronidazy i lizozymu z neutrofili szczurów (2, 30). 2´,5´-Dihydroksychalkony, podobnie jak dialkoksychalkony, są inhibitorami tlenku azotu. 2´,4´-Dihydroksy-5´-karboksychalkon, a także jego analogi zawierające grupę -OH w pozycji C-2 oraz grupy -OH w pozycji C-4 i -COOH w pozycji C-3, wykazują właściwości przeciwzapalne oraz wzmacniające naczynia kapilarne (7). Wykazano brak zależności między obserwowanym działaniem przeciwzapalnym związków a uwalnianiem przez nie hormonów z nadnerczy (2).
Chalkony hamują biosyntezę interleukiny-1, która jest aktywna w stanach zapalnych i uwalniana w odpowiedzi na obecność drobnoustrojów i antygenów (7). Przykładem takiego związku jest 2´,4´,6´-trimetoksychalkon. Syntetyczne analogi tego związku wywierają jednak niewielki wpływ na 5-lipooksygenazę i cyklooksygenazę.
Niektóre związki z grupy chalkonów, np. 4-metylochalkon, wykazują aktywność przeciwzapalną porównywalną z ibuprofenem, przy nieznacznym działaniu przeciwbólowym i braku działania przeciwgorączkowego (7). Związek ma również zdolność do zmiatania anionu nadtlenkowego, nie działając jednak na rodnik hydroksylowy (7).
2´,3-Dihydroksychalkon i 4-chloro-2´,5´-dihydroksychalkon hamowały rozwój stanu zapalnego w teście obrzęku tylnej kończyny u myszy (2). Natomiast likochalkon A wywierał działanie przeciwzapalne w obrzęku ucha u myszy wywołanym kwasem arachidonowym lub TPA (13-octan-12-O-tetradekanoiloforbolu) (7).
Działanie przeciwhistaminowe
Floretyna (ryc. 3) hamuje, wywołane przez TPA i aplyzjatoksynę, uwalnianie histaminy z bazofili (7). Chalkon ten jest inhibitorem enzymu kinazy proteinowej C, która wiążąc się z TPA i aplyzjatoksyną, powoduje uwalnianie mediatorów stanu zapalnego. Działanie przeciwalergiczne wykazują również 2´-hydroksychalkony, strukturalnie podobne do kromoglikanu disodowego.
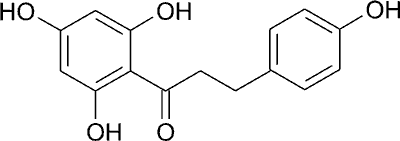
Ryc. 3. Wzór strukturalny floretyny.
Działanie immunosupresyjne
Spośród chalkonów działanie immumosupresyjne wykazano dla likochalkonu A (ryc. 2) i niektórych jego syntetycznych pochodnych (20). Hamują one proliferację limfocytów (7) oraz wytwarzanie cytokin, zarówno prozapalnych (TNF-α, IL-1, IL-6), jak i przeciwzapalnych (IL-10), nie wywierając wpływu na ich uwalnianie (20). W związku z powyższym działaniem, związki te mogą znaleźć zastosowanie w chorobach o podłożu autoimmunizacyjnym oraz w przeszczepach. W przypadku stosowania likochalkonu A (ryc. 2), jako leku w zakażeniu pierwotniakami, wystąpienie efektu immunosupresyjnego jest działaniem niepożądanym.
Działanie przeciwnowotworowe
Aktywność przeciwnowotworową chalkonów badano na zwierzętach w modelu chemicznie indukowanej karcynogenezy. Stosowano jednocześnie dwa związki: DMBA (7,12-dimetylobenzo(a)antracen) i TPA (13-octan-12-O-tetradekanoiloforbolu), stymulując inicjację zmian nowotworowych DMBA, a ich dalszy rozwój przy użyciu TPA. Inną kombinację karcynogenów stanowiły: N-metylo-N-nitrozomocznik (MNU) i benzo(a)piren (BP) (5).
Działanie przeciwnowotworowe w raku skóry u myszy stymulowanym TPA wykazywał zespół chalkonów z soku z łodyg Angelica keiskei ( Umbelliferae), zawierający ksantoangelol (ryc. 4), 4-hydroksyderrycynę (ryc. 4), ksantoangelol F, ksantoangelol H oraz izobawachalkon (ryc. 5) (5).
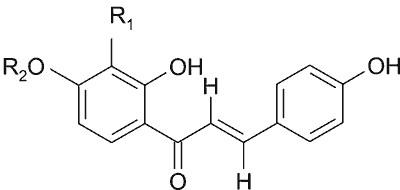
Ryc. 4. Wzory strukturalne:
ksantoangelolu:
R1 = CH2CH=C(CH3)CH2CH2CH=C(CH3)2; R2 = H
4-hydroksyderrycyny:
R1 = CH2CH=C(CH3)2; R2 = CH3
aszitaby:
R1 = CH2CH(COOH)C(CH3)=CH2; R2 = CH3.
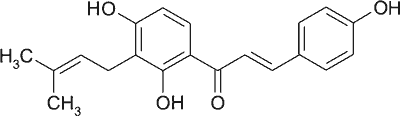
Ryc. 5. Wzór strukturalny izobawachalkonu.
Chalkony w stężeniu 1?103 moli powodowały około 92-100% zahamowanie zmian nowotworowych, a w stężeniu 5?102 moli około 51-84%. Najwyższą (100% przy stężeniu 1?103 moli) aktywnością spośród badanych chalkonów charakteryzowały się: izobawachalkon i 4-hydroksyderrycyna, przy jednoczesnym efekcie ochronnym na zdrowe komórki w zakresie od 60% do 70% (5). Działanie ksantoangelolu i aszitaby (ryc. 4), hamujące rozwój nowotworu skóry u myszy indukowanego DMBA i TPA, przypisuje się działaniu antagonistycznemu w stosunku do układu Ca2+ – kalmodulina (7). 3,4,2´,4´-Tetrahydroksychalkon, 3,4,2´-trihydroksychalkon i 3,4,4´-trihydroksychalkon oraz 3,4-dihydroksychalkon, w modelu nowotworu skóry stymulowanym DMBA i TPA, hamowały rozwój zmian nowotworowych (7). Te same związki badano na myszach z nowotworem płuc stymulowanym benzo(a)pirenem (7). Po 21 tygodniach podawania chalkonów odnotowano poprawę stanu zdrowia u 29% myszy (7, 12, 13). Podobnie w badaniach na szczurach z nowotworem piersi, stymulowanym MNU (N-metylo-N-nitrozomocznik), po 17 tygodniach kuracji obserwowano poprawę stanu zdrowia u 49% badanych zwierząt (7, 13). Natomiast inne chalkony, m.in. 3´- oraz 4´-metylo-3-hydroksychalkon, hamują in vitro rozwój nowotworu szyjki macicy (linia komórek HeLa) oraz in vivo rozwój raka skóry u myszy, inicjowanego DMBA (11).
Do chalkonów o właściwościach przeciwnowotworowych należą: izolikwirytygenina (ryc. 6), 3-hydroksy-3´-metylochalkon oraz 3-hydroksy-3´,4´-dimetylochalkon (7).
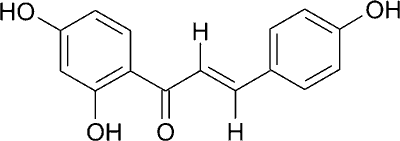
Ryc. 6. Wzór strukturalny izolikwirytygeniny.
2-Hydroksychalkon ogranicza rozwój nowotworu jamy ustnej u szczurów inicjowanego 1-tlenkiem 4-nitrochinoliny (7). Działanie przeciwnowotworowe chalkonów związane jest także z ich aktywnością antyestrogenną (31).
Działanie antymitotyczne
Jednym z mechanizmów działania przeciwnowotworowego jest hamowanie podziałów mitotycznych komórek nowotworowych poprzez blokowanie tworzenia wrzeciona podziałowego lub zahamowanie jednej z faz cyklu życiowego komórki (7).
Pedycyna (ryc. 7), występująca w roślinie Fissistigma lanuginosum ( Annonaceae), obok fizystyny i izofizystyny, wykazuje działanie hamujące polimeryzację tubuliny do mikrotubul, w tworzeniu wrzeciona podziałowego podczas mitozy (w profazie) (3).
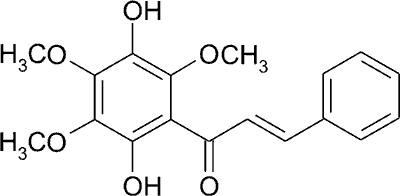
Ryc. 7. Wzór strukturalny pedycyny.
Wyodrębniona z korzeni Calythropsis aurea ( Myrtaceae) kalitropsyna (ryc. 8) wykazuje słaby efekt antymitotyczny, przypuszczalnie poprzez wpływ na polimeryzację tubuliny (32).
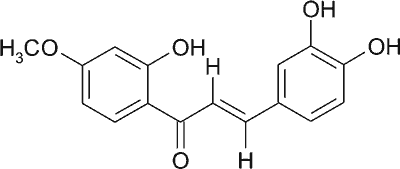
Ryc. 8. Wzór strukturalny kalitropsyny.
1-(2,5-Dimetoksyfenylo)-3-(4-(dimetylamino)fenylo)-2-propen-1-on oraz grupa chalkonów o zbliżonej budowie wykazują działanie antymitotyczne (8). Związek ma większe powinowactwo do tubuliny niż alkaloidy barwinka ( Cataranthus roseus, Apocynaceae). W warunkach in vivo jego działanie było porównywalne z działaniem winblastyny. Z kolei 1-(2,5-dimetoksyfenylo)-3-(4-(dimetylamino)fenylo)-2-propen-1-on hamuje u szczurów rozwój białaczki opornej na działanie adriamycyny i winblastyny oraz u chomików rozwój nowotworu jajnika opornego na winblastynę.
2´,5´-Dimetoksy-4-dimetylaminochalkon (MDL 27048) silnie i odwracalnie wiąże się z tubuliną (7), hamując tworzenie mikrotubul i w efekcie blokując mitozę. Uważa się, że jest to związane z obecnością grupy 2´,5´-dimetoksyfenylowej, wiążącej tubulinę, podobnie jak w przypadku kolchicyny i podofilotoksyny. 2´,5´-Dimetoksy-4-dimetylaminochalkon podawany w dawkach od 6,25 do 50 mg/kg zwiększa przeżywalność myszy z zaszczepioną białaczką odpowiednio w zakresie od 26 do 54%, (7). Innym potencjalnym cytotostatykiem jest wiążący się z tubuliną 3,4,3´,4´,5´-pentametoksychalkon (9).
2-Hydroksychalkon, 2´-hydroksychalkon, 4,2´-dihydroksychalkon, 2´,6´-dihydroksy-4´-metoksychalkon, 3,4,2´,4´-tetrahydroksychalkon i 4,2´,4´,6´-tetrahydroksychalkon wykazują działanie cytotoksyczne silniejsze od 5-fluorouracylu (IC50 = 50 μM), odpowiednio w zakresie IC50 od 2 do 23 μM (7). Spośród analizowanych związków 3,4,2´,4´-tetrahydroksychalkon charakteryzował się najwyższą aktywnością hamowania syntezy DNA, RNA i białek.
3-Hydroksy-3´-metylochalkon wykazuje cytotoksyczność w stosunku do linii nowotworów żołądka oraz raka szyjki macicy, trzustki i nowotworu układu nerwowego u dzieci. Związek ten powoduje zwiększenie liczby komórek w fazie S i blokadę przejścia z fazy S do fazy G2 (7).
Działanie antyinwazyjne
Związki hamujące rozprzestrzenianie się komórek raka piersi, poprzez ich selektywne niszczenie, są obiektem badań naukowych, jako potencjalne leki w terapii nowotworów (10). Uważa się, że za działanie antyinwazyjne są odpowiedzialne m.in. grupy prenylowe. 2´,4´-Dimetoksy-5´-prenylochalkon, 2´-hydroksy-4´,5´,6´-trimetoksychalkon oraz związki 85 i 88 (10) (ryc. 9) hamują rozprzestrzenianie się komórek raka piersi na komórki serca, wykazując cytotoksyczność wobec komórek rakowych oraz niewielką toksyczność wobec komórek mięśnia sercowego (10). W przypadku stosowania 2´,4´-dimetoksy-5´-prenylochalkonu i 2´-hydroksy-4´,5´,6´-trimetoksychalkonu następuje przyrost masy komórek serca przy zachowanej, normalnej ich wielkości. Działanie 2´,4´-dimetoksy-5´-prenylo- i 2´-hydroksy-4´,5´,6´-trimetoksychalkonów, hamujące wzrost komórek rakowych, nie wynika ze stymulacji apoptozy, natomiast jest spowodowane zwiększoną agregacją komórek nowotworowych (10).
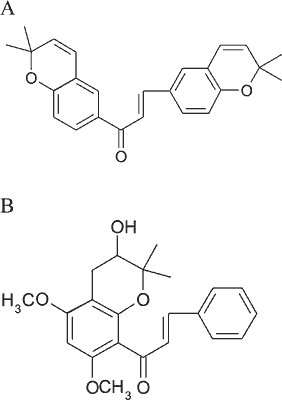
Ryc. 9. Wzory strukturalne związków: A – 85 i B – 88 (10).
Działanie przeciwbakteryjne
Chalkony i ich analogi, z grupami hydroksylowymi i metoksylowymi w pierścieniach aromatycznych, wykazują właściwości przeciwbakteryjne (7). Pochodne 2´-hydroksychalkonów wykazują wysoką aktywność przeciwbakteryjną w stosunku do drobnoustrojów chorobotwórczych roślinnych i zwierzęcych (19).
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
29 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
69 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
129 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 78 zł
Piśmiennictwo
1. Tomas-Barberan F.A., Clifford M.N.: Flavanones, chalcones and dihydrochalcones – nature, occurence and dietary burden. J. Sci. Food Agric. 2000, 80, 1073. 2. Hsieh H.K. et al.: Synthesis and anti-inflamatory effect of chalcones and related compounds. Pharm. Res. 1998, 15, 39. 3. Iwashina T.: The structure and distribution of the flavonoids in plants. J. Plant Res. 2000, 113, 287. 4. Kohlmünzer S.: Farmakognozja. Wydawnictwo lekarskie PZWL, Warszawa 1998. 5. Akihisa T. et al.: Chalcones, coumarins, and flavanones from the exudate of Angelica keiskei and their chemopreventive effects. Cancer Lett. 2003, 201, 133. 6. Alias Y. et al.: An antimitotic and cytotoxic chalcone from Fissistigma lanuginosum.J. Nat. Prod. 1995, 58, 1160. 7. Dimmock J.R. et al.: Bioactivities of chalcones. Curr. Med. Chem. 1999, 6, 1125. 8. Edwards M.L., et al.: Chalcones: A new class of antimitotic agents. J. Med. Chem. 1990, 33, 1948. 9. Lawrence N.J. et al.: The interaction of chalcones with tubulin. Anticancer Drug Res. 2000, 15, 135. 10. Parmar V.S. et al.: Anti-invasive activity of alkaloids and polyphenolics in vitro. Bioorg. Med. Chem. 1997, 5, 1609. 11. Shibata S.: Anti-tumorigenic chalcones. Stem. Cells 1994, 12, 44. 12. Wattenberg L.: Chalcones, myo-inositol and other novel inhibitors of pulmonary carcinogenesis. J. Cell Biochem. Suppl. 1995, 22, 162. 13. Wattenberg L.W. et al.: Inhibition of carcinogen-induced pulmonary and mammary carcinogenesis by chalcone administered subsequent to carcinogen exposure. Cancer Lett. 1994, 83, 165. 14. Alcaraz L.E. et al.: Antibacterial activity of flavonoids against methicillin-resistant Staphylococcus aureus strains. J. Theor. Biol. 2000, 205, 231. 15. De Los Angeles Alvarez M. et al.: Bacteriostatic action of synthetic polyhydroxylated chalcones against Escherichia coli.Biocell. 2004, 28, 31. 16. Devia C.M. et al.: Structure-biological activity relationship of synthetic trihydroxilated chalcones. Rev. Microbiol. 1998, 29, 307. 17. Popova M. et al.: New bioactive chalcones in propolis from El Salvador. Z. Naturforsch. C. 2001, 56, 593. 18. Sato M. et al.: Growth inhibition of oral bacteria related to denture stomatitis by anti-candidal chalcones. Australian Dental J. 1997, 42, 343. 19. Vibhute Y.B., Baseer M.A.: Synthesis and activity of a new series of chalcones as antibacterial agents. Indian J. Chem. B. 2003, 42, 202. 20. Barfod L. et al.: Chalcones from Chinese liquorice inhibit proliferation of T cells and production of cytokines. Int. Immunopharmacol. 2002, 2, 545. 21. Go M.L. et al.: Antiplasmodial chalcones inhibit sorbitol-induced hemolysis of Plasmodium falciparum - infected erythrocytes. Antimicrob. Agents Chemother. 2004, 48, 3241. 22. Kayser O., Kiderlen A.F.: In vitro leishmanicidal activity of naturally occurring chalcones. Phytother. Res. 2001, 15, 148. 23. Kharazmi A. et al.: Discovery of oxygentade chalcones as novel antimalarial agents. Ann. Trop. Med. Parasitol. 1997, 91, 91. 24. Li R. et al.: In vitro antimalarial activity of chalcones and their derivatives. J. Med. Chem. 1995, 38, 5031. 25. Lunardi F. et al.: Trypanocidal and leishmanicidal properties of substitution-containing chalcones. Antimicrob. Agents Chemother. 2003, 47, 1449. 26. Zhai L. et al.: The antileishmanial activity of novel oxygenated chalcones and their mechanism of action. J. Antimicrob. Chemother. 1999, 43, 793. 27. Ko H.H. et al.: Structure-activity relationship studies on chalcone derivatives: Potent inhibition of platelet aggregation. J. Pharm. Pharmacol. 2004, 56, 1333. 28. Lin C.N. et al.: Chalcones as potent antiplatelet agents and calcium channel blockers. Drug Dev. Res. 2001, 53, 9. 29. De la Rocha N. et al.: Cytoprotective effects of chalcones from Zuccagnia punctata and melatonin on the gastroduodenal tract in rats. Pharmacol. Res. 2003, 48, 97. 30. Hsieh H.K. et al.: Synthesis and anti-inflammatory effect of chalcones. J. Pharm. Pharmacol. 2000, 52, 163. 31. Le Bail J.C. et al.: Chalcones are potent inhibitors of aromatase and 17b-hydroxysteroid dehydrogenase activities. Life Sci. 2001, 68, 751. 32. Beutler J.A. et al.: Two new cytotoxic chalcones from Calythropsis aurea.J. Nat. Prod. 1993, 56, 1718. 33. Opletalová V. et al.: Chalcones (1,3-diarylpropen-1-ones) and their analogues as potential therapeutic agents of diseases of the cardiovascular system. Ces. Slov. Farm. 2003, 52, 12. 34. Amor E.C. et al.: Spasmolytic flavonoids from Syzygium samarangenese (Blume) Merr. & L.M. Perry. Z. Naturforsch. C. 2005, 60, 67. 35. Corréa R. et al.: Antinociceptive properties of chalcones. Structure-activity relationships. Archiv. Pharmazie. 2001, 334, 332.









