© Borgis - Postępy Nauk Medycznych 6/2006, s. 344-358
*Jaromir Wasyluk
Ocena pomiarów grubości warstwy włókien nerwowych siatkówki wykonywanych za pomocą dwu różnych, skaningowych polarymetrów laserowych GDx FCC i GDx VCC u pacjentów z wczesną jaskrą pierwotną otwartego kąta i nadciśnieniem ocznym
Evaluation of the retinal nerve fiber layer measurements performed with two different scanning laser polarimeters GDx FCC and GDx VCC in patients with early primary open angle glaucoma and ocular hypertension
NZOZ Centrum Leczenia Jaskry i Chorób Oka w Warszawie
Kierownik: prof. dr hab. med. Krystyna Czedrowicz-Janicka
Streszczenie
Jaskra pierwotna otwartego kąta (JPOK) to neuropatia degeneracyjna nerwu wzrokowego, a zarazem choroba społeczna, będąca pierwszą przyczyną nieodwracalnej ślepoty w krajach cywilizowanych. Nadciśnienie oczne (NO) jest stanem izolowanego, podwyższonego ciśnienia śródgałkowego, mogącego w niektórych przypadkach prowadzić do jaskry. Skaningowa polarymetria laserowa umożliwia wykrycie najwcześniejszych postaci tych chorób i ich wzajemnego rozróżnienia, a także stopnia zaawansowania i szybkości progresji choroby, poprzez badanie pierwszego ogniwa neuropatii - degeneracyjnych ubytków włókien komórek zwojowych siatkówki. W niniejszej pracy badano i porównywano wiarygodność kliniczną dwóch dostępnych polarymetrów laserowych w dwóch grupach chorych - z wczesną postacią JPOK i NO. Wiarygodność pomiarów określano m.in. wobec pomiarów morfologicznych tarczy nerwu wzrokowego w laserowej oftalmoskopii skaningowej HRT i badania pola widzenia w statycznej progowej perymetrii komputerowej Octopus 101. W celu określenia wpływu rogówki na pomiary polarymetryczne, wykonano także pomiar jej grubości centralnej - pachymetrię. Stwierdzono znamienne rozbieżności w wynikach między dwoma aparatami w pomiarach u tych samych chorych. Wykazano lepszą korelację wyników polarymetru typu GDx VCC z innymi wskaźnikami klinicznymi. Nie wykazano znaczącego wpływu centralnej grubości rogówki na najistotniejsze parametry polarymetryczne.
Summary
Primary open angle glaucoma (POAG) is a degenerative optic nerve neuropathy and the social disease by WHO, being the first cause of irreversible blindness in developed countries. Ocular hypertension (OH) is a state of isolated, elevated intraocular pressure, which in some cases may lead to glaucoma. Scanning laser polarimetry enables the earliest detection of above mentioned diseases and its differentiation as well as estimating the degree of advancement and severity of progression. It can be achieved by measuring degenarative loss of retinal ganglion cell fiber layer - the first element in glaucoma pathway. In this study clinical accuracy of two different scanning laser polarimeters were evaluated and compared in two groups of patients - early POAG and OH. Clinical accuracy was identified considering optical nerve head measurements by scanning laser ophthalmoscopy HRT and visual field examination by static threshold automated perimetry. Central corneal thickness was also measured by pachymetry to evaluate its influence on the polarimetry indices. Significant differences between two polarimeters in the same patients measurements were detected. GDx VCC results seems to have better correlation with other clinical indices. No significant influence of central corneal thickness on main polarimetric indices was observed.

1. WSTĘP
1.1. Jaskra pierwotna otwartego kąta
Jaskra pierwotna otwartego kąta (JPOK) to grupa postępujących neuropatii nerwu wzrokowego z charakterystycznymi, morfologicznymi zmianami tarczy nerwu wzrokowego i warstwy włókien nerwowych siatkówki, przy braku innych chorób narządu wzroku i wrodzonych anomalii. Zmianom tym towarzyszy postępująca utrata komórek zwojowych siatkówki i charakterystyczne ubytki w polu widzenia (wg Europejskiego Towarzystwa Jaskrowego EGS, 2003) (1, 2).
Jaskra (JPOK) jest pierwszą przyczyną nieodwracalnej ślepoty w krajach cywilizowanych – z jej powodu niewidomych jest ok. 7 mln. osób. Przez WHO uznana jest za chorobę społeczną. Szacuje się, że w Polsce świadoma choroby i leczona jest co dziesiąta osoba wśród ok. 700 tys. chorych (dane z programu „Usprawnienie wczesnej diagnostyki i zwiększenie efektywności leczenia jaskry w Polsce” realizowanego przez Klinikę Okulistyki CMKP pod patronatem Ministerstwa Zdrowia w latach 1998-2001, koordynator prof. dr hab. med. Krystyna Czechowicz-Janicka).
Największym problemem w jaskrze jest wciąż zbyt późno stawiana diagnoza. W dalszym ciągu, mimo ogromnego postępu w badaniach nad jaskrą, który dokonał się w ostatnich latach, nie wiemy do końca, jaki jest patomechanizm tej neuropatii i nie potrafimy w sposób powtarzalny prognozować jej przebiegu (3, 4).
W niniejszej pracy określenie „jaskra” odnosi się do najczęściej występującej i najgroźniejszej jej postaci – jaskry pierwotnej otwartego kąta (JPOK). Jest to choroba bezobjawowa lub prawie bezobjawowa – aż do momentu wystąpienia znacznych ubytków w polu widzenia, zaczynających utrudniać normalne funkcjonowanie chorego. Późna diagnoza – to najczęstsza przyczyna niepowodzenia w leczeniu, gdyż powstałych zmian nie da się już cofnąć, a szybkość progresji jest zwykle proporcjonalna do stopnia zaawansowania choroby. Uszkodzenie pola widzenia jest przez długi czas niedostrzegane przez chorego, ponieważ stopniowe narastanie względnych, a następnie bezwzględnych ubytków czułości siatkówki, postępuje na ogół asymetrycznie, od obwodu pola widzenia i trwa przez lata, a niekiedy nawet przez dziesiątki lat. Szacuje się, że chorobowość w grupie osób 40-45 letnich wynosi 2%, wzrastając do 10% w populacji powyżej 70 roku życia (5, 6).
Definicja jaskry ulegała przez lata znacznym przeobrażeniom. Najbardziej dynamiczny rozwój badań nad tą chorobą to ostatnie dziesięciolecia – w tym czasie wyodrębniono geny, pozwalające określić obciążenie dziedziczne jaskrą lub odpowiedzialne za dynamikę jej przebiegu. Przeprowadzono też szereg badań, dowodzących jej wieloczynnikowej etiopatogenezy, a także stworzono nowoczesny arsenał badań i urządzeń diagnostycznych pozwalających na wczesną diagnostykę (5, 6).
W jaskrze pierwotnej otwartego kąta wyróżnia się czynniki ryzyka zachorowania na jaskrę, jak i wykryte w ostatnim czasie – czynniki ryzyka progresji jaskry (7). Czynniki ryzyka zachorowania na jaskrę można podzielić na ogólne i miejscowe. Do czynników ogólnych należą: dziedziczenie, wiek powyżej 60 lat, płeć żeńska, rasa czarna, nadciśnienie i niedociśnienie tętnicze, zespoły naczynioskurczowe (migreny, zespół Raynaud´a), przewlekły stres, zespół bezdechu sennego, cukrzyca i zaburzenia gospodarki lipidowej. Wśród miejscowych czynników ryzyka wyróżniamy m.in.: podwyższone ciśnienie wewnątrzgałkowe, lokalne zaburzenia krążenia w gałce ocznej i krótkowzroczność> – 4.0 dioptrii. Czynniki ryzyka progresji jaskry to przede wszystkim: płeć żeńska, wysokie ciśnienie wewnątrzgałkowe, migreny, krwotoczki na tarczy nerwu II, zanik okołotarczowy.
We współczesnej definicji jaskry nie wspomina się już o ciśnieniu wewnątrzgałkowym, jako jedynym czynniku sprawczym uszkodzenia nerwu II, choć obniżanie tegoż ciśnienia nadal pozostaje główną metodą leczenia, zarówno zachowawczego, jak i zabiegowego (8-10). W ostatnich latach szczególnie podkreśla się znaczenie naczyniopochodnego podłoża etiopatogenetycznego jaskry, na tle zarówno trwałych (sklerotyczne zwężenie drobnych naczyń tętniczych w nadciśnieniu tętniczym, hiperlipidemii), jak i przejściowych (lokalny skurcz naczyniowy, dekompensacja autoregulacji siatkówkowo-naczyniowkowej, hipotonia tętnicza) zaburzeń ukrwienia głowy nerwu wzrokowego i komórek zwojowych siatkówki (11-13). Wyodrębnienie w jaskrze pierwotnej otwartego kąta „podjednostki” – jaskry z normalnym ciśnieniem wewnątrzgałkowym (JNC) – dowodzi możliwości uszkodzenia jaskrowego niezależnie od poziomu ciśnienia (14). W neuropatii, występującej w jaskrze z normalnym ciśnieniem wewnątrzgałkowym, pierwszoplanową rolę odgrywają mechanizmy naczyniopochodne, prawdopodobnie zależne głównie od gry neuro-hormonalnej na poziomie ogólnym oraz tkankowym (mediatory śródbłonkowopochodne, autoregulacja łożyska kapilarnego siatkówki) (15-18).
Największy nacisk kładzie się obecnie na końcowy efekt wspólny neuropatii – niezależnie od jej podłoża – zmiany morfologiczne głowy nerwu wzrokowego, a wcześniej – warstwy włókien komórek zwojowych siatkówki, skutkujące powstawaniem funkcjonalnego uszkodzenia wzroku, pod postacią ubytków w polu widzenia.
1.2. Nadciśnienie oczne
Termin „nadciśnienie oczne” po raz pierwszy został użyty w 1962 roku przez Drance´a, a w literaturze anglojęzycznej zdefiniowany przez Perkinsa w roku 1966. Według do dziś obowiązującej definicji, jest to stan oka, w którym istnieje podwyższone ponad górną granicę statystycznej normy (21 mmHg) ciśnienie wewnątrzgałkowe, przy braku patologicznych zmian zarówno w badaniu pola widzenia, morfologii głowy nerwu wzrokowego, jak i we włóknach nerwowych siatkówki. Kąt przesączania w oku jest szeroki i otwarty. Nie stwierdza się także innych chorób oka, mogących powodować wtórny wzrost ciśnienia wewnątrzgałkowego.
Wieloośrodkowe, prospektywne i największe, jak dotąd, badania nad nadciśnieniem ocznym (OHTS – Ocular Hypertension Treatment Study, zakończone w roku 2002), wskazują na możliwość progresji nadciśnienia ocznego we wczesną jaskrę w przypadku braku stosowania zachowawczego leczenia hipotensyjnego (19). Byłoby to sprzeczne z dotychczasowym stanowiskiem światowych autorytetów okulistycznych, według których nadciśnienie oczne, jako rodzaj anomalii w granicach fizjologii, należy jedynie obserwować, a nie leczyć.
W kontekście niniejszej pracy warto zwrócić uwagę, że definicja tego stanu powstawała w czasach, gdy nie było jeszcze dostępnych badań, pozwalających na dokładny ilościowy pomiar i wykrywanie najwcześniejszych ubytków w warstwie włókien nerwowych siatkówki – czyli pierwszego ogniwa w kaskadzie neuropatii jaskrowej (20).
Szczególną uwagę zwraca się obecnie na rolę badania grubości rogówki (pachymetrii) w diagnostyce nadciśnienia ocznego (21), jak również jaskry z normalnym ciśnieniem (22, 23) oraz weryfikacji wcześniej postawionych rozpoznań. Zbyt gruba rogówka może fałszować dodatnio, a zbyt cienka – ujemnie – wyniki pomiaru ciśnienia wewnątrzgałkowego, będącego tu głównym kryterium klasyfikacji (24-30). Niektóre prace (przede wszystkim wspomniane powyżej – OHTS) sugerują, że mała grubość rogówki sama w sobie jest ważnym czynnikiem ryzyka progresji neuropatii jaskrowej (być może z powodu aktywacji metaloproteinaz w gałce ocznej), jak również ewentualnego przekształcenia się nadciśnienia ocznego w jaskrę (31).
Obecnie uważa się, że grupa pacjentów z nadciśnieniem ocznym nie jest homogenna – istnieją w niej podgrupy bardziej niż inne zagrożone powstaniem neuropatii – osoby obciążone chorobami układu krążenia, z cienkimi rogówkami czy z ciśnieniem wewnątrzgałkowym przekraczającym 30 mmHg (32).
Istnieje prawdopodobieństwo, że nadciśnienie oczne i jaskra to jedynie etapy tej samej choroby. Możliwe jest, że nadciśnienie oczne jest swego rodzaju bezobjawowym „wstępem” mogącym, u osób predysponowanych, prowadzić do jaskry pre-perymetrycznej – to znaczy takiej, w której istnieje już uszkodzenie komórek zwojowych, jednak bez widocznego odzwierciedlenia w standardowych badaniach pola widzenia (33). Jaskra taka – nieleczona – może z kolei przekształcić się w klasyczną jaskrę z ubytkami w polu widzenia. Podstawowym problemem lekarskim w obserwacji osób z nadciśnieniem ocznym jest „wyłapanie” pacjentów, u których wystąpiło już ścieńczenie warstwy włókien nerwowych siatkówki, bowiem osoby te należą do grupy szczególnie zagrożonej rozwinięciem jaskry pierwotnej otwartego kąta w najbliższej przyszłości.
Być może, wprowadzenie do szerszej diagnostyki polarymetrycznego skaningu laserowego włókien nerwowych siatkówki, pozwoli w przyszłości, kolejny raz, zmodyfikować definicje jaskry i nadciśnienia ocznego. Stworzenie metody diagnostycznej, mogącej w wiarygodny sposób wykryć jaskrę na etapie początkowym, czyli ubytków w warstwie aksonów komórek zwojowych siatkówki, byłoby równoznaczne z sukcesem w leczeniu, jako że jedynie wczesne wdrożenie terapii może uchronić potencjalnych chorych przed uszkodzeniem pola widzenia (35). Dotyczy to szczególnie osób obciążonych czynnikami ryzyka, z których głównym jest podwyższone ciśnienie wewnątrzgałkowe.
W grupie osób z nadciśnieniem ocznym – z jednej strony wczesne, niejako „profilaktyczne”, włączenie leku może zapobiec rozwojowi jaskry u pacjentów do niej predysponowanych, z drugiej – nieprawidłowa diagnoza i niepotrzebne leczenie spowoduje u tych, u których jaskra nigdy by się nie rozwinęła, stres i znaczne pogorszenie jakości życia (36). Jak odróżnić jednych od drugich?
Metoda pomiarowa zmian morfologicznych komórek zwojowych siatkówki powinna być swoista, czuła i powtarzalna. Powinna być także jak najmniej podatna na błędy, wynikające z indywidualnych uwarunkowań anatomicznych oka, jak przezierność ośrodków optycznych czy osobnicze różnice parametrów układu optycznego (np. grubość i dwójłomność rogówki). Duże nadzieje pokładane są w laserowych polarymetrach skaningowych, obecnie najdokładniejszych narzędziach diagnostycznych, służących do obrazowania warstwy włókien nerwowych siatkówki i pozwalających na śledzenie dynamiki jej ubytków u chorych z najwcześniejszymi postaciami jaskry i nadciśnieniem ocznym (37, 38).
1.3. Warstwa włókien nerwowych siatkówki i polarymetria laserowa
Warstwa włókien nerwowych (w.w.n.), znajdująca się w powierzchownej części siatkówki (ryc. 1), ma budowę tubularną – składa się z początkowo bezrdzennych aksonów komórek zwojowych, których początek stanowią ciała komórkowe leżące w warstwie zwojowej siatkówki, koniec zaś – synapsy znajdujące się w ciele kolankowatym bocznym mózgu. Włókna nerwowe, w liczbie 1,2-1,4 mln., zbiegają się w tarczy nerwu wzrokowego w postaci otaczającego ją pierścienia nerwowo-siatkówkowego. Włókna przewodzące bodźce z obwodowych rejonów dna oka leżą głębiej w w.w.n i bardziej obwodowo w pierścieniu nerwowo-siatkówkowym i nerwie wzrokowym. Włókna przewodzące impulsy z centralnej siatkówki – znajdują się odpowiednio płyciej w w.w.n. i przyosiowo w nerwie II. Włókna nerwowe siatkówki, ciała komórek zwojowych i komórki dwubiegunowe należą to tzw. części mózgowej siatkówki (stratum cerebrale).
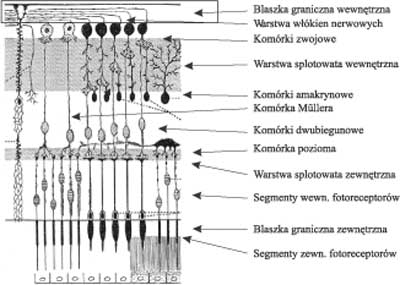
Ryc. 1. Komórki nerwowe siatkówki w przekroju poprzecznym. Zakres badania polarymetrycznego.
Komórki zwojowe siatkówki dzielą się na podtypy ze względu na swą budowę, rodzaj odbieranych bodźców i miejsce docelowego regionu, osiąganego przez ich włókna w ciele kolankowatym bocznym w mózgowiu. Najważniejsze ich subpopulacje to komórki typu magnocellular – M (warstwy 1 i 2), parvocellular – P (warstwy 3-6) i subklasa – koniocellular (międzyblaszkowe, między komórkami M i P) (39).
Zaopatrzenie tego rejonu (w.w.n., komórek zwojowych, a także częściowo komórek dwubiegunowych) w krew tętniczą, pochodzi głównie z odgałęzień tętnicy środkowej siatkówki, co jest istotne ze względu na patomechanizm neuropatii jaskrowej. Zarówno główne naczynia tętnicze, jak i żylne leżą w warstwie zwojowej siatkówki. Ich odgałęzienia sięgają do warstwy splotowatej zewnętrznej, od którego to miejsca rolę zaopatrzenia naczyniowego siatkówki przejmuje naczyniówka.
Skaningowa polarymetria laserowa jest techniką badawczą wprowadzoną do diagnostyki jaskry około 1998 roku pod nazwą GDx (ang. Glaucoma Detection). Za jej pomocą możliwe jest zbadanie grubości warstwy włókien komórek zwojowych siatkówki (in. warstwy włókien nerwowych – w.w.n.), pomiar ewentualnych ubytków, zobrazowanie jej rozkładu wokół tarczy nerwu II, a także odniesienie wyników do normatywnej bazy danych, za pomocą multianalizy kilkudziesięciu wskaźników w.w.n. opartej na sieci neuronalnej. Zasada badania opiera się na pomiarze opóźnienia jednej składowej światła spolaryzowanego względem drugiej składowej, prostopadłej do niej. Opóźnienie to uzależnione jest od tego, pod jakim kątem wiązka światła laserowego wnika w dwójłomną, tubularną strukturę w.w.n., i która ze składowych tego światła lepiej „dopasowuje” się do tzw. osi szybkiej. Dwójłomnością chrakteryzują się także niektóre inne struktury gałki ocznej, z których rogówka może powodować największe błędy w badaniu, jako że jej dwójłomność jest znacząca i indywidualnie zmienna. Błędy te konstruktorzy GDx starali się wyeliminować poprzez wbudowanie do aparatu bądź stałego optycznego kompensatora rogówkowego (Fixed Corneal Compensation – GDx typu FCC), bądź kompensatora zmiennego (Variable Corneal Compensation – GDx typu VCC), który ustawia swoją oś estymując oś polaryzacji rogówki z pomiaru włókien nerwowych warstwy Henlego w okolicy plamki. Obydwa aparaty funkcjonują w ośrodkach klinicznych, obydwa mają swoje wady i zalety. Ponieważ ubytki w warstwie włókien nerwowych są pierwszym, subklinicznym objawem neuropatii jaskrowej, dlatego na podstawie wyników badań poarymetrycznych GDx często opiera się decyzja o włączeniu leczenia, jego zaprzestaniu bądź modyfikacji.
2. CELE PRACY
1. Ocena porównawcza parametrów w.w.n. siatkówki, określonych za pomocą dwóch różnych skaningowych polarymetrów laserowych – GDx FCC i GDx VCC, u pacjentów z wczesną jaskrą pierwotną otwartego kąta i nadciśnieniem ocznym oraz wykrycie i pomiar ilościowy ewentualnych niezgodności.
2. Zbadanie korelacji wskaźników GDx z klinicznym obrazem pacjentów, wyrażonym cechami ich pola widzenia w badaniu progowym perymetrii statycznej i cechami morfologicznymi tarczy nerwu wzrokowego w skaningowej oftalmoskopii laserowej.
3. Ocena trafności wskaźników dwóch typów skaningowej polarymetrii laserowej w wykrywaniu zmian charakterystycznych dla wczesnej jaskry.
4. Określenie wpływu centralnej grubości rogówki – czynnika ryzyka progresji jaskry i nadciśnienia ocznego – na powstawanie rozbieżności między wynikami pomiarów, uzyskanych z dwóch różnych skaningowych polarymetrów laserowych.
5. Porównanie przydatności badań aparatami GDx FCC i GDx VCC u pacjentów z nadciśnieniem ocznym w wykrywaniu zmian warstwy włókien nerwowych, mogących sugerować wczesną postać jaskry.
3. MATERIAŁ
Kryteria doboru i charakterystyka badanych pacjentów
Badaniem objęto 70 pacjentów (140 oczu), w tym u 29 (58 oczu) spośród nich występowało nadciśnienie oczne (NO), a u 41 (82 oczu) rozpoznano wczesną jaskrę pierwotną otwartego kąta (JPOK). Wszystkie badane osoby były pacjentami Poradni Jaskrowej Kliniki Okulistyki Centrum Medycznego Kształcenia Podyplomowego w Samodzielnym Państwowym Szpitalu Klinicznym im. Prof. W. Orłowskiego w Warszawie.
Wszyscy pacjenci otrzymali pisemną informację o przebiegu i celu badania, wyrazili na nie pisemną zgodę, a po jego zakończeniu otrzymali informację zwrotną o wynikach wszystkich przeprowadzonych testów.
Badanie zostało zaakceptowane przez Komisję Etyczną CMKP.
Badania aparaturowe przeprowadzono w Klinice Okulistyki CMKP oraz w Centrum Leczenia Jaskry i Chorób Oka w Warszawie.
Badanie przeprowadzono w dwóch niezależnych grupach:
1) 29 pacjentów (58 oczu) z nadciśnieniem ocznym – 21 kobiet i 8 mężczyzn (średnia wieku: 45.2 ± 12.2 lat),
2) 41 pacjentów (82 oczu) z wczesną jaskrą pierwotną otwartego kąta – 26 kobiet i 15 mężczyzn (średnia wieku: 51.8 ± 10.6 lat),
–?Rozpoznanie jaskry pierwotnej otwartego kąta postawione zostało na podstawie:
1) obecności otwartego kąta przesączania – 3, 3/4 lub 4 stopnie (wg Schaffera) w obrazie gonioskopowym,
2) występowania charakterystycznych dla jaskry zmian morfologicznych głowy nerwu wzrokowego: stosunek C/D ≥ 0.5, zblednięcie, ścieńczenie ogólne lub lokalne pierścienia nerwowo-siatkówkowego,
3) zarejestrowanych zmian parametrów w badaniu progowym perymetrii statycznej (Octopus 101, dG2), przynajmniej w jednym oku: wskaźnik MD (Mean Defect – średni ubytek czułości siatkówki)> 2 dB i/lub wskaźnik LV (Loss Variance – wariancja ubytku)> 6 dB, przy wskaźniku wiarygodności RF (Reliability Factor) <15%. Klasyfikacja badanych pól jako posiadających „wczesne uszkodzenie jaskrowe” bazowała na klasyfikacji Hodappa (1, 40, 41) podanej przez Europejskie Towarzystwo Jaskrowe w 2003 roku. W ciągu ostatnich lat stwierdzono możliwość istnienia wczesnej jaskry u chorych nie wykazujących znaczących zmian w polu widzenia (stopień II A wg klasyfikacji Spaetha) (42) – taką postać choroby określono jako tzw. „jaskrę pre-perymetryczną”. W związku z powyższym, do grupy z jaskrą zaliczono także pacjentów z izolowanymi zmianami morfologicznymi głowy nerwu wzrokowego, wykazanymi w laserowej oftalmoskopii skaningowej HRT. Klasyfikacja parametrów głowy nerwu II w tym badaniu oparta jest na sektorowej analizie regresji Moorfields, opracowanej przez Wollstein´a i wsp. (dla aparatu HRT II; opublikowanej w Ophthalmology 1998; 105: 1557-1569) lub na klasyfikacji Mikelberga i wsp. (dla aparatu HRT; opublikowanej w J Glaucoma 1995; 4: 242-247). Przyporządkowuje ona poszczególne części tarczy i całą tarczę nerwu II do grupy „prawidłowej”, „granicznej” lub „nieprawidłowej” przez porównanie do normatywnej bazy danych,. Dla poszczególnych, istotnych przy rozpoznawaniu uszkodzenia jaskrowego parametrów stereometrycznych tarczy, takich jak objętość i powierzchnia rąbka nerwowo-siatkówkowego, powierzchnia przekroju warstwy włókien nerwowych, wskaźnik kształtu zagłębienia, wariancja wysokości konturu tarczy, są automatycznie wyliczone normy, w odniesieniu do normatywnej bazy danych, uwzględniając wiek pacjenta i powierzchnię tarczy w zakresie 1,2-2,8 mm2 (wszystkie badane tarcze mieściły się w tym zakresie). Wg opublikowanych wcześniej prac czułość badania HRT wynosi 62-94%, przy swoistości dla wczesnej jaskry 74-96% (43, 44).
–?Rozpoznanie nadciśnienia ocznego postawione zostało na podstawie:
1) zarejestrowanego kilkukrotnie w okresie obserwacji ciśnienia wewnątrzgałkowego o wartościach> 21 mmHg (zweryfikowanego pomiarem pachymetrycznym rogówki),
2) braku zmian morfologicznych głowy nerwu wzrokowego zarówno w oftalmoskopii pośredniej i laserowej oftalmoskopii skaningowej HRT,
3) braku ubytków w badaniu pola widzenia w perymetrii statycznej (Octopus 101, dG2),
4) brakiem towarzyszących chorób i anomalii ocznych, mogących skutkować wtórnie podwyższonym ciśnieniem wewnątrzgałkowym.
4. METODY
Badanie I
1. Badanie wstępne – kwalifikacyjne (pełne badanie okulistyczne: pomiar ostrości wzroku do dali i bliży, ocena przedniego odcinka oka w biomikroskopii, wziernikowanie dna oka, pomiar ciśnienia wewnątrzgałkowego, gonioskopia).
2. Badanie w.w.n. siatkówki skaningowym polarymetrem laserowym GDx FCC (ryc. 2).

Ryc. 2. Skaningowy polarymetr laserowy GDx FCC i przykładowy wydruk badania włókien nerwowych siatkówki.
3. Badanie pola widzenia komputerowym perymetrem statycznym Octopus 101, strategia progowa dG2, „białe na białym”.
4. Badanie morfologii głowy nerwu II skaningowym oftalmoskopem laserowym HRT.
Badanie II (w odstępie nie dłuższym, niż 14 dni)
1. Badanie morfologii głowy nerwu II skaningowym oftalmoskopem laserowym HRT II u osób, u których nie przeprowadzono badania HRT.
2. Badanie centralnej grubości rogówki pachymetrem ultradźwiękowym Tomey SP 3000.
3. Badanie w.w.n. siatkówki skaningowym polarymetrem laserowym GDx VCC (ryc. 3).
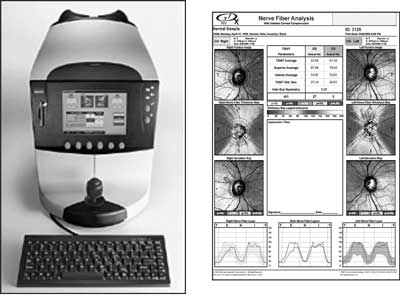
Ryc. 3. Skaningowy polarymetr laserowy GDx VCC i przykładowy wydruk badania włókien nerwowych siatkówki.
Zbiór 17 analizowanych zmiennych (wyjaśnienie skrótów na końcu pracy):
1. Polarymetria laserowa GDx FCC i GDX VCC: N/NFI, EA, S, SN, IR, SR, EM, MM.
2. Oftalmoskopia laserowa HRT/HRTII: RA, RV, MR, RC, C/D, klasyfikacja.
3. Perymetria komputerowa Octopus 101: MD, LV.
4. Pachymetria rogówki: c.g.r.
Główne metody statystyczne:
1) Porównywanie zmiennych pacjentów z 2 grup: JPOK i NO:
– test U – porównywanie średnich z prób niepowiązanych,
– test LL-Manna-Whitneya (nieparametryczny), j.w., gdy rozkład odbiegał od normalnego.
2) Wzajemne zależności zmiennych:
– wyznaczenie liniowości regresji za pomocą testu F-Snedecora,
a) gdy liniowa – obliczano współczynnik korelacji Pearsona,
b) gdy nieliniowa – obliczano współczynnik korelacji rang.
3) Określenie parametrów trafności wskaźników polarymetrii:
– zbadanie czułości, swoistości, wyników fałszywie (+) i (–).
4) Badanie wartości diagnostycznej wskaźników z najwyższym stopniem trafności (N I EA):
– określenie predykcji dodatniej (PPV%) i ilorazu wiarygodności wyników dodatnich (PLR).
5. WYNIKI
5.1. Ocena porównawcza wybranych parametrów w.w.n. siatkówki, określonych za pomocą dwóch różnych skaningowych polarymetrów laserowych u pacjentów z wczesną JPOK i NO oraz wykrycie i pomiar ilościowy ewentualnych niezgodności.
Przy aparacie VCC wartości większości parametrów (SR, IR, SN, MM i EM) przewyższają analogiczne parametry tych wskaźników przy aparacie FCC, niektóre ponad dwukrotnie. Z kolei średnia parametru N przy aparacie FCC stanowi dwukrotną wielokrotność średniej przy VCC. W aparacie FCC istotnie częściej, niż w VCC notowano wyniki nieprawidłowe i na granicy normy. Dziewięć par wskaźników jest ze sobą wysoce powiązanych w przypadku badania aparatem FCC i siedem par wskaźników, gdy były one określane aparatem VCC. Związki między wskaźnikami przy VCC są silniejsze, a trzy pary spośród nich osiągają nawet stopień korelacji prawie pełnej. Nie stwierdzono większego powiązania między każdym wskaźnikiem ze sobą przy FCC i VCC, co potwierdza istotne różnice pomiarów między aparatami (ryc. 4).
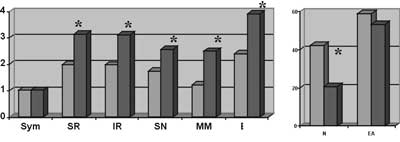
Ryc. 4. Wartości średnie analizowanych wskaźników określonych za pomocą dwóch skaningowych polarymetrów laserowych (w obu badanych grupach).
Po przyjęciu ustalonych wartości norm dla analizowanych wskaźników, określono częstości występowania wartości granicznych oraz wartości poza normą.
Wyniki takie łącznie dla zbioru ośmiu zmiennych wykazywano w 77,1% oczu, badanych aparatem FCC i 30,0% gałek ocenianych aparatem VCC. Różnica w występowaniu zmian jest wysoce znamienna statystycznie (p<0,001). Wartości wyłącznie na pograniczu normy notowano w co czwartej gałce ocznej w przypadku zastosowania aparatu FCC i u 13,6% oczu, gdy pomiar wykonywano aparatem VCC (p<0,05). Wyniki mieszane, tj. graniczne lub poza normą, stwierdzono w 45,0% oczu przy FCC i w 9,3% gałek przy VCC (p<0,001). Odsetki oczu z wartościami wyłącznie poza normą są dla obu aparatów zbliżone i stanowią odpowiednio: 7,8 i 7,1%, (ryc. 5).

Ryc. 5. Struktura występujących zmian w zakresie 8 wskaźników polarymetrii.
Poza oceną jakościową, dotyczącą koincydencji nieprawidłowych wyników, stwierdzanych przez cechy skaningowej polarymetrii, dokonano analizy ilościowej, mającej na celu ustalenie, w jakim stopniu rozważane wskaźniki są ze sobą skorelowane. Macierze korelacji przy obu polarymetrach przedstawia tabela 1, w której szczególną uwagę zwrócono na zależności wysokie. W tabeli tej podano również współczynniki wzajemnej korelacji każdego wskaźnika ze sobą przy dwóch różnych aparatach.
Tabela 1. Macierze korelacji między wskaźnikami grubości włókien nerwowych siatkówki określonych dwoma polarymetrami FCC i VCC.
| SR | 0,275** | | | | | FCC | |
| IR | -0,273** | 0,837** | | | | | |
| SN | 0,060 | 0,440** | 0,378** | | | | |
| MM | -0,214** | 0,694** | 0,805** | 0,592** | | | |
| EM | 0,026 | 0,431** | 0,413** | 0,371** | 0,608** | | |
| N | 0,019 | -0,647** | -0,644** | -0,509** | -0,558** | -0,427** | |
| EA | -0,079 | -0,053 | -0,023 | -0,016 | -0,122 | -0,061 | -0,475** |
| Cechy | Sym | SR | IR | SN | MM | EM | N |
* p <0,05 wg testu jednostronnego
** p <0,01
Legenda:
| mmm | korelacja prawie pełna rxy ≤ 0,9 |
| mmm | korelacja bardzo wysoka 0,7 ≤ rxy < 0,9 |
| mmm | korelacja wysoka 0,5 &le rxy < 0,7 |
5.2. Wartość diagnostyczna wskaźników polarymetrii laserowej u pacjentów z wczesną jaskrą pierwotną otwartego kąta i nadciśnieniem ocznym – zbadanie ich korelacji z klinicznym obrazem pacjentów, wyrażonym cechami ich pola widzenia w badaniu progowym komputerowej perymetrii statycznej i cechami morfologicznymi głowy nerwu wzrokowego, określonymi w skaningowej oftalmoskopii laserowej.
Korelacja większości wskaźników polarymetrii ze zmienną MD, wyrażającą średni ubytek pola widzenia, przy obu aparatach jest istotna i ujemna. Wyjątek stanowi wskaźnik N/NFI, dodatnio i wysoko powiązany z MD, zwłaszcza przy pomiarze tego wskaźnika aparatem VCC. Nie wykazano istotnej zależności współczynników polarymetrii ze wskaźnikiem LV, obrazującym głębokość ubytku zlokalizowanego pola widzenia (korelacja słaba), z wyjątkiem pary NFI i LV, dla których odnotowano korelację przeciętną przy pomiarze aparatem VCC (tab. 2). Nie udało się wykazać korelacji wskaźników polarymetrii laserowej FCC z cechami morfologicznymi głowy nerwu II w skaningowej oftalmoskopii laserowej. Współczynniki korelacji Pearsona przyjmują wartości świadczące o braku wyraźnego skorelowania między analizowanymi podzbiorami zmiennych. Jedynie para zmiennych EA i MR ze współczynnikiem rxy = 0,314 nieznacznie przekroczyła granicę korelacji słabej. Przy pomiarach warstwy włókien nerwowych aparatem VCC odnotowano 4 korelacje o przeciętnym stopniu powiązania.
Tabela 2. Mierniki zależności między wskaźnikami polarymetrii laserowej a cechami pola widzenia.
a) wyznaczone w oparciu o średnie wartości poszczególnych wskaźników przy 6 różnych przedziałach zmiennej MD,
b) wartości współczynników po wyłączeniu z obliczeń 9 bardzo wysokich pomiarów LV.
Korelacje rang bardzo wysokie oznaczono kolorem szarym.
| Wskaźniki | MD | LV |
| FCC | VCC | FCC | VCC |
| Współczynniki korelacji rang a) | Współczynniki korelacji Pearsona b) |
| Sym | -0,029 | 0,314 | 0,035 | 0,041 |
| SR | -0,943** | -0,886* | -0,093 | -0,171* |
| IR | -0,943** | -0,714 | -0,129 | -0,185* |
| SN | -0,257 | -0,486 | -0,043 | -0,102 |
| MM | -0,371 | -0,714 | -0,122 | -0,186* |
| EM | -0,600 | -0,943** | -0,035 | -0,216** |
| N | 0,657 | 1,000** | 0,114 | 0,288** |
| EA | -0,043 | -0,886* | -0,060 | -0,226* |
* p <0,05 wg testu jednostronnego, przy czym istotność współczynnika korelacji rang odnosi się do
** p <0,01 6 wartości średnich, a istotność współczynnika Pearsona do 131 oczu.
Korelację wskaźników polarymetrii laserowej z cechami głowy nerwu II w skaningowej oftalmoskopii laserowej HRT ilustruje tabela 3.
Tabela 3. Współczynniki korelacji między wskaźnikami polarymetrii laserowej a cechami tarczy nerwu wzrokowego w badaniu HRT.
Wskaźniki | RA | RV | MR | RC | C/D |
| A. Przy polarymetrze FCC |
| Sym | -0,161* | -0,273** | -0,278** | -0,220** | 0,231** |
| SR | 0,160* | 0,063 | 0,029 | 0,121 | 0,058 |
| IR | 0,228** | 0,187* | 0,161* | 0,215** | -0,066 |
| SN | 0,071 | 0,027 | -0,006 | 0,007 | -0,063 |
| MM | 0,282** | 0,217** | 0,125 | 0,173 | -0,154* |
| EM | 0,143* | 0,022 | -0,031 | 0,011 | -0,062 |
| N | -0,127 | -0,136 | 0,152* | -0,090 | 0,246** |
| EA | 0,144* | 0,264** | 0,314* | 0,212* | -0,298** |
| B. Przy polarymetrze VCC |
| Sym | 0,003 | -0,001 | 0,015 | 0,054 | 0,080 |
| SR | 0,039 | 0,046 | 0,203* | 0,208* | 0,051 |
| IR | 0,030 | 0,037 | 0,194* | 0,184* | 0,032 |
| SN | 0,177 | 0,283** | 0,403** | 0,467** | 0,013 |
| MM | 0,078 | 0,140* | 0,312** | 0,299** | -0,018 |
| EM | 0,090 | 0,124 | 0,266** | 0,230** | -0,088 |
| N | -0,374** | -0,229** | -0,178 | -0,209** | 0,213** |
| EA | 0,379** | 0,244** | 0,085 | 0,109 | -0,305** |
* p <0,05
** p <0,01 wg testu jednostronnego. Najwyższe korelacje oznaczono kolorem szarym.
Dokonana analiza korelacji wskaźników skaningowej polarymetrii laserowej z cechami pola widzenia i cechami głowy nerwu wzrokowego upoważnia do poniższych wniosków:
1) Większość wskaźników polarymetrycznych, obrazujących w.w.n., przy ich pomiarach dwoma aparatami jest ujemnie powiązana z MD, wykazując malejący trend średnich wartości wraz ze zmianą MD od najwyższych wartości ujemnych do najwyższych dodatnich. Z kolei dodatnio i wysoko skorelowany z MD jest wskaźnik N, zwłaszcza przy jego pomiarze aparatem VCC. Związki wskaźników skaningowej polarymetrii laserowej z drugą zmienną pola widzenia – LV – są słabe, czego wyrazem są niskie współczynniki korelacji Pearsona (rxy <0,300).
2) Powiązanie wskaźników polarymetrycznych z cechami morfologicznymi głowy nerwu wzrokowego jest zróżnicowane względem stosowanych aparatów FCC i VCC. Przy polarymetrze FCC nie stwierdzono, by wskaźniki były powiązane z cechami HRT, natomiast przy pomiarach aparatem VCC, odnotowano skorelowanie przeciętnego stopnia między czterema parami zmiennych, tj. SN z MR i z RC oraz N i EA z RA, w tym kierunek zależności N i RA jest ujemny.
5.3. Ocena trafności wskaźników dwóch typów skaningowej polarymetrii laserowej w wykrywaniu zmian charakterystycznych dla wczesnej jaskry.
Rozważane w pracy grupy diagnostyczne zostały wyłonione w oparciu o kryteria kliniczne. W przebadanej grupie pacjentów z NO wyróżnia się brak zmian w polu widzenia, prawidłowa ogólna klasyfikacja parametrów głowy nerwu II (dopuszczalne odchylenia od normy pojedynczych parametrów) oraz nieobecność w grupie cienkich rogówek. Powyższe właściwości sprawiają, że podjęta w tym miejscu ocena trafności w wykrywaniu zmian dotyczy wyłącznie grupy z JPOK. Wśród mierników trafności uwzględniono: czułość, swoistość, wyniki fałszywie dodatnie i ujemne oraz zgodność całkowitą z wyodrębnieniem wartości nieprawidłowych.
Dla weryfikacji trafności wskaźników układem odniesienia były wyniki komputerowego badania pola widzenia oraz klasyfikacja kliniczna obrazu morfologicznego głowy nerwu wzrokowego, będąca zbiorczą oceną statystyczną cech HRT.
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
29 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
69 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
129 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 78 zł
Piśmiennictwo
1. European Glaucoma Socjety. Terminology and Guidelines for Glaucoma. IInd Edition. DOGMA Srl; Savona 2003, Ch.1: 27-29, Ch. 2: 5.
2. Jonas J.B.: Morphological aspects in the diagnosis and pathogenesis of glaucomatous optic neuropaty. Glaucoma: decision making in therapy. Sprinter-Verlag, Milano 1996: 51-63.
3. Czajkowski J., Matusiak D., Grabowski R.: Jaskra - narastający problem społeczny XXI wieku: materiały szkoleniowe Łódzkich Warsztatów Jaskrowych. Okulistyka - wyd. spec. 2004, 4: 3-4.
4. Czechowicz-Janicka K.: Jaskra - choroba nieznana. Klinika Oczna 2003; 105 (1-2): 76-78.
5. Czechowicz-Janicka K.: Jaskra pierwotna z szerokim kątem przesączania. Wydanie I. Mako, Warszawa 1996.
6. Niżankowska M.H., Krzyżanowska P.: Współczesne poglądy na istotę i patomechanizm jaskry pierwotnej oraz ich wpływ na zasady i strategię leczenia. Terapia 2000; 4: 4-7.
7. Leske M.C., et al.: Factors for glaucoma progression and effect of treatment: the early manifest glaucoma trial. Arch. Ophtalmol., 2003; 121: 48-56.
8. Heil A, et al.: Early Manifest Glaucoma Trial Group. Reducion of intraocular pressure and glaucoma progression: results from the EMGT. Arch. Ophthalmol., 2002; 120: 1268-1279.
9. AGIS Investigators. The Advanced Glaucoma Intervention Study: Baseline risk factors for sustained loss of visual field and visual acuity in patients with advanced glaucoma. Am. J. Ophthalmol., 2002; 134; 499-512.
10. AGIS Investigators. The Advanced Glaucoma Intervention Study: The relationship between control of the intraocular pressure and visual field deterioration. Am. J. Ophthalmol., 2000; 130: 329-440.
11. Flammer J: The vascular concept of glaucoma. Surv. Ophthalmol., 1994 Suppl; 38: 3-6.
12. Flammer J: To what extent are vascular factors involved in the pathogenesis of normal-tension glaucoma? Ocular Blood-Flow, Karger, Basel 1996: 12-39.
13. Czajkowski J., et al.: Rola naczyniowych czynników ryzyka i ich występowanie w polskiej populacji chorych na jaskrę : wyniki 14208 badań ankietowych. Okulistyka - wyd. spec 2003, 1-8.
14. Czechowicz-Janicka K.: Jaskra normalnego ciśnienia - czy już odrębna jednostka chorobowa? Okulistyka-numer specjalny 1999; 2: 6-8.
15. Czajkowski J., et al.: Jaskra z niskim ciśnieniem śródgałkowym. Zmiany biochemiczne w krwi obwodowej. Klin. Oczna 1988, 90: 341-343.
16. Czajkowski J., Krawczykowa Z.: Rola naczyniówki otaczającej głowę nerwu wzrokowego w etiopatogenezie jaskry z niskim ciśnieniem śródgałkowym. Klin Oczna 1985; 87: 193-195
17. Terelak-Borys B.: Badanie udziału mechanizmów naczynioskurczowych w patogenezie neuropatii jaskrowej. Praca doktorska. Klinika Okulistyki Centrum Medycznego Kształcenia Podyplomowego w Warszawie, 2001.
18. Niżankowska M.H.: Rola warunków hemodynamicznych w obrębie tylnego odcinka oka w powstawaniu i rozwoju neuropatii jaskrowej. Klin. Oczna 1996; 3: 241-247.
19. Kass M.A., et al.: The ocular hypertension tratment study: a randomized trial determines that topical ocular hypotensive medication delays or prevents the onset of primary open angle glaucoma. Arch. Ophthalmol., 2002; 12(6): 701-713.
20. Lemij H.G.: The value of polarimetry in the evaluation of the optic nerve disc in glaucoma. Curr. Opin. Ophthalmol., 2001; 12(2): 138-142.
21. Brandt J.D., et al.: Central corneal thickness in the Ocular Hypertension Treatment Study (OHTS). Ophthalmology 2001; 108: 1779-1788.
22. Copt R.P., et al.: Corneal thickness in ocular hypertension, primary open-angle glaucoma, and normal tension glaucoma. Arch. Ophthalmol., 1999; 117: 14-16.
23. Ehlers N., et al.: Central corneal thickness in low tension glaucoma. Acta. Ophthalmol., 1975; 53: 34-43.
24. Ehlers N., et al.: Applanation tonometry and central corneal thickness. Acta. Ophthalmol., 1974; 52: 740-746.
25. Whitacre M.M., Stein R.: Sources of error with use of Goldmann-type tonometers. Surv. Ophtalmol., 1993; 38: 1-30.
26. Whitacre M.M., Stein R. Hassanein.: The effect of corneal thickness on applanation tonometry. Am. J. Ophthalmol., 1993; 115: 592-596.
27. Wolfs R.C.W., et al.: Distribution of central corneal thickness and its association with intraocular pressure: Rotterdam Study. Am. J. Ophthalmol., 1997; 123: 767-772.
28. Argus W.A.: Ocular hypertension and central corneal thickness. Ophthalmology 1995; 102(12): 1810-1812.
29. Eysteinsson T., et al.: Reykjavik Eye Study Group. Central corneal thickness, radius of the corneal curvature and intraocular pressure in normal subjects using non-contact techniques: Reykjavik Eye Study. Acta. Ophth. Scand., 2002; 80(1): 11.
30. Langwińska-Wośko E., et al.: Zależność pomiędzy centralną grubością rogówki a ciśnieniem śródgałkowym. Okulistyka - numer specjalny 2000; 4: 3-5.
31. Gordon M.O., et al.: The ocular hypertension tratment study: baseline factors that predict the onset of primary open angle glaucoma. Arch. Ophtalmol., 2002; 120(6): 714-720.
32. Landers J., et al.: Analysis of risk factors that may be associated with progression from ocular hypertension to primary open angle glaucoma. Clin. Experiment. Ophthalmol., 2002; 30(4): 242-247.
33. Kerrigan-Baumrind L.A., et al.: Number of ganglion cells in glaucoma eyes compared with threshold visual fields in the same person. Invest. Ophthalmol. Vis. Sci., 2000; 41(3): 741-748.
34. Airaksinen P.J., et al.: Rate and pattern of neuroretinal rim area decrease in ocular hypertension and glaucoma. Arch. Ophthalmol., 1992; 110: 206-210.
35. Czechowicz-Janicka K: Monitorowanie jaskry. Okulistyka polska początku XXI wieku. Kęcik T (red), Oftal Sp. z o.o., Warszawa 2002: 51-56.
36. Janz N.K., et al.: The Collaborative Initial Glaucoma Treatment Study: interim quality of life findings after initial medical or surgical treatment of glaucoma. Ophthalmology 2001; 108: 1954-1965.
37. Quigley H.A. Addicks E.M.: Quantitative studies of retinal nerve fiber layer defects. Arch. Ophthalmol. 1982; 100: 807-814.
38. Quigley H.A., et al.: Optic nerve damage in human glaucoma: III. Quantitative correlation of nerve fiber loss and visual field defect in glaucoma, ischemic optic neuropathy, papilledema, and toxic neuropathy. Arch. Ophthalmol., 1982; 100: 135-146.
39. Yucel Y.H., et al.: Effects of retinal ganglion cell loss on magno-, parvo-, konio-cellular pathways in the lateral geniculate nucleus and visual cortex in glaucoma. Prog. Retin. Eye Res., 2003; 22; 465-481.
40. Hodapp E., et al.: Clinical decision in glaucoma. St. Louis CV Mosby Comp 1993; 52-61.
41. Aasman P., Heil A.: Evaluation of methods for automated hemifield analysis in perimetry. Arch. Ophthalmol., 1992; 110: 812-819.
42. Spaeth G.L.: Stadia jaskry. Klin Oczna 1998; 5: 341-342.
43. Mikelberg F.S., et al.: Ability of the Heidelberg Retina Tomograph to detect early glaucomatous visual field loss. J. Glaucoma 1995; 4: 242-247.
44. Wollstein G., et al.: Identification of early glaucoma cases with the scanning laser ophthalmoscope. Ophthalmology 1998; 105: 1557-1563.
45. Wasyluk J.T., et al.: Ocena wpływu centralnej grubości rogówki na wzajemną zgodność parametrów warstwy włókien nerwowych siatkówki, badanych za pomocą różnych skaningowych polarymetrów laserowych u pacjentów z wczesną jaskrą i nadciśnieniem ocznym. Okulistyka 2005; 1(I): 12-15.
46. Wasyluk J.T., et al.: Porównanie wyników pomiarów grubości warstwy włókien nerwowych siatkówki wykonanych za pomocą skaningowych polarymetrów laserowych GDx FCC oraz GDx VCC - doniesienie wstępne. Okulistyka - suplement 2003; 1: 89-94.
47. Greenfield D.S., et al.: Effect of corneal polarization axis on assessment of retinal nerve fiber layer thickness by scanning laser polarimetry. Am J Ophthalmol 2000; 129: 715-722
48. Zhou Q., Weinreb R.N.: Individualized compensation of anterior segment birefringence during scanning laser polarimetry. Invest. Ophthalmol. Vis. Sci., 2002; 43(7): 2221-8.
49. Knighton R.W., et al.: Analytical model of scanning laser polarimetry for retinal nerve fiber layer assessment. Invest. Ophthalmol. Vis. Sci., 2002; 43(2): 383-92.
50. Greenfield D.S., et al.: Correction of corneal polarization axis improves the discriminating power of scanning laser polarimetry. Am. J. Ophthalmol., 2002; 134(1): 27-33.
51. Jonas J.B., Schiro D.: Localised wedge shaped defects of the retinal nerve fibre layer in glaucoma. Br. J. Ophthalmol., 1994; 78: 285-290.
52. Vermeer K.A., et al.: Detecting glaucomatous wedge shaped defects in polarimetric images. Med. Im. Anal., 2003; 7: 503-511.
53. Hoh S.T., et al.: Peripapillary nerve fiber layer thickness measurement reproductibility using scanning laser polarimetry. J. Glaucoma 1998; 7(1): 12-15.
54. Holló G., et al.: Influence of post-LASIK corneal healing on scanning laser polarimetric measurement of the retinal nerve fibre layer thickness. Br. J. Ophthalmol., 2002; 86: 627-631.
55. Angeles R., et al.: Corneal changes after laser in situ keratomileusis: measurement of corneal polarization magnitude and axis. Am. J. Ophthalmol., 2004; 137(4): 697-703.
56. Hoffmann E.M., et al.: Scanning laser polarimetry and retinal thickness analysis before and after laser in situ keratomileusis. Eur. J. Ophthalmol., 2005; 15(4): 434-40.
57. Krajewska M., et al.: Wartość diagnostyczna komputerowej perymetrii statycznej, laserowej tomografii siatkówkowej (HRT) oraz skaningowej polarymetrii laserowej (GDx) w ocenie progresji jaskry pierwotnej otwartego kąta. Okulistyka-supl. 2003; 1: 85-87.
58. Schlottmann P.G., et al.: Relationship between visual field sensitivity and retinal nerve fiber layer thickness as measured by scanning laser polarimetry. Invest. Ophthalmol. Vis. Sci., 2004; 45(6): 1823-9.
59. Reus N.J, Lemij H.G.: The relationship between standard automated perimetry and GDx VCC measurements. Invest. Ophthalmol. Vis. Sci., 2004 ; 45(3): 840-5.
60. Bagga H., et al.: Scanning laser polarimetry with variable corneal compensation and optical coherence tomography in normal and glaucomatous eyes. Am. J. Ophthalmol., 2003; 135(4): 521-529.
61. Bowd C., et al.: Association Between Scanning Laser Polarimetry Measurements Using Variable Corneal Polarization Compensation and Visual Field Sensitivity in Glaucomatous Eyes. Arch. Ophthalmol., 2003; 121(7): 961-966.
62. Kogure S., et al.: A new parameter for assessing the thickness of the retinal nerve fiber layer for glaucoma diagnosis. Eur. J. Ophthalmol., 1999; 9(2): 93-8.
63. Krajewska M., et al.: Ocena zależności pomiędzy wskaźnikami pola widzenia a grubością warstwy włókien nerwowych siatkówki u chorych na jaskrę pierwotną otwartego kąta. Okulistyka 2001; 12: 3-4.
64. Weinreb R.N., et al.: Association between quantitative nerve fiber layer measurement and visual field loss in glaucoma. Am. J. Ophthalmol., 1995; 120(6): 732-8.
65. Kwon Y.H., et al.: Correlation of automated visual field parameters and peripapillary nerve fiber layer thickness as measured by scanning laser polarimetry. J. Glaucoma 2000; 9(4): 281-8.
66. Marraffa M., et al.: Does nerve fiber layer thickness correlate with visual field defects in glaucoma? A study with the nerve fiber analyzer. Ophthalmologica 1997; 211(6): 338-40.
67. Mohammadi K., et al.: Retinal nerve fiber layer thickness measurements with scanning laser polarimetry predict glaucomatous visual field loss. Am. J. Ophthalmol., 2004; 138(4): 592-601.
68. Sihota R., et al.: Correlation between confocal scanning laser ophthalmoscopy and scanning laser polarimetry in open angle glaucoma. Eur. J. Ophthalmol., 2003; 13(3): 266-75.
69. Eid T.M., et al.: Quantitative estimation of retinal nerve fiber layer height in glaucoma and the relationship with optic nerve head topography and visual field. J. Glaucoma 1997; 6(4): 221-30.
70. Tjon-Fo-Sang M.J., Lemij H.G.: The sensitivity and specificity of nerve fiber layer measurements in glaucoma as determined with scanning laser polarimetry. Am. J. Ophthalmol., 1997; 123(1): 62-9.
71. Choplin N.T., Lundy D.C.: The sensitivity and specificity of scanning laser polarimetry in the detection of glaucoma in a clinical setting. Ophthalmology 2001; 108(5): 899-904.
72. Munkwitz S., et al.: Sensitivity and specificity of scanning laser polarimetry using the GDx. Br. J. Ophthalmol., 2004; 88: 1142-1145.
73. Sinai M.J., et al.: Diffuse and localized nerve fiber layer loss measured with a scanning laser polarimeter: sensitivity and specificity of detecting glaucoma. J. Glaucoma 2000; 9(2): 154-62.
74. Lauande-Pimentel R., et al.: Discrimination between normal and glaucomatous eyes with visual field and scanning laser polarimetry measurements. Br. J. Ophthalmol., 2001; 85: 586-591.
75. Weinreb R.N., et al.: Glaucoma Detection Using Scanning Laser Polarimetry with variable corneal polarization compensation. Arch. Ophthalmol., 2003; 121(2): 218-224.
76. Tannenbaum D.P., et al.: Variable corneal compensation improves discrimination between normal and glaucomatous eyes with the scanning laser polarimeter. Ophthalmology 2004; 111(2): 259-64.
77. Brusini P., et al.: Discrimination between normal and early glaucomatous eyes with scanning laser polarimeter with fixed and variable corneal compensator settings. Eur. J. Ophthalmol., 2005; 15(4): 468-76.
78. Horn F.K., et al.: Polarimetric measurement of retinal nerve fiber layer thickness in glaucoma diagnosis. J. Glaucoma 1999; 8(6): 353-62.
79. Xu L., et al.: Quantitative nerve fiber layer measurement using scanning laser polarimetry and modulation parameters in the detection of glaucoma. J. Glaucoma 1998; 7(4): 270-7.
80. Kamal D.S., et al.: Use of the GDx to detect differences in retinal nerve fibre layer thickness between normal, ocular hypertensive and early glaucomatous eyes. Eye 2000; 14: 367-70.
81. Reus N.J., Lemij H.G.: Scanning laser polarimetry of the retinal nerve fiber layer in perimetrically unaffected eyes of glaucoma patients. Ophthalmology 2004; 111(12): 2199-203.
82. Weinreb R.N., et al.: Risk assessment in the management of patients with ocular hypertension. Am. J. Ophthalmol 2004; 138: 458-467.
83. Tjon-Fo-Sang M.J., et al.: Measurement by nerve fiber analyzer of retinal nerve fiber layer thickness in normal subjects and patients with ocular hypertension. Am. J. Ophthalmol., 1996; 122(2): 220-7.





