© Borgis - Postępy Nauk Medycznych 3-4/2003, s. 106-112
Lech Konopka
Leczenie krwią i preparatami krwiopochodnymi u chorych na nowotwory
Transfusion therapy in cancer patients
Klinika Chorób Wewnętrznych i Hematologii Instytut Hematologii i Transfuzjologii w Warszawie
Kierownik Kliniki: prof. dr hab. med. Lech Konopka
Streszczenie
Zwalczanie niedokrwistości w chorobach nowotworach jest częścią leczenia wspomagającego, warunkującego odpowiednią jakość życia chorym (QOL).
Występowanie niedokrwistości w nowotworach łączy się z ostrą lub przewlekłą utratą krwi, zaburzeniami wytwarzania krwinek czerwonych, bądź hemolizą erytrocytów. Typowa dla chorób nowotworowych jest niedokrwistość uwarunkowana upośledzonym wytwarzaniem krwinek czerwonych, często z równoczesną ich wewnątrzszpikową hemolizą. Nasilenie niedokrwistości i jej wpływ na ustrój człowieka zależą głównie od czasu i stopnia ubytku krwi krążącej oraz zmniejszania się stężenia hemoglobiny i liczby krwinek czerwonych. Niedokrwistość jest szczególnie źle znoszona przez ludzi w starszym wieku ze współistniejącymi chorobami układu krążenia i ośrodkowego układu nerwowego (oun). Dodatkowo niedokrwistość u chorych na nowotwory może ulegać pogłębieniu wskutek leczenia cytostatykami lub/i radioterapią.
Za najważniejsze wskazania do przetoczenia krwi uważa się obecność klinicznych objawów niedokrwistości (trachycardia, bóle wieńcowe), pojawienie się lub nasilenie niewydolności krążenia lub krążenia mózgowego.
Współczesne zasady krwiolecznictwa obejmują stosowanie elementów morfotycznych krwi lub składników osocza. Osocze i preparaty osoczopochodne mają zastosowanie w leczeniu osoczowych skaz krwotocznych.
W arsenale koncentratów krwinek czerwonych znajduje się obecnie znaczna liczba różnorodnych preparatów, pozwalająca na zaspokojenie potrzeb u chorych na nowotwory z różnymi postaciami niedokrwistości.
Z przetaczaniem krwi i jej produktów, o czym należy zawsze pamiętać, wiąże się niebezpieczeństwo przeniesienia zakażeń bakteryjnych i wirusowych, wystąpienie immunizacji, gorączkowych odczynów poprzetoczeniowych lub hemolitycznych.
Wprowadzenie w ostatnich latach nowych technologii i wytwarzanie rekombinowanych czynników krzepnięcia, albuminy, a także czynników wzrostu (G-CSF, GM-CSF) oraz erytropetyny wybitnie zmniejszyło niebezpieczeństwo związane z przetaczaniem preparatów krwiopochodnych. Spełniają one oczekiwania chorych i wzbudzają u nich nadzieję na przedłużenie życia w warunkach „względnego komfortu”.
Summary
Anaemia is a common complication in cancer patients. The decrease in haemoglobin level may lead to several symptoms such as fatigue, exhaustion, and impaired quality of life (QOL), and it may worsen prognosis.
Anemia in cancer and in haematologic malignancies may caused mainly by an impairment of haematopoiesis due to bone marrow infiltraion by malignant cells. It is also caused by acute or chronic blood loss hemolysis, nutritional deficiences and most notably by chemotcherapy – induced bone marrow suppression.
Even the introduction of recombinant human erythropoietin and other blood components (Factor VIII, Albumin) and growth factors (G-CSF, GM-CSF) red blood cell (RBC) transfusions are still the traditional treatment for improvement of Hb levels. The major benefit of RBC transfusions is their immediate effect. Transfusions, however, are associated with several adverse events and risks, have only transient effects, and have a limited capacity to ameliorate the symptoms of anaemia.
Thus, the current paradigm of the anaemia treating in cancer patients must equilibre between of the conservative treatment with RBC and the recent possibilities of treatment with erythropoietin.

Zwalczanie niedokrwistości w chorobach nowotworowych jest częścią złożonego leczenia wspomagającego, warunkującego odpowiednią jakość życia chorym (quality-of-life) (tab. 1). Obecna i utrzymująca się u chorych na nowotwory niedokrwistość upośledza dotkliwie nie tylko wydolność fizyczną chorego lecz osłabia w nim wiarę w możliwość wyleczenia oraz powrotu do czynnego życia oraz pracy zawodowej (2, 5).
Tabela 1. Postępowanie zapewniające odpowiednią jakość życia u chorych na nowotwory.
Zwalczanie choroby nowotworowej i objawów ubocznych leczenia.
Zapewnienie sprawności fizycznej.
Dbałość o stan psychiczny.
Zaspokojenie potrzeb materialnych.
Współdziałanie środowiska, rodziny i otoczenia.
|
Prawidłowy stan układu krwiotwórczego lub jego poprawne wyrównanie stanowi poza tym niezbędny warunek przeprowadzenia skutecznego leczenia przeciwnowotworowego w odpowiednich dawkach i w zaplanowanym czasie (6).
Występowanie niedokrwistości w chorobach nowotworowych łączy się z ostrą lub przewlekłą utratą krwi, zaburzeniami wytwarzania krwinek czerwonych, bądź hemolizą erytrocytów (tab. 2).
Tabela 2. Patogeneza niedokrwistości w chorobach nowotworowych.
Utrata krwi:
? ostra,
? przewlekła.
Upośledzone wytwarzanie erytrocytów:
? hypo- lub aplazja szpiku,
? niedobór żelaza,
? niedokrwistości megaloblastyczne, syderoblastyczne,
? niedokrwistości towarzyszące przewlekłym chorobom (ACD).
Hemoliza erytrocytów:
? niedokrwistości hemolityczne na podłożu immunologicznym
? hypersplenizm.
|
Te 3 główne mechanizmy patogenetyczne obejmują szeroką gamę różnorodnych czynników warunkujących powstanie i rozwój niedokrwistości u chorych na nowotwory. Pomijając oczywiste przypadki niedokrwistości pokrwotocznych (ostra lub przewlekła utrata krwi) mechanizm większości postaci niedokrwistości występujących u chorych na nowotwory łączy się z zaburzeniami szpikowego wytwarzania krwinek czerwonych.
Naciekanie szpiku przez komórki nowotworowe, uszkodzenie komórki macierzystej lub nieprawidłowości w wytwarzaniu i/lub działaniu czynników odpowiedzialnych za ich dojrzewanie i różnicowanie stanowią główne przyczyny upośledzonego wytwarzania krwinek czerwonych (8, 9, 10).
Toksyczne działanie cytostatyków i wpływ promieniowania rentgenowskiego, jako uboczne skutki leczenia energią promienistą, są główną przyczyną hypoplazji utkania krwiotwórczego i powstania pancytopenii.
Do samoistnej aplazji szpiku niezwykle rzadkiej w chorobach nowotworowych (np. w przebiegu grasiczaka) dołączyła ostatnio aplazja szpiku wywołana przez antyerytropoetynowe przeciwciała powstające u chorych leczonych przewlekle preparatami rekombinowanej erytropoetyny (3, 4).
Duże znaczenie w powstawaniu niedokrwistości w chorobach nowotworowych przypisuje się niedoborom czynników krwiotwórczych (m.in. żelaza, witaminy B12, kwasu foliowego lub pirydoksyny – witaminy B6). Niedostateczna podaż tych witamin w diecie, bądź utrata łaknienia, wymioty, biegunki prowadzą do typowych objawów niedokrwistości syderopenicznej, megaloblastycznej lub rzadziej syderoblastycznej.
Na osobne omówienie zasługuje dość typowa dla chorób nowotworowych anemia określana mianem niedokrwistości w przebiegu schorzeń przewlekłych (anaemia chronic disease- ACD-angl.).
Niedokrwistość ta jest pierwotnie wynikiem obniżonego wytwarzania krwinek czerwonych i skróconego czasu ich przeżycia (często hemoliza wewnątrzszpikowa).
Tej normocytowej i normochromicznej postaci niedokrwistości towarzyszą dość charakterystyczne zaburzenia metabolizmu żelaza (tab. 3): obniżone stężenie żelaza w osoczu, jak i zmniejszone stężenie transferryny, natomiast zawartość ferrytyny jest prawidłowa lub zwiększona, a szpik cechują złogi żelaza w erytroblastach i żelaza pozakomórkowego.
Tabela 3. Różnicowanie niedokrwistości syderopenicznej z anemią w przebiegu chorób przewlekłych (ACD).
| Zachowanie się żelaza i białek wiążących żelazo
w surowicy | Niedokrwistości |
| Syderopeniczna | ACD |
| Poziom żelaza | niski | niski |
| Utajona zdolność wiązania żelaza (UZWŻ) | wysoka | niska lub prawidłowa |
| Stężenie transferryny | podwyższone lub prawidłowe | obniżone lub prawidłowe |
| Stężenie ferrytyny | obniżone | prawidłowe lub podwyższone |
| Zapasy żelaza w szpiku | brak | prawidłowe lub zwiększone |
Przyczyny niedokrwistości związanej z przewlekłymi chorobami (w tym nowotworowymi) są wciąż dyskusyjne. Pod uwagę brane są: zaburzone uwalnianie żelaza z makrofagów, niskie stężenie erytropoetyny, supresja erytropoetyny przez hamujące cytokiny (TNF, IL -1) wytwarzane przez pobudzone makrofagi oraz interferon – g, a także „wykradanie” żelaza z transferryny przez pochodzącą z makrofagów laktoferrynę. Nie bez znaczenia na podsycanie tej postaci niedokrwistości mają towarzyszące chorobom nowotworowym zakażenia (8, 9).
Ustalenie przyczyny i charakteru niedokrwistości ma w każdym przypadku, nie tylko w chorobach nowotworowych podstawowe znaczenie dla taktyki jej leczenia. Zahamowanie lub wyeliminowanie na stałe źródeł krwawienia, wyrównanie niedoborów i stała suplementacja substancji krwiotwórczych, opanowanie zakażeń lub skuteczna kortykoterapia bądź splenektomia w zespołach hemolitycznych i hyperplemizmie prowadzi nie tylko do wyrównania niedokrwistości lecz ogranicza znacznie wskazania do przetaczania krwi i jej pochodnych. Dokładna znajomość przyczyny powstawania niedokrwistości u chorych na nowotwory pozwala dodatkowo na jej profilaktykę i zapobiega następstwom wynikającym z wieloukładowej pancytopenii.
Nasilenie niedokrwistości i jej wpływ na ustrój człowieka zależą głównie od czasu i stopnia ubytku objętości krwi krążącej oraz zmniejszania się stężenia hemoglobiny i liczby krwinek czerwonych (tab. 4).
Tabela 4. Objawy kliniczne niedokrwistości w zależności od zmniejszenia objętości krwi krążącej.
| Zmniejszenie objętości krwi krążącej (OKK) | Objawy kliniczne |
| Mniej niż 1000 ml (< 20% OKK) | Bez objawów klinicznych |
| Więcej niż 1000 ml (> 20% OKK) | Hipotonia ortostatyczna |
| Więcej niż 1500 ml (> 30% OKK) | Zmniejszenie ciśnienia krwi w pozycji leżącej, niepokój, bezsenność |
| Więcej niż 2000 ml (> 40% OKK) | Wstrząs hypowolemiczny, duszność, poty, dezorientacja |
W przewlekłych niedokrwistościach, które z reguły występują w chorobach nowotworowych, do anemii dochodzi znacznie wolniej niż w stanach nagłej utraty krwi, więc i objawy kliniczne są znacznie słabiej zaznaczone. Należy również pamiętać, że ogólnie uznane objawy podmiotowe towarzyszące przewlekłym niedokrwistościom (m.in. osłabienie, zawroty głowy, zadyszka, duszność wysiłkowa, przyspieszone bicie serca itp.) mogą być u chorych na choroby nowotworowe tłem innej współistniejącej choroby np. upośledzenia czynności płuc, niedokrwienia mięśnia sercowego, zmian miażdżycowych tak krążenia mózgowego jak i innych naczyń obwodowych (1). Ważniejsze są zatem badania kliniczne i wyniki badań laboratoryjnych. Zezwalają one na obiektywną ocenę zmian w objętości krwi krążącej i stopnia niedoboru krwinek czerwonych. Z obniżeniem wskaźnika hematokrytowego krwi i zmniejszeniem stężenia hemoglobiny wiąże się upośledzenie przenoszenia tlenu do tkanek, co przy dalszym pogłębianiu się niedokrwistości prowadzi szybko do załamania się fizjologicznych mechanizmów kompensacyjnych (ryc. 1). Ubytek w objętości krwi krążącej prowadzi do zmniejszenia minutowego rzutu serca, którego nie wyrównuje nawet przyspieszenie czynności serca. Pochodną obniżonego stężenia hemoglobiny we krwi jest zmniejszenie zawartości tlenu we krwi tętniczej, a w następstwie mniejszego rzutu serca dochodzi do upośledzenia (obniżenia) transportu tlenu do tkanek wraz ze zmniejszeniem jego zużycia.
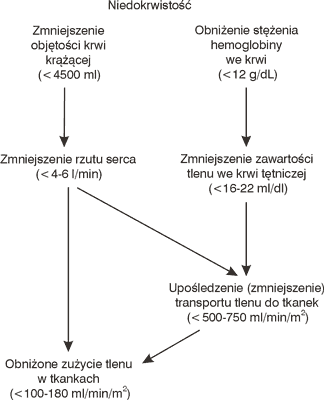
Ryc 1. Wpływ niedokrwistości na transport tlenu w ustroju.
W niedokrwistościach ustrój ludzki jak wspomniano wyżej uruchamia swoiste mechanizmy kompensacyjne (tab. 5). I tak np. reakcją na normowolemiczną niedokrwistość jest zwiększenie rzutu serca przez pobudzenie układu współczulnego, a zmiany w lepkości krwi zwiększają objętość wyrzutową dzięki nasileniu napływu żylnego i zmniejszeniu obciążenia następczego. Wysiłek, zwłaszcza maksymalny, prowadzi do znacznego przyspieszenia częstości uderzeń serca, jednak rzut serca jest mniejszy niż u osób zdrowych. Przyspieszenie akcji serca skraca czas rozkurczu, co ma niekorzystny wpływ na ukrwienie mięśnia sercowego.
Tabela 5. Mechanizmy wyrównawcze (kompensacyjne) w niedokrwistości.
Zwiększenie rzutu serca:
? przyspieszenie częstości uderzeń serca (mechanizm główny),
? zwiększenie objętości wyrzutowej.
Zwiększenie wieńcowego przepływu tętniczego:
? mechanizm ograniczony przy zwężeniu tych tętnic,
Zmiany przepływu przez poszczególne narządy:
? ograniczenie przepływu przez dobrze ukrwione narządy o małym zużyciu tlenu, a zwiększenie przepływu przez narządy o wysokim zapotrzebowaniu na tlen.
Zwiększenie ekstrakcji tlenu:
? wzrost współczynnika ekstrakcji tlenu z 0,25 do 0,75
Zwiększenie ilości 2,3-dwufosfoglicerynianu w erytrocytach:
? przesunięcie krzywej dysocjacji oksyhemoglobiny w prawo zwiększa uwalnianie tlenu w tkankach.
|
Na dystrybucję obniżonej zawartości tlenu krwi tętniczej do ważnych dla życia narządów, mają wpływ zmiany przepływu w krążeniu wieńcowym oraz zmiany w przepływach narządowych. Zwiększenie dowozu tlenu do mięśnia sercowego i do mózgu w niedokrwistościach jest możliwe dzięki zwiększeniu przepływu wieńcowego oraz przepływu w naczyniach mózgowych, kosztem innych narządów. Niestety w wyniku takich zmian w dystrybucji tlenu i ograniczeniu dopływu krwi do innych tkanek może dochodzić szybko do ich niedokrwienia, co np. w przypadku przewodu pokarmowego może prowadzić do zakażeń.
Do ważnych mechanizmów obronnych przed niedokrwistością należy zachowanie się 2,3-dwufosfoglicerynianu w krwinkach czerwonych. Zwiększona produkcja tego związku w erytrocytach u chorych z niedokrwistością wpływa na krzywą dysocjacji oksyhemoglobiny i zwiększa uwalnianie tlenu do tkanek.
Trzeba wyraźnie podkreślić, że mechanizmy adaptacyjne, podobnie jak objawy kliniczne w przewlekłej niedokrwistości normowolemicznej, różnią się znacznie od tychże mechanizmów występujących w stanach ostrych i nagłych anemii.
Uwzględnienie wszystkich okoliczności, w tym zwłaszcza poznanie przyczyny niedokrwistości u chorych na nowotwory, stanowi podstawowy warunek przy ustalaniu wskazań do leczenia krwią i preparatami krwiopochodnymi.
Obecnie przetaczane są przede wszystkim elementy morfotyczne krwi lub składniki osocza. Stosowanie osocza i preparatów osoczopochodnych ma zastosowanie w leczeniu osoczowych skaz krwotocznych.
Z przetaczaniem krwi i jej produktów, o czym trzeba zawsze pamiętać, wiąże się niebezpieczeństwo przeniesienia zakażeń bakteryjnych i wirusowych, występowanie immunizacji, rozwój choroby „przeszczep przeciw gospodarzowi”, występowanie gorączkowych odczynów poprzetoczeniowych lub hemolitycznych oraz hemosyderozy (tab. 6).
Tabela 6. Powikłania po przetoczeniach krwi i preparatów krwiopochodnych.
Niehemolityczne powikłania gorączkowe.
Reakcje alergiczne (pokrzywkowe, anafilaktyczne).
Ostre i opóźnione reakcje hemolityczne.
Bakteryjne zanieczyszczenie składników krwi.
Ostra poprzetoczeniowa niewydolność oddechowa (TRALI).
Plamica poprzetoczeniowa.
Reakcje hipotensyjne.
Hemoliza nieimmunologiczna.
Poprzetoczeniowe przeciążenie krążenia.
Poprzetoczeniowa hipotermia.
Poprzetoczeniowa hiperkaliemia.
|
Wprowadzane w ostatnich latach nowe technologie i wytwarzanie rekombinowanych czynników krzepnięcia i albuminy, a także czynników wzrostu dla linii granulocytowej i płytkowej (G-CSF, GM-CSF) oraz erytropoetyny, wybitnie zmniejszyło niebezpieczeństwo związane z przetaczaniem ludzkich preparatów krwiopochodnych. Szczególne znaczenie ma zwłaszcza wprowadzenie do szerszego użytku klinicznego preparatów rekombinowanej genetycznie erytropoetyny. Zastosowanie jej w niedokrwistościach towarzyszących chorobom nowotworowym eliminuje w wielu przypadkach przetoczenia krwi i poprawia jakość życia tych chorych (7, 9).
Od wielu lat toczą się szerokie dyskusje dotyczące ustalenia „wytycznych”, które stanowiłyby racjonalne uzasadnienie do leczenia krwią różnych postaci niedokrwistości, w tym zwłaszcza anemii w przebiegu chorób nowotworowych.
Mimo licznych kontrowersji za najważniejsze wskazanie do przetoczenia krwi uważa się obecność klinicznych objawów niedokrwistości (tachycardia, bóle wieńcowe, pojawienie się lub nasilenie niewydolności krążenia lub krążenia mózgowego).
Próba ustalenia „krytycznego” poziomu hemoglobiny we krwi (7,0 g/dl) oraz wskaźnika hematokrytowego 0,24 stanowi niewątpliwie dolną granicę, której generalnie nie powinno się lekceważyć, zwłaszcza w tych przypadkach, w których nie można szybko uzupełnić objętości krwi krążącej poprzez proste wyrównanie niedoborów substancji krwiotwórczych lub zastosowanie środków krwiozastępczych.
Nawet w przewlekłych, powoli narastających niedokrwistościach, ludzie w starszym wieku ze współistniejącymi chorobami układu krążenia i ośrodkowego układu nerwowego (o u n) mogą ujawniać nasilone objawy kliniczne niedokrwistości przy niezbyt niskich wartościach hemoglobiny (np. poniżej 9 g/dl).
U chorych na nowotwory, u których niedokrwistość może ulegać pogłębieniu wskutek leczenia cytostatykami lub/i radioterapią jej zwalczanie ma dodatkowe uzasadnienie, gdyż może zapobiegać lub opóźniać procesy angiogenezy.
Ustalenia różnych Towarzystw Naukowych w Europie i w Stanach Zjednoczonych doprowadziły ostatnio do przedstawienia schematu ze wskaźnikami i wytycznymi, które należy uwzględniać przy rozważaniu wskazań do leczenia krwią zwłaszcza u chorych na nowotwory (tab. 7).
Tabela 7. Wskazówki i wytyczne przetaczania krwi chorym z przewlekłą niedokrwistością.
Czynniki do rozważenia:
? naturalny przebieg choroby
? przewidywane przeżycie chorych
? nagłość rozwoju niedokrwistości
? fizjologiczne mechanizmy adaptacyjne
? wydolność krążeniowo-oddechowa
? współistnienie zmian niedokrwiennych
? stężenie hemoglobiny i wartość hematokrytu
? objawy podmiotowe niedokrwistości zgłaszane przez chorego
Podjęcie decyzji:
? oddzielna analiza każdego przypadku
? odrębne uzasadnienie przetoczenia każdej jednostki
Krytyczny poziom Hb/Ht:
? 8 g/dl/0,24 (7 g/dl/0,21-9,0 g/dl/0,27)
|
Poza wymienionymi w tej tabeli czynnikami istotne znaczenie mają również i inne kryteria np. wiek i płeć chorego, a przede wszystkim dotychczasowa „historia” przetoczeń krwi, w tym zwłaszcza ich skuteczność, występowanie reakcji niepożądanych lub powikłań poprzetoczeniowych.
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
24 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
59 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
119 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 28 zł
Piśmiennictwo
1. Aapro M.S. et al.: Age, anemia and fatigue. Semin.Oncol. 2002, 29 (Suppl. 8):55-59.
2. Carelle N. et al.: Changing patients of the side effects of cancer chemotherapy. Cancer, 2002, 95:155-163.
3. Casadevall N.: Antibodies against rHuEPO: native and recombinant. Nephrol.Dial.Transplant. 2002, 17 (Suppl. 5):42-47.
4. Casadevall N. et al.: Pure red-cell aplasia and antierythropoietin antibodies in patients treated with recombinant erythropoietin. New Engl. J. Med. 2002, 346:469-475.
5. Cella D. et al.: Advances in quality measurements in oncology patients. Semin. Oncol. 2002, 29 (Suppl. 8):60-88.
6. Dicato M., Harper P.: The optimal hemoglobin level in the cancer patient. Semin. Oncol. 2002, 29 (Suppl. 8):88-91.
7. Glaspy J. et al.: Comparable efficacy of epoetin alfa for anemic cancer patients receiving platinum and nonplatinum - based chemotherapy: a retrospective subanalysis of two large, community-based trials. The Oncologist, 2002, 7:126-135.
8. Littlewood T., Mandelli F.: The effects of anemia in hematologic malignancies: more than a symptom. Semin. Oncol.. 2002, 29, (Suppl. 8):40-45.
9. Ludwig H et al.: Management of disease - related anemia in patients with multiple myeloma or chronic lymphocytic leukemia: epoietin treatment recommendations. Hemat. J. 2002, 3:121-130.
10. Ludwig H.: Anemia of hematologic malignancies: what are the treatment options? Semin. Oncol. 2002, 29 (suppl. 8):45-54.

