© Borgis - Postępy Fitoterapii 3/2015, s. 144-152
Katarzyna Karłowicz-Bodalska1, Stanisław Han1, Tomasz Han2, Kornelia Koppa3, Ilona Krzak3, Marzena Ruszkiewicz4, *Adam Kowalczyk4
Wybrane rośliny lecznicze stosowane w menopauzie
Some selected medicinal plants for menopausal symptoms
1Zakład Farmacji Przemysłowej, Wydział Farmaceutyczny, Uniwersytet Medyczny we Wrocławiu
Kierownik Zakładu: dr Stanisław Han
2Przedsiębiorstwo Produkcji Farmaceutycznej Hasco-Lek S.A.
3Studenckie Koło Naukowe, Zakład Farmacji Przemysłowej, Wydział Farmaceutyczny, Uniwersytet Medyczny we Wrocławiu
Opiekun Koła: mgr farm. Katarzyna Karłowicz-Bodalska
4Katedra i Zakład Farmakognozji, Wydział Farmaceutyczny, Uniwersytet Medyczny we Wrocławiu
Kierownik Zakładu: dr hab. Izabela Fecka
Summary
In the literature of the recent years much attention has been paid to the therapy of the estrogen deficiency-related menopausal complaints, among them cardiovascular disease, emotional instability, depression, sleep disturbances and osteoporosis are the most difficult ones. Hormone/estrogen replacement therapy (HRT/ERT) is the most common method used by women to alleviate the menopausal symptoms. Recently some studios have been shown, that longterm treatment with HRT can cause the increased occurrence of the negative side effects such as breast cancer, heart diseases or strokes. This is the reason of actually great interest to the complementary and alternative medicine and to herbal nonsteroid compounds with the similar activity to estrogens in order to replace them in the diet preparations, administered in menopause. Worth of mentioning is also common known chemopreventive activity of many herbal substances. This review describes investigation results of 11 plants: Rheum raponticum L. (Polygonaceae), Cyclopia genistoides, C. subternata Vogel (Fabaceae), Glycyrrhiza glabra, G. inflata, G. uralensis (Leguminosae), Humulus lupulus L. (Cannabaceae), Nigella sativa L. (Ranunculaceae), Agrimonia pilosa Ledeb. (Rosaceae), Labisia pumila var. alata (Myrinaceae), Crotalaria pallida Ailton (Fabaceae) in aspect of their estrogen properties, which (according to the opinion of their authors) could be helpful as prospective natural substances, effective in menopausal disorders.

Wstęp
Menopauza jest okresem powolnego zmniejszania się zdolności rozrodczych kobiety, który spowodowany jest postępującym zanikaniem syntezy estrogenów. Następstwem tego jest stopniowe zmniejszenie aktywności jajników, co prowadzi początkowo do nieregularnego, później całkowitego ustania miesiączkowania. Objawami menopauzy są uderzenia krwi do głowy, uzewnętrzniające się nagłym zaczerwienieniem twarzy, nocne poty, problemy z zasypianiem, osteoporoza oraz inne choroby, obserwowane u kobiet w tym okresie.
W opracowaniu przeglądowym Gryszczyńskiej i wsp. (1) zostały przedstawione badania wpływu medycyny alternatywnej na stan pacjentek menopauzalnych lub postmenopauzalnych, leczonych hormonalną terapią zastępczą (ang. hormone replacement therapy – HRT), którą stanowią estrogen i/lub progesteron. Na podstawie wieloletnich badań zaobserwowano, że oba hormony działają korzystnie nie tylko w łagodzeniu objawów menopauzy. Stosowanie terapii HRT zapobiega także utracie gęstości kości, zmniejszając ryzyko występowania osteoporozy o ok. 50%, oraz śmiertelności z powodu chorób serca i układu krążenia o ok. 35%. To korzystne działanie terapii HRT występuje jednak tylko wówczas, gdy trwa ona stosunkowo krótko. Po dłuższym stosowaniu HRT (trwającym ok. 5 lat) następuje odwrócenie działania – obserwuje się zwiększenie ryzyka wystąpienia licznych chorób, łącznie z chorobą niedokrwienną serca, nowotworową dróg rodnych, raka piersi i wątroby, może również wystąpić udar mózgu, zwłaszcza u starszych kobiet (2-7). We wspomnianym wyżej opracowaniu opisano również wyczerpująco działanie i skład chemiczny najczęściej wykorzystywanych roślin leczniczych bądź otrzymywanych z nich produktów naturalnych w menopauzie, a także w leczeniu niektórych chorób pojawiających się w tym okresie.
Wśród roślin korzystnie działających w menopauzie wymienić należy przede wszystkim gatunki zawierające substancje o strukturze niesteroidowej, lecz o działaniu zbliżonym do naturalnych i syntetycznych estrogenów, tzw. fitoestrogeny, które stanowią naturalną grupę substancji egzogennych (ksenoestrogenów). Liczne badania potwierdziły działanie fitoestrogenne m.in. w klasie polifenoli, takich substancji, jak powszechnie występujące w roślinach związki flawonoidowe (grupa pochodnych fenylochromonu, do których należą flawony, flawonole, flawanony, chalkony, izoflawonoidy) (ryc. 1) oraz wśród lignanów i stilbenów. Znaczącą aktywność fitoestrogenną odnotowano zwłaszcza w podgrupie izoflawonów (pochodnych 3-fenylo-chromonu). Związki te znajdują się głównie w gatunkach rodziny strączkowych (Fabaceae).
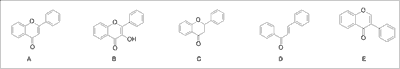
Ryc. 1. Struktury wybranych związków flawonoidowych o działaniu fitoestrogennym: A. flawon, B. flawonol, C. flawanon, D. chalkon, E. izoflawon.
Biorąc powyższe pod uwagę, Bouè i wsp. (8) przeprowadzili badanie aktywności estrogennej wyciągów metanolowych z 6 roślin pochodzących z tej rodziny: Glycine max L. – soja, Phaseolus vulgaris L. – fasola zielona, Medicago sativa L. – lucerna polna, Vigna radiata L. – fasola mung, Pueraria lobata L. – kudzu i Trifolium pratense L. – koniczyna łąkowa. Wśród aktywnych izoflawonów autorzy zidentyfikowali w badanych surowcach daidzeinę, daidzynę, genisteinę, genistynę, puerarynę, formononetynę, kumestrol i biochaninę A (ryc. 2).
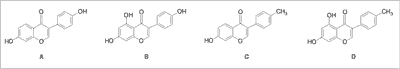
Ryc. 2. Struktury wybranych izoflawonów o działaniu estrogennym: A. daidzeina, B. genisteina, C. formononetyna, D. biochanina.
Związki te wykazują zdolność wiązania wewnątrzkomórkowych receptorów estrogenowych (RE), odpowiedzialnych za wzrost, różnicowanie i funkcję wielu komórek. Według aktualnych danych, receptory estrogenowe występują w postaci dwóch głównych izoform (RE-α i RE-β), kodowanych przez dwa różne geny. Obie izoformy wykazują analogiczną budowę chemiczną; różnią się jedynie sekwencją aminokwasów, rozmieszczeniem w tkankach i narządach, powinowactwem z ligandami oraz pełnioną funkcją w organizmie (1-2, 9). Podobne, chociaż znacznie słabsze działanie wykazują również pochodne 2-fenylochromonu, np. flawony i flawonole (glukozyd i glukuronid apigeniny, glukuronid luteoliny, kemferol i kwercetyna, niektóre pochodne hydroksylowe chalkonu), a także kumestany, lignany i inne (10-12).
Aktywność terapeutyczna izoflawonów w porównaniu z HRT jest jednak znacznie słabsza i wymaga dłuższego stosowania roślinnych produktów estrogennych w celu uzyskania nie zawsze w pełni oczekiwanego efektu leczniczego. Mimo tych niedogodności medycyny alternatywnej obserwuje się aktualnie duże zainteresowanie roślinami bądź produktami roślinnymi zawierającymi fitoestrogeny. Ważnym powodem, skłaniającym do coraz szerszego stosowania tych naturalnych źródeł estrogenów jako suplementów diety, zwłaszcza w okresie postmenopauzalnym, jest ich korzystny wpływ na masę i uwapnienie kości w osteoporozie, zmniejszenie ryzyka rozwoju hormonozależnych nowotworów raka piersi, raka prostaty, miażdżycy tętnic, choroby niedokrwiennej serca, demencji, objawów depresji oraz, co ma istotne znaczenie, przeważnie brak niepożądanych efektów ubocznych (2, 13-15).
Moreira i wsp. (16) podkreślają, że lepsze zrozumienie objawów patofizjologii związanych z okresem menopauzy oraz postępujący rozwój nowych strategii polepszających leczenie tych objawów są ważnym wyzwaniem dla klinicystów. Autorzy opisują fizjologiczne i hormonalne zmiany obserwowane w okresie menopauzy. Krytycznie oceniają rezultaty leczenia tradycyjną HRT, rozważając możliwość zastosowania fitoestrogenów jako alternatywnej metody w kontekście minimalizowania objawów menopauzy.
Ponieważ zagadnienie stosowania w menopauzie roślin wykazujących działanie estrogenne budzi powszechne zainteresowanie wielu ośrodków naukowych, celem niniejszego doniesienia jest prześledzenie dalszych opracowań związanych z badaniami fitoestrogenów w aspekcie łagodzenia objawów menopauzy oraz podsumowanie uzyskanych wyników.
Rheum raponticum L.
Vollmer i wsp. (17) prześledzili dane piśmiennictwa dotyczące badań in vitro i in vivo aktywności estrogennej narządów podziemnych rzewienia ogrodowego Rheum raponticum L., rodz. Polygonaceae. Surowcowi temu przypisuje się właściwość łagodzenia poważnych symptomów klimakteryjnych, wraz z polepszeniem stanu zdrowia i samopoczucia u kobiet w okresie okołomenopauzalnym. Autorzy opisali efektywność stosowania ekstraktu z kłączy rzewienia ogrodowego (ERr) w łagodzeniu symptomów menopauzy po przeprowadzeniu randomizowanych, kontrolowanych placebo badań na 54 pacjentkach z dolegliwościami klimakteryjnymi, którym podawano preparat w ilości 4 mg/dziennie przez 3 miesiące. Poza znacznym ustąpieniem objawów menopauzy w porównaniu z kontrolą (wg Menopause Rating Scale II), u badanych pacjentek potwierdzono działanie sedatywne wg skali Hamiltona (Hamilton Anxiety Scale). Nie stwierdzono przy tym niekorzystnych zmian w badaniach ginekologicznych, testowanych parametrach laboratoryjnych ani w badaniu śluzówki macicy (17). Podawanie pacjentkom preparatu ERr nawet przez okres 48-96 tygodni nie skutkowało przerostem endometrium ani innymi szkodliwymi efektami ubocznymi (18, 19).
Związkami biologicznie czynnymi rzewienia ogrodowego są pochodne stilbenu, głównie rapontycyna (ok. 90%) i dezoksyrapontycyna, oraz ich aglikony: rapontygenina i deoksyrapontygenina (ryc. 3). Pozostałe hydroksystilbeny są pochodnymi resweratrolu.
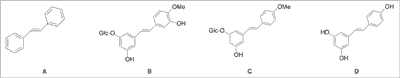
Ryc. 3. Struktury związków czynnych rzewienia ogrodowego: A. stilben, B. rapontycyna, C. dezoksyrapontycyna, D. resweratrol.
Ekstrakt metanolowy z kłączy rzewienia ogrodowego (ERr) jest w handlu dostępny i bezpieczny, pozbawiony niepożądanych efektów ubocznych, mimo że syntetyczny dietylostilbestrol, o podobnej strukturze do hydroksystilbenów, wykazuje szkodliwe działanie przezłożyskowe u kobiet (20). Stwierdzono ponadto, że ERr (lub jego komponenty) wykazuje właściwość selektywnego modulatora receptora estrogenowego (SERM) (21). Znane SERM (jak Raloxifen czy Tamoxifen) obniżają ryzyko raka piersi i podwyższają gęstość kości. Natomiast zagadnienie, czy i w jaki sposób receptor estrogenowy ER lub jego podtypy (izoformy) wpływają na mechanizm wiązania tych związków, nadal nie zostało wyjaśnione. Funkcja receptora ERβ, który wydaje się odgrywać ważną rolę w mechanizmie działania wyciągu, sprowadza się jak dotąd do pośredniczenia w uzyskiwaniu efektu uspokajającego. Konkludując, autorzy uważają, że dotychczasowe badania potwierdzają korzystne działanie hydroksystilbenów rzewienia w łagodzeniu objawów menopauzalnych.
Cyclopia spp.
Visser i wsp. (22) badali właściwości estrogenne ekstraktów otrzymanych z dwóch gatunków rodzaju Cyclopia (C. genistoides i C. subternata), rodz. Fabaceae, roślin pochodzących z Południowej Afryki, używanych do sporządzania aromatycznego napoju (honeybush), który wykazuje wielokierunkowe działanie lecznicze. Skład chemiczny cyklopii stanowią głównie flawonoidy o różnej aktywności estrogennej: luteolina, eriodykcjol, naryngenina i formononetyna, oraz dwa izomeryczne C-glukozydy pochodne ksantonu: mangiferyna i izomangiferyna (ryc. 4) (23, 24).
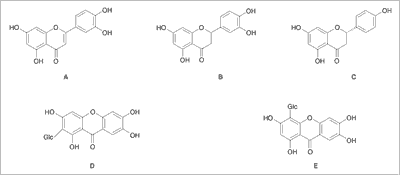
Ryc. 4. Struktury wybranych związków aktywnych Cyclopia spp. o właściwościach estrogennych: A. luteolina, B. eriodykcjol, C. naryngenina, D. mangiferyna, E. izomangiferyna.
W przeprowadzonych badaniach Verhoog i wsp. (23) oceniali aktywność kilku ekstraktów z cyklopii i wykazali, że wszystkie badane wyciągi są antagonistami ERα, podczas gdy dwa z nich wykazują równocześnie agonizm wobec ERβ oraz że ekstrakt z C. genistoides ulega transaktywacji jedynie przez ERβ, chociaż jest wiązany przez obie izoformy. W rezultacie uzyskane wyniki sugerują, że ekstrakty z cyklopii, wykazujące powyższe własności, mogą stanowić naturalne, bezpieczne źródło tego surowca do leczenia osteoporozy lub zapobiegania osteoporozie i innym symptomom premenopauzy. Obecne w cyklopii zespoły polifenoli mogą również zawierać dotąd niezidentyfikowane związki o analogicznej aktywności, z polepszonym profilem ryzyka oraz dodatkowo z właściwościami chemoochronnymi.
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
24 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
59 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
119 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 28 zł
Piśmiennictwo
1. Gryszczyńska A, Gryszczyńska B, Opala B i wsp. Zastosowanie roślin leczniczych w menopauzie. Post Fitoter 2012; Cz. I, 79-92; Cz. II, 173-83. 2. Woźniak M, Murias M. Ksenoestrogeny: substancje zakłócające funkcjonowanie układu hormonalnego. Ginekol Pol 2008; 79:785-90. 3. Lockler TD, Huang Y, Frasor J i wsp. Estrogenic and progestagenic effects of extracts of Justicia pectoralis Lacq, in herbal medicine from Costa Rica used for treatment of menopause and PMS. Maturitas 2010; 66:315-22. 4. Frei-Kleiner S, Schaffner W, Rahls VW i wsp. Cimicifuga racemosa dried ethanolic extract in menopausal disorders: a double-blind placebo-controlled clinical trial. Maturitas 2005; 51:397-404. 5. Wuttke W, Seidlova-Wuttke D i wsp. The Cimicifuga preparation BNO 1055 vs. conjugated estrogens in a double-blind placebo-controlled study: effects on menopause symptoms and bone markers. Maturitas 2003; 44, 1:67-77. 6. Seidlova-Wuttke D, Jarry H, Becker T i wsp. Pharmacology of Cimicifuga racemosa extract BNO 1055 in rats: bone, fet and uterus. Maturitas 2003; 44, 1:39-50. 7. El-Shitany NA, Hegazy S, El-Desoky K. Evidence of antiosteoporotic and selective estrogen receptor modulation activity of sylimarin compared with ethinylestradiol in ovariectomized rats. Phytomed 2010; 17:116-25. 8. Bouè SM, Wiese TE, Nehls S i wsp. Evaluation of the estrogenic effect of legume extracts containing phytoestrogens. J Agric Food Chem 2003; 51:2193-9. 9. Michel T, Halabalaki M, Skaltsounis AL. New concepts, experimental approaches and dereplication strategies for the discovery of novel phytoestrogens from natural sources. Planta Med 2013; 79:514-32. 10. Huntley AL, Ernst E. A systematic review of herbal medicinal products for the treatment of menopausal symptoms. Menopause 2000; 10, 5:465-76. 11. Mhady GB, Parrot J, Lee C i wsp. Botanical dietary supplement use in peri- and postmenopausal women. Menopause 2003; 10:65-72. 12. Beck V, Unterrieder E, Krenn L i wsp. Comparison of hormonal activity (estrogen, androgen and progestin) of standardized plant extracts for large scale use in hormone replacement therapy. J Stereo Biochem Mol Biol 2003; 84:259-68. 13. Panay N. Taking an integrated approach: managing women with phytoestrogens. Climacteric 2011; 14:2-7. 14. Usui T. Pharmaceutical prospects of phytoestrogens. Endocr J 2006; 53:7-20. 15. Kris-Etherton P, Hecker P, Bonanome A i wsp. Bioactive compounds in foods: their role in the prevention of cardiovascular disease and cancer. Am J Med 2002; 113 (suppl. 9B):71-88. 16. Moreira AC, Silva AM, Santos MS i wsp. Phytoestrogens as alternative hormone replacement therapy in menopause: What is real, what is unknown. J Steroid Biochem Mol Biology 2014; 143:61-71. 17. Vollmer G, Papke A i Zierau O. Treatment of menopausal symptoms by an extract from the roots of rhapontic rhubarb: the role of estrogen receptors. Chinese Med 2010; 5:7. 18. Heger M, Ventskovskyj BM, Borzenko I i wsp. Efficacy and safety of a special extract of Rheum raponticum (Err 731) in perimenopausal women with climacteric complaints: a 12-week randomized, double blind, placebo-controlled trial. Menopause 2006; 13:744-59. 19. Kaszkin-Betag M, Ventskovskyj BM, Krawczenko A i wsp. The special extract Err 731 of the roots of Rheum raponticum decreases anxiety and improves health state and general well-being in perimenopausal women. Menopause 2007; 14:270-83. 20. Herbst AL. Diethylstilbestrol and adenocarcinoma of the vagina. Am J Obstet Gynecol 1999; 181:1576-8. 21. Crabtree JS, Peano BJ, Zhang X i wsp. Activity of three selective estrogen receptor modulators on hormone-dependent responses on the mouse uterus and mammary gland. Mol Cell Endocrinol 2008; 1-2:40-6. 22. Visser K, Mortimer M, Louw A. Cyclopia extracts act as ERα antagonists and ERβ agonists, in vitro and in vivo. PLoS ONE 2013; 8:e79223. 23. Verhoog NJ, Joubert E, Louw A. Evaluation of the phytoestrogenic activity of Cyclopia genistoides (honeybush) methanol extracts and relevant polyphenols. J Agric Food Chem 2007; 55:4371-81. 24. Kamara BJ, Brand DJ, Brandt EV i wsp. Phenolic metabolites from honeybush tea Cyclopia subternata. J Agric Food Chem 2004; 52:5391-5. 25. Kokotkiewicz A, Łuczkiewicz M, Sowiński P i wsp. Isolation and structure elucidation of phenolic compounds from Cyclopia subternata Vogel (honeybush) intact plant and in vitro cultures. Food Chem 2012; 133:1373-82. 26. Mfenyana C, De Beer D, Joubert E, Louw A. Selective extraction of Cyclopia for enhanced in vitro phytoestrogenicity and benchmarking against commercial phytoestrogen extracts. J Steroid Biochem Molecular Biol 2008; 112:74-86. 27. Hajirahimkhan A, Simmler C, Yuan Y i wsp. Evaluation of estrogenic activity of Licorice species in comparison with hops used in botanicals for menopausal symptoms. PLoS ONE 2013; 8:e67947. 28. Dietz BM, Kang YH, Liu G i wsp. Xanthohumol isolated from Humulus lupulus inhibits menadione-induced DNA damage through induction of quinone reductase. Chem Res Toxicol 2005; 18:1296-305. 29. Over CR, Yao P, Chadwick LR i wsp. Comparison of the in vitro estrogenic activities of compounds from hops (Humulus lupulus) and red clover (Trifolium pratense). J Agric Food Chem 2005; 53:6246-53. 30. Taylor M. Complementary and alternative medicine preparations used to treat symptoms of menopause. Men Med 2012; 210:1-8. 31. Ibrahim RM, Hamdan NS, Mahmud R. A randomised controlled trial on hypolipidemic effects of Nigella sativa seeds powder in menopausal women. J Translat Med 2014; 12:82. 32. Lee YM, Kim JB, Bae JH i wsp. Estrogen-like activity of aqueous extract from Agrimonia pilosa Ledeb. in MCF-7 cells. Complement Altern Med 2012; 12:260. 33. Kato H, Li W, Koike M i wsp. Phenolic glycosides from Agrimonia pilosa. Phytochem 2010; 71(16):1925-9. 34. Nazrun AS, Ping LL, Norliza M i wsp. The effects of Labisia pumila var. alata on bone markers and bone calcium in a rat model of postmenopausal osteoporosis. J Ethnopharmacol 2010; 133:538-42. 35. Fathilah SN, Ahmad NS, Norazlina M i wsp. Labisia pumila protects the bone of estrogen-deficient rat model: a histomorphometric study. J Ethnopharmacol 2012; 142:294-9. 36. Fathilah SN, Mohamed N, Muhammad N i wsp. Labisia pumila regulates bone-related genes expressions in postmenopausal osteoporosis model. Complement Altern Med 2013; 13:217. 37. Boldrin KP, Resende FA, Hohne APO i wsp. Estrogenic and mutagenic activities of Crotalaria pallida measured by recombinant yeast assay and Ames test. Complement Altern Med 2013; 13:216. 38. Masullo M, Montoro P, Mari A i wsp. Medicinal plants in the treatment of women’s disorders analytical strategies to assure quality, safety and efficacy. J Pharm Biomed Anal 2015; 12 (w druku). 39. Girardi A, Piccinni C, Raschi E i wsp. Use of phytoestrogens and effects perceived by postmenopausal women: results of a questionnaire-based survey. BMC Complement Altern Med 2014; 14:262. 40. Depypere HT, Comhaire FH. Herbal preparations for the menopause: Beyond isoflavones and black cohosh. Maturitas 2014; 77:191-4.




