*Dorota Olczak-Kowalczyk1, Maria Borysewicz-Lewicka2, Barbara Adamowicz-Klepalska3, Teresa Jackowska4, Urszula Kaczmarek5
Stanowisko polskich Ekspertów dotyczące indywidualnej profilaktyki fluorkowej choroby próchnicowej u dzieci i młodzieży
Consensus statement of Polish experts on individual caries prevention with fluoride in children and adolescents
1Department of Paediatric Dentistry, Medical University of Warsaw; national consultant in paediatric dentistry
Head of Department: prof. Dorota Olczak-Kowalczyk, MD, PhD
2Chair and Clinic of Paediatric Dentistry, Karol Marcinkowski University of Medical Sciences in Poznań
Head of Chair and Clinic: prof. Maria Borysewicz-Lewicka, MD, PhD
3Former national consultant in paediatric dentistry
4Department of Paediatrics, Centre of Postgraduate Medical Education, Warsaw; national consultant in paediatrics
Head of Department: prof. Teresa Jackowska, MD, PhD
5Chair and Department of Conservative Dentistry and Pedodontics, Wrocław Medical University of Silesian Piasts
Head of Chair and Department: prof. Urszula Kaczmarek, MD, PhD
1,2,3,5The Alliance for a Cavity-Free Future, Polish Society of Pediatric Dentistry
Streszczenie
Jednym z głównych elementów zapobiegania chorobie próchnicowej jest stosowanie środków profilaktycznych zawierających związki fluoru. Skuteczność i bezpieczeństwo profilaktyki fluorkowej wymaga znajomości mechanizmu kariostatycznego działania fluoru oraz przestrzegania zasad stosowania środków profilaktycznych zawierających fluorki. W ramach działalności Grupy Roboczej ds. Profilaktyki Fluorkowej Polskiego Oddziału Sojuszu dla Przyszłości Wolnej od Próchnicy (ACFF) powołano zespół Ekspertów w dziedzinie stomatologii dziecięcej i pediatrii w celu opracowania stanowiska dotyczącego indywidualnej profilaktyki fluorkowej u dzieci i młodzieży w Polsce.
Dokonano przeglądu piśmiennictwa dotyczącego stomatologicznych potrzeb profilaktycznych pacjentów w wieku rozwojowym w Polsce, skuteczności i bezpieczeństwa stosowania środków profilaktycznych zawierających związki fluoru oraz zaleceń towarzystw naukowych w zakresie profilaktyki fluorkowej. Opracowaną pierwszą wersję dokumentu zrecenzował zespół Ekspertów w dziedzinie pediatrii i stomatologii dziecięcej oraz przedstawiciele rodziców/opiekunów dzieci. Ostateczny dokument został zaakceptowany przez zespół Ekspertów 12 grudnia 2015 roku. Aktualizację zaplanowano nie później niż po 5 latach od jego publikacji.
Dokument zawiera podstawowe informacje dotyczące potrzeb w zakresie zapobiegania próchnicy zębów u dzieci i młodzieży, mechanizmu przeciwpróchnicowego działania fluoru, bezpieczeństwa i skuteczności różnych metod profilaktyki fluorkowej i zasad jej stosowania w zależności od wieku i poziomu ryzyka próchnicy.
Summary
Using fluoride agents is one of key elements of caries prevention. For it to be safe and effective, it is crucial to know the cariostatic mechanisms of fluoride and follow the guidelines of fluoride use for caries prevention. Experts in paediatric dentistry and paediatrics prepared, within the The Alliance for a Cavity-Free Future working group (ACFF), guidelines on individual caries prevention for children and adolescents in Poland.
Publications featuring the need for prevention in children and adolescents in Poland, the effectiveness and safety of preventive fluoridation methods and guidelines of scientific societies on caries prevention have been reviewed. The first draft was reviewed by paediatricians, paediatric dentists, and the representatives of parents/legal guardians of patients. The final version of the document was approved on 12 December 2015. It will be updated not later than five years after it is published.
The document defines the basics of preventing dental caries in children and adolescents, the anticaries mechanisms of fluoride, the safety and effectiveness of different fluoridation methods, and their use depending on patient age and risk of caries.

Wprowadzenie
Filarami zapobiegania chorobie próchnicowej są: prawidłowe odżywianie, dbałość o higienę jamy ustnej oraz stosowanie środków profilaktycznych zawierających fluorki. Fluorki wykorzystywane są w masowych, grupowych oraz indywidualnych działaniach zapobiegawczych. Światowa Organizacja Zdrowia (WHO) i Światowa Federacja Dentystyczna (FDI) rekomendują ich stosowanie, podkreślając profilaktyczną skuteczność i bezpieczeństwo fluorków, zwracając jednocześnie uwagę na konieczność monitorowania ekspozycji i oceny ich efektywności działania (1-3).
W profilaktyce indywidualnej fluor może być dostarczany:
– doustnie (tabletki lub krople) – metoda endogenna (suplementacja) i wówczas wpływa na rozwijające się szkliwo zębów,
– zewnętrznie – metoda egzogenna, przez miejscową aplikację na wyrznięte zęby.
Pasty do zębów, płukanki, pianki, żele i lakiery zawierają różne stężenia związków fluoru. Mogą być one stosowane w domu (profilaktyka domowa) lub w gabinecie stomatologicznym (profilaktyka profesjonalna). Warunkiem skuteczności i bezpieczeństwa profilaktyki fluorkowej jest przestrzeganie zasady indywidualnego doboru metod profilaktycznych, z uwzględnieniem: ekspozycji na związki fluoru pochodzące z różnych źródeł, wieku dziecka oraz poziomu ryzyka próchnicy. Zgodnie z wynikami badań ankietowych przeprowadzonych w 2014 roku w Polsce 14% lekarzy dentystów nie dokonuje oceny ryzyka próchnicy przed wyborem metody profilaktycznej. Ponad połowa ankietowanych uważa, że profilaktyka fluorkowa powinna być stosowana u każdego pacjenta, 38,9% – przy wysokim ryzyku próchnicy niezależnie od wieku, a 21,3%, iż tylko w okresie uzębienia mlecznego i mieszanego (4).
Należy podkreślić, że w Polsce profilaktyka fluorkowa w podstawowym zakresie może być realizowana w ramach świadczeń gwarantowanych finansowanych ze środków publicznych (Wykaz świadczeń ogólnostomatologicznych dla dzieci i młodzieży do ukończenia 18. roku życia oraz Wykaz świadczeń stomatologicznych dla dzieci od 6. miesiąca życia do ukończenia 19. roku życia w formie 13 zróżnicowanych dla wieku pakietów działań zapobiegawczych).
W 2013 roku opublikowano stanowisko Niezależnego Panelu Ekspertów na temat indywidualnej profilaktyki fluorkowej (5). W związku z nowymi badaniami naukowymi i metaanalizami wykazującymi różnice w zakresie skuteczności różnych środków profilaktycznych zawierających fluorki w zapobieganiu próchnicy zębów i bezpieczeństwa stosowania konieczna jest aktualizacja tego dokumentu.
Metodyka
Grupa Robocza ds. Profilaktyki Fluorkowej Polskiego Oddziału Sojuszu dla Przyszłości Wolnej od Próchnicy (ACFF) dokonała przeglądu piśmiennictwa dotyczącego stomatologicznych potrzeb profilaktycznych dzieci i młodzieży w Polsce, mechanizmu działania, skuteczności i bezpieczeństwa stosowania związków fluoru w zapobieganiu próchnicy zębów w tej grupie wiekowej oraz analizy zaleceń dotyczących profilaktyki fluorkowej towarzystw naukowych, m.in. Amerykańskiej Akademii Stomatologii Dziecięcej (AAPD), Europejskiej Akademii Stomatologii Dziecięcej (EAPD) i Amerykańskiego Towarzystwa Stomatologicznego (ADA). Uzyskane informacje stanowiły podstawę opracowania pierwszej wersji dokumentu przez prof. Dorotę Olczak-Kowalczyk i prof. Urszulę Kaczmarek. Wersja ta została przekazana Ekspertom w dziedzinie pediatrii (prof. Teresa Jackowska) i stomatologii dziecięcej (prof. Barbara Adamowicz-Klepalska i prof. Maria Borysewicz-Lewicka) oraz przedstawicielom rodziców dzieci. Po uwzględnieniu ich uwag opracowano ostateczną wersję dokumentu, który został zaakceptowany przez zespół Ekspertów 30 listopada 2015 roku. Jego aktualizację zaplanowano nie później niż po 5 latach od publikacji.
Wyniki
Potrzeby w zakresie zapobiegania próchnicy zębów u polskich dzieci
Na potrzeby w zapobieganiu chorobie próchnicowej u polskich dzieci wskazują wyniki ogólnopolskich badań epidemiologicznych realizowanych od 1987 roku we współpracy ze Światową Organizacją Zdrowia (6-9). Wyniki badań monitoringowych stanu zdrowotnego jamy ustnej wskazują, że u dzieci w wieku od 3 do 6 lat około dwukrotnie – z 2,7 do 5,3 – wzrasta liczba zębów mlecznych dotkniętych chorobą próchnicową i o ok. 30% częstość występowania próchnicy – z 57,2 do 85,6%. W wieku 12 lat próchnicą objętych jest średnio 2,8 zębów stałych i liczba ta po upływie kolejnych 3 lat życia wzrasta ponad dwukrotnie (w wieku 15 lat wynosi 6,12), a po następnych 3 latach 2,4-krotnie – w wieku 18 lat osiąga wartość 7,65 (10-14). Niepokojące jest stwierdzanie próchnicy w wyrzynających się zębach stałych pierwszych trzonowych, stwierdza się ją u 3/100 dzieci w wieku 5 lat, u 18/100 w wieku 6 lat i u 56/100 w wieku 7 lat (12, 14). Rozpatrując trend choroby próchnicowej u dzieci 12-letnich, w okresie 27 lat (1987-2014) stwierdzono tendencję spadkową frekwencji (z 89,9 do 75,9%) oraz intensywności próchnicy (z 4,4 do 2,8 zębów dotkniętych próchnicą) (6, 13). Tymczasem dla tej grupy wiekowej przewidziany do realizacji do 2000 roku globalny cel zdrowia jamy ustnej Światowej Organizacji Zdrowia i Światowej Federacji Dentystycznej zakładał występowanie tylko 3 lub mniej zębów objętych procesem próchnicowym (15, 16). Powyższy cel został osiągnięty w 70% krajów świata, tj. w 128 krajach reprezentujących 85% światowej populacji, a średnia globalna wartość zębowego wskaźnika próchnicy PUW/Z wynosiła 1,74 (17). Niestety, tylko 48,9% polskich dzieci ten cel zdrowia jamy ustnej uzyskało w 2000 roku, a po upływie 10 lat tylko ok. 10% więcej dzieci (58,7%) (13, 18).
Przytoczone dane podkreślają ważność wzmocnienia stomatologicznych działań zapobiegawczych w Polsce oraz konieczność zaangażowania w nie, oprócz personelu stomatologicznego, także personelu medycznego oraz opiekunów dzieci (19, 20).
Badania epidemiologiczne potwierdziły także polaryzację próchnicy, tj. występowanie osób z bardzo wysoką intensywnością choroby nawet przy ogólnie niskich lub umiarkowanych średnich wskaźnikach intensywności próchnicy. Dlatego zasadne jest wyodrębnienie osób z wysokim ryzykiem próchnicy i stosowanie u nich intensywnych, indywidualnie ukierunkowanych działań profilaktycznych.
Ryzyko choroby próchnicowej a profilaktyka fluorkowa
Wybór metody profilaktyki fluorkowej oraz rodzaju środków profilaktycznych zawierających fluor uwarunkowany jest wieloma czynnikami, w tym wiekiem dziecka, ogólnym stanem zdrowia, stosowaną terapią lekową ogólnoustrojową, potrzebami profilaktyczno-leczniczymi, poziomem ryzyka próchnicy, ekspozycją na fluor pochodzący z różnych źródeł, a także stopniem zaangażowania i możliwościami rodziców. Zapobieganie próchnicy oparte na ocenie poziomu ryzyka próchnicy polega na intensyfikacji profilaktyki przy wzroście ryzyka choroby. Wszystkie dzieci powinny podlegać ocenie ryzyka próchnicy, zanim lekarz dentysta zleci działania zapobiegawcze i kontrolujące próchnicę. Stanowi to krytyczny punkt dla opracowania zindywidualizowanego planu zapobiegawczego.
Ryzyko próchnicy to prawdopodobieństwo wystąpienia nowych zmian próchnicowych w przyszłości i progresji zmian już obecnych. Zgodnie z koncepcją dynamicznej równowagi między demineralizacją a remineralizacją tkanek zęba, ocena ryzyka próchnicy oparta jest na określeniu relacji między czynnikami uznanymi za ochronne (stosowanie profilaktyki fluorkowej, środków antybakteryjnych i laków szczelinowych, właściwe nawyki dietetyczne, prawidłowe wydzielanie śliny), które sprzyjają remineralizacji szkliwa, a czynnikami patologicznymi powodującymi demineralizację (poziom bakterii produkujących kwasy, częstość konsumpcji ulegających fermentacji węglowodanów, zmniejszona sekrecja śliny) oraz na stwierdzeniu indykatorów choroby (obecność początkowych zmian próchnicowych w postaci białych plam, defektów rozwojowych szkliwa zwiększających retencję płytki bakteryjnej, liczby wypełnień zębów założonych w okresie krótszym niż 3 lata oraz liczby ubytków próchnicowych sięgających do zębiny) (21-23).
Brak jest walidowanych narzędzi oceniających ryzyko próchnicy ze znaną czułością i specyficznością u dzieci. Sprawia to, iż wyzwanie stanowi podstawa zaleceń zapobiegawczych związanych z ryzykiem przyszłego rozwoju choroby. Ocena walidowanych narzędzi ryzyka próchnicy u dorosłych wykazała, że narzędzia te nie są wysoce precyzyjne w prognozowaniu przyszłego rozwoju próchnicy. Za najlepszy predyktor indywidualnego rozwoju próchnicy w przyszłości uważa się aktualną obecność zębów dotkniętych procesem próchnicowym. Istnieje kilka metod oceny ryzyka próchnicy zębów. AAPD (American Academy of Pediatric Dentistry) do oceny ryzyka próchnicy zaproponowała system CRA (Caries Risk Assessment), który składa się z trzech narzędzi oceny ryzyka próchnicy, w tym dwóch do zastosowania przez personel stomatologiczny: dla dzieci w wieku 0-5 lat oraz dla dzieci > 6 lat oraz jednego do stosowania przez personel medyczny niestomatologiczny, przeznaczonego dla dzieci w wieku 0-3 lata (tab. 1-3) (24).
Tab. 1. Ocena ryzyka próchnicy u dzieci w wieku 0-5 lat przez personel stomatologiczny w systemie CRA (Caries Risk Assessment Test wg AAPD) (24)
| Czynniki | Wysokie ryzyko | Średnie ryzyko | Niskie ryzyko |
| Czynniki biologiczne |
| U matki/opiekuna aktywne zmiany próchnicowe w zębach | Tak | | |
| Niski status socjoekonomiczny rodziny | Tak | | |
| Dziecko spożywa w ciągu dnia > 3 przekąski zawierające cukier lub słodkie napoje | Tak | | |
| Dziecko zasypia z butelką zawierającą pokarm/płyn z cukrem naturalnym lub cukrem dodanym | Tak | | |
| Dziecko wymaga specjalistycznej opieki pediatrycznej | | Tak | |
| Dziecko pochodzi z rodziny imigranckiej | | Tak | |
| Czynniki ochronne |
| Optymalna ekspozycja endogenna na fluor (woda, tabletki/krople fluorkowe) | | | Tak |
| Codzienne stosowanie pasty do zębów z fluorem | | | Tak |
| Profesjonalna miejscowa aplikacja fluoru | | | Tak |
| Regularne wizyty w gabinecie stomatologicznym/profilaktyka domowa | | | Tak |
| Badanie stomatologiczne |
| puwz > 1 | Tak | | |
| Aktywne białe plamy lub defekty szkliwa zęba | Tak | | |
| Wysoki poziom Streptococcus mutans | Tak | | |
| Obecna płytka nazębna (bakteryjna) | | Tak | |
Tab. 2. Ocena ryzyka próchnicy dla dzieci ≥ 6. roku życia do stosowania przez personel stomatologiczny (24)
| Czynniki | Wysokie ryzyko | Średnie ryzyko | Niskie ryzyko |
| Czynniki biologiczne |
| Niski status socjoekonomiczny | Tak | | |
| Spożywanie codziennie między posiłkami > 3 przekąsek zawierających cukier lub słodkich napojów | Tak | | |
| Konieczność specjalistycznej opieki medycznej | | Tak | |
| Pochodzenie z rodziny imigranckiej | | Tak | |
| Czynniki ochronne |
| Spożywanie wody z optymalną zawartością fluoru | | | Tak |
| Codzienne szczotkowanie zębów pastą z fluorem | | | Tak |
| Profesjonalna miejscowa aplikacja fluoru | | | Tak |
| Stosowanie ksylitolu, pasty MI (Tooth Mousse), środków antybakteryjnych w domu | | | Tak |
| Regularne wizyty w gabinecie stomatologicznym/profilaktyka domowa | | | Tak |
| Badanie stomatologiczne |
| 1 ≥ zmiana próchnicowa na powierzchni stycznej zębów | Tak | | |
| Aktywne białe plamy próchnicowe lub defekty szkliwa | Tak | | |
| Niska sekrecja śliny | Tak | | |
| Wypełnienia z próchnicą wtórną | | Tak | |
| Aparat ortodontyczny lub ruchome uzupełnienia protetyczne | | Tak | |
Tab. 3. Ocena ryzyka próchnicy u dzieci do 3 lat przez personel niestomatologiczny w systemie CRA (Caries Risk Assessment Test wg AAPD) (24)
| Czynniki | Wysokie ryzyko | Niskie ryzyko |
| Czynniki biologiczne | |
| U matki/opiekuna aktywne zmiany próchnicowe w zębach | Tak | |
| Niski status socjoekonomiczny rodziców/opiekunów | Tak | |
| Dziecko spożywa dziennie między posiłkami > 3 przekąski zawierające cukier lub słodkie napoje | Tak | |
| Dziecko zasypia z butelką zawierającą z cukier naturalny lub cukier dodany (zawartość inna niż woda) | Tak | |
| Dziecko wymaga specjalistycznej opieki pediatrycznej | Tak | |
| Dziecko pochodzi z rodziny imigranckiej | Tak | |
| Czynniki ochronne |
| Profilaktyka fluorkowa endogenna (tabletki, krople) lub woda fluorkowana | | Tak |
| Codzienne stosowanie pasty do zębów z fluorem | | Tak |
| Profesjonalna miejscowa aplikacja fluoru | | Tak |
| Regularne wizyty w gabinecie stomatologicznym/działania zapobiegawcze w domu | | Tak |
| Oznaki kliniczne |
| Dziecko ma białe plamy próchnicowe lub defekty szkliwa na zębach | Tak | |
| Dziecko ma ubytki próchnicowe lub wypełnienia w zębach | Tak | |
| Dziecko ma płytkę bakteryjną na zębach | Tak | |
CRA jest systemem łatwym do zastosowania w praktyce klinicznej, który umożliwia nie tylko oszacowanie ryzyka próchnicy zębów (niskie, średnie lub wysokie), ale także uwidacznia pacjentom i opiekunom przyczyny choroby próchnicowej oraz ułatwia sformułowanie zaleceń lekarskich i wybór właściwych stomatologicznych metod profilaktycznych.
Mechanizm kariostatycznego działania fluoru
Liczne dowody naukowe potwierdzają skuteczność stosowania związków fluoru w zapobieganiu próchnicy zębów oraz w nieinwazyjnym leczeniu początkowych zmian próchnicowych.
Endogenna, doustna podaż optymalnej dawki fluoru podczas rozwoju zawiązków zębów powoduje wzrost zawartości fluoru w powierzchownej warstwie szkliwa, umożliwiając tworzenie stabilnej sieci krystalicznej apatytu. Fluor wpływa na pierwotną mineralizację organicznej matrycy i przederupcyjne dojrzewanie szkliwa. Katalizuje reakcję powstawania hydroksyapatytu Ca10(PO4)6(OH)2. Zastępując jony hydroksylowe (OH-) tworzy fluorohydroksyapatyt Ca5(PO4)3OH1-xFx. Sprzyja tworzeniu większych kryształów apatytów z mniejszą zawartością węglanów. W przederupcyjnym dojrzewaniu szkliwa zębów fluor uczestniczy w usuwaniu wody i białek (25).
Do niedawna uważano, że efektem przederupcyjnego działania fluoru jest mniejsza podatność szkliwa na działanie kwasów. Obecnie wiadomo, że zawartość fluoru w szkliwie nie zmniejsza na stałe w istotny sposób ryzyka rozwoju choroby próchnicowej, natomiast nadmierna podaż może być przyczyną fluorozy zębów (26-28). Zatem ważniejsze jest stałe dostarczanie niewielkich ilości fluoru do środowiska jamy ustnej po wyrznięciu zębów (głównie za pośrednictwem past do zębów z fluorem) przez działanie egzogenne – miejscowe. Losy fluorków dostarczanych do jamy ustnej przedstawia rycina 1.
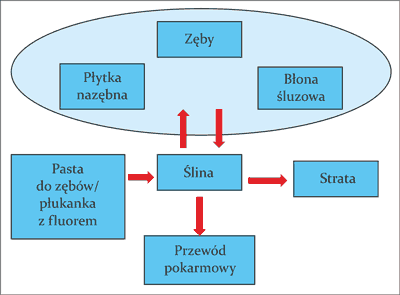
Ryc. 1. Losy fluorków po miejscowej aplikacji; szczególnie ważnym rezerwuarem jonów fluoru jest powierzchnia błony śluzowej jamy ustnej stanowiąca znaczny magazyn uwalnianych powoli fluorków (wg modyfikacji ten Cate) (29, 30)
Przeciwpróchnicowe oddziaływanie fluoru po wyrznięciu zębów polega na:
a) ograniczaniu wpływu bakterii próchnicotwórczych przez:
– zmniejszenie produkcji kwasów,
– zmniejszenie odkładania płytki bakteryjnej na powierzchni zębów,
– hamowanie przemian metabolicznych węglowodanów w komórce bakteryjnej (m.in. poprzez obniżanie aktywności enolazy i upośledzenie transportu glukozy do wnętrza bakterii),
b) hamowaniu demineralizacji i wspomaganiu remineralizacji poprzez:
– stałą obecność niskich stężeń jonów fluorkowych (< 50 ppm) umożliwiającą repozycję związków mineralnych utraconych w czasie powtarzających się ataków kwasów wraz z tworzeniem mniej podatnych kryształów z powłoką fluoroapatytopodobną (tworzenie fluorohydroksyapatytu) (ryc. 2),
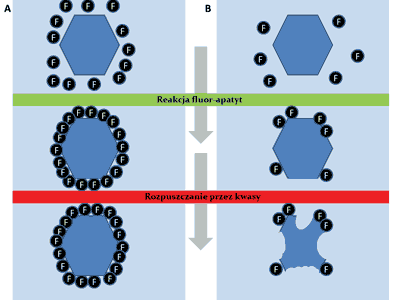
Ryc. 2. Jony fluorkowe adsorbowane są na powierzchni kryształów szkliwa. A – obecność wystarczającej ilości jonów fluorkowych zapobiega rozpuszczaniu kryształów podczas ataku kwasów. B – niewystarczająca ilość jonów fluorkowych na powierzchni kryształu szkliwa – częściowe rozpuszczenie kryształu (wg modyfikacji ten Cate) (29, 33, 34)
– dostarczanie wyższych stężeń jonów fluorkowych (> 100 ppm), które dodatkowo zapewniają tworzenie fluorku wapnia (CaF2) stanowiącego rezerwuar jonów fluorkowych uwalnianych podczas ataku kwasów bakteryjnych na szkliwo zęba (25, 31, 32).
Bezpieczeństwo profilaktyki fluorkowej u dzieci
Stosowanie fluoru, ze względu na jego wysoką cytotoksyczność i małą różnicę między dawką toksyczną i dawką leczniczą, wymaga bardzo rozważnego postępowania. Nieprzestrzeganie zasad profilaktyki fluorkowej jest czynnikiem ryzyka zatruć ostrych i przewlekłych. W swoim raporcie z 1994 roku WHO podkreśla zasadność monitorowania poziomu ekspozycji na fluorki, polegającego na ocenie zrównoważenia przebiegu ciężkości choroby próchnicowej zębów w populacji dzieci z ryzykiem rozwoju fluorozy zębów, wynikającym z kumulacji podaży fluoru pochodzącego z różnych źródeł (3). FDI rekomenduje wypracowanie w danym kraju własnej polityki zdrowotnej i monitorowanie skuteczności działań zapobiegających rozwojowi choroby próchnicowej (1, 2).
Ryzyko wystąpienia fluorozy zębów nie tylko zależy od ekspozycji na fluorki, ale także od wrażliwości poszczególnych osób w danej populacji na fluor. Dlatego objawy łagodnej fluorozy zębów mogą występować także na obszarach, gdzie jego zawartość w wodzie pitnej mieści się w przedziale uważanym za optymalny, tj. 0,5-1,0 mg/l (3).
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
29 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
69 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
129 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 78 zł
Piśmiennictwo
1. FDI Policy Statement Stanowisko PTS: Poprawa zdrowia zębów poprzez fluoryzację. J Stoma 2011; 64(10): 808-809. 2. FDI Policy Statement Stanowisko PTS: Poprawa zdrowia zębów poprzez fluoryzację wody. J Stoma 2011; 64(10): 810-811. 3. Fluorides and Oral Health. Report of a WHO Expert Committee on Oral Health Status and Fluoride Use. WHO Technical Report Series No. 846. Geneva 1994; 37: 1-19. 4. Kaczmarek U, Majewska L, Olczak-Kowalczyk D: Postawa i wiedza stomatologów w zakresie profilaktyki fluorkowej. Nowa Stomatol 2015; 20(1): 23-28. 5. Adamowicz-Klepalska B, Borysewicz-Lewicka M, Dobrzańska A et al.: Aktualny stan wiedzy na temat indywidualnej profilaktyki fluorkowej choroby próchnicowej u dzieci i młodzieży. Niezależny Panel Ekspertów. J Stoma 2013; 66(4): 428-453. 6. Jańczuk Z: Stan narządu żucia polskiej populacji. Pomorska Akademia Medyczna, Szczecin 1990. 7. Szatko F, Boczkowski A: Skuteczność opieki stomatologicznej w Polsce. Fakty, oceny, perspektywy. Instytut Medycyny Pracy, Łódź 1995. 8. Oral health surveys: basic methods. 4th ed. World Health Organization, Geneva 1997. 9. Wierzbicka M, Szatko F, Michalski A et al.: Adaptacja i wdrożenie systemu monitorowania stanu zdrowia jamy ustnej. Ministerstwo Zdrowia, Warszawa 1997. 10. Wierzbicka M, Szatko F, Zawadziński M et al.: Ogólnokrajowy monitoring zdrowia jamy ustnej i jego uwarunkowań. Polska 2002. Ministerstwo Zdrowia, Zakład Stomatologii Zachowawczej AM w Warszawie, Katedra Higieny i Epidemiologii AM w Łodzi 2002. 11. Jodkowska E, Wierzbicka M, Szatko F et al.: Monitoring Zdrowia Jamy Ustnej. Polska 2009. Stan zdrowia jamy ustnej i jego uwarunkowania oraz potrzeby profilaktyczno-lecznicze dzieci i osób dorosłych w wieku 65-74 lata. Warszawa 2009. 12. Wierzbicka M, Szatko F, Strużycka I et al.: Monitoring Zdrowia Jamy Ustnej. Stan zdrowia jamy ustnej i jego uwarunkowania oraz potrzeby profilaktyczno-lecznicze dzieci w wieku 5, 7 i 15 lat. Polska 2010. Warszawa 2011. 13. Małkiewicz E, Wierzbicka M, Szatko F et al.: Monitoring Zdrowia Jamy Ustnej. Stan zdrowia jamy ustnej i jego uwarunkowania oraz potrzeby profilaktyczno-lecznicze dzieci w wieku 6 i 12 lat oraz osób dorosłych w wieku 35-44 lat. Polska 2010. Warszawa 2010. 14. Jodkowska E, Wierzbicka M, Szatko F et al.: Monitoring Zdrowia Jamy Ustnej. Stan zdrowia jamy ustnej dzieci i młodzieży. Polska 2008. Warszawa 2008. 15. FDI: Global goals for oral health in the year 2000. Int Dent J 1982; 32: 74-77. 16. Hobdell M, Petersen PE, Clarkson J, Johnson N: Global goals for oral health 2020. Int Dent J 2003; 53: 285-286. 17. Global caries data for 12-year-old age group WHO Oral Health Country/Area Profile Programme. http://www.mah.se/CAPP/Country-Oral-HealthProfiles/According-to-Alphabetical/Global-DMFTfor-12-year-olds-2011. 18. Wierzbicka M, Szatko F, Radziejewska M et al.: Ogólnokrajowy monitoring zdrowia jamy ustnej i jego uwarunkowań. Polska 2000. Ministerstwo Zdrowia, Zakład Stomatologii Zachowawczej AM w Warszawie, Katedra Higieny i Epidemiologii AM w Łodzi 2000. 19. Jadach R, Siwek-Jadach K, Migas-Mastalerz A: Rola lekarza rodzinnego w prewencji próchnicy zębów u dzieci i młodzieży. Family Medicine and Primary Care Review 2007; 9(3): 442-444. 20. Janus S, Olczak-Kowalczyk D, Wysocka M: Rola lekarzy niestomatologów w zapobieganiu próchnicy wczesnego dzieciństwa. Nowa Pediatria 2011; 1: 6-14. 21. Featherstone JD: The caries balance: The basis for caries management by risk assessment. Oral Health Prev Dent 2004; 2 (suppl. 1): 259-264. 22. Featherstone JD, Adair SM, Anderson MH et al.: Caries management by risk assessment: Consensus statement, April 2002. J Calif Dent Assoc 2003; 31(3): 257-269. 23. Featherstone JDB, Domejean-Orliaguet S, Jenson L et al.: Caries risk assessment in 16 practice for age 6 through adult. J Calif Dent Assoc 2007; 35(10): 703-712. 24. Guideline on Caries-risk Assessment and Management for Infants, Children, and Adolescents. The American Academy of Pediatric Dentistry, 2014; http://www.aapd.org/media/policies_guidelines/g_cariesriskassessment.pdf. 25. Kaczmarek U: Mechanizmy kariostatyczne fluoru. Czas Stomatol 2005; 6: 404-413. 26. Szczepańska J: Wpływ różnych aspektów higieny jamy ustnej na występowanie próchnicy u dzieci w okresie poniemowlęcym. Nowa Stomatol 2003; 1: 4-9. 27. D’Hoore W, Van Nieuwenhuysen JP: Benefits and risks of fluoride supplementation: caries prevention versus dental fluorosis. Eur J Pediatr 1992; 152: 613-617. 28. Dąbrowska E, Balunowska M, Letko E: Zagrożenia wynikające z nadmiernej podaży fluoru. Nowa Stomat 2001; 4(18): 22-27. 29. ten Cate JM: Contemporary perspective on the use of fluoride products in caries prevention. British Dental Journal 2013; 214: 161-167. 30. Duckworth RM, Morgan SN: Oral fluoride retention after use of fluoride dentifrices. Caries Res 1991; 25: 123-129. 31. ten Cate JM, Larsen MJ, Pearce EIF, Fejerskov O: Chemical interactions between the tooth and oral fluids. [In:] Fejerskov O, Kidd EAM (eds.): Dental caries. The disease and its clinical management. Black-well Munksgaard 2003: 49-70. 32. Ogaard B: CaF2 formation: cariostatic properties and factors of enhancing the effect. Caries Res 2001; 35 (suppl. 1): 40-44. 33. Arends J, Christoffersen J: Nature and role of loosely bound fluoride in dental caries. J Dent Res 1990; 69: 601-605. 34. Buzalaf MA, Pessan JP, Honório HM, ten Cate JM: Mechanisms of action of fluoride for caries control. Monogr Oral Sci 2011; 22: 97-114. 35. Borysewicz-Lewicka M, Chłapowska J, Wagner L, Trykowski J: Ocena zawartości fluorków w niektórych krajowych wodach mineralnych. Czas Stom 1999; 52(1): 29-32. 36. Opydo-Szymaczek J: Znaczenie oceny ekspozycji na fluorki w profilaktyce stomatologicznej. Stomat Współ 2003; 5(10): 44-48. 37. Opydo-Szymaczek J: Fluoride Exposure from Diet in Infants and Young Children Fed with the Foodstuffs for Particular Nutritional Uses. Dent Med Probl 2012; 49(2): 209-215. 38. Borysewicz-Lewicka M, Opydo-Szymaczek J, Opydo J: Fluoride ingestion after brushing with a gel containing a high concentration of fluoride. Biol Trace Elem Res 2007; 120(1-3): 114-120. 39. Lis J, Pasieczna A: Atlas geochemiczny Polski. Państwowe Wydawnictwo Kartograficzne, Warszawa 1995. 40. Czarnowski W, Wrześniowska K, Krechniak K: Fluoride in drinking water and human urine in Northern and Central Poland. Sci Total Environ 1996; 191(1-2): 177-184. 41. Erdal S, Buchanan SN: A quantitative look at fluorosis, fluoride exposure, and intake in children using a health risk assessment approach. Environ Health Perspect 2005; 113: 111-117. 42. Bergmann R: Fluorid in der Ernährung des Menschen. Biologische Bedeutung für denwachsenden Organismus. Habilitationsschrift Medical Faculty, Free University Berlin 1994. 43. Guidelines on the use of fluoride in children: an EAPD policy document. Eur Arch Paediatr Dent 2009; 10(3): 129-135. 44. Guideline on Fluoride Therapy. AAPD, 2014, http://www.aapd.org/media/policies_guidelines/g_fluoride therapy.pdf. 45. Policy on Early Childhood Caries (ECC): Classifications, Consequences, and Preventive Strategies. 2014, http://www.aapd.org/media/policies_guidelines/p_eccclassifications.pdf. 46. Weyant RJ, Tracy SL, Anselmo TT et al.: American Dental Association Council on Scientific Affairs Expert Panel on Topical Fluoride Caries Preventive Agents: Topical fluoride for caries prevention: executive summary of the updated clinical recommendations and supporting systematic review. J Am Dent Assoc 2013; 144(11): 1279-1291. 47. Rozier RG, Adair S, Graham F et al.: Evidence-Based Clinical Recommendations on the Prescription of Dietary Fluoride Supplements for Caries Prevention. A report of the American Dental Association Council on Scientific Affairs. JADA 2010; 141(12): 1480-1489. 48. American Dental Association Council on Scientific Affairs. Fluoride toothpaste use for young children. J Am Dent Assoc 2014; 145(2): 190-191. 49. Dietary Reference intakes for Calcium, Phosphorus, Magnesium, Vitamin D, and Fluoride. Standing Committee on the Scientific Evaluation of Dietary Reference Intakes Food and Nutrition Board Institute of Medicine. National Academy Press, Washington, D.C. 1997; 288-313. 50. Opinion of the Scientific Panel on Dietetic Products, Nutrition and Allergies on a request from the Commission related to the Tolerable Upper Intake Level of Fluoride. The EFSA Journal 2005; 192: 1-65. 51. Opydo-Szymaczek J, Opydo J: Salivary fluoride concentrations and fluoride ingestion following application of preparations containing high concentration of fluoride. Biol Trace Elem Res 2010; 137(2): 159-167. 52. Beltran-Aguilar ED, Barker LK, Canto MT et al.: Surveillance for dental caries, dental sealants, tooth retention, edentulism, and enamel fluorosis: United States, 1988-1994 and 1999-2002. MMWR Surveill Summ 2005; 54: 1-43. 53. Iida H, Kumar JV: The association between enamel fluorosis and dental caries in U.S. schoolchildren. JADA 2009; 140: 855-862. 54. European Commision. Directorate-Deneral for Health & Consumers. Scientific Committee on Health and Environmental Risks SCHER: Critical review of any new evidence on the hazard profile, health effects, and human exposure to fluoride and the fluoridating agents of drinking water. SCHER 16.05.2011. 55. Tubert?Jeannin S, Auclair C, Amsallem E et al.: Fluoride supplements (tablets, drops, lozenges or chewing gums) for preventing dental caries in children. Cochrane Database Syst Rev 2011; 7(12): CD007592. doi: 10.1002/14651858.CD007592.pub2. 56. Steinbacher DM, Glick M: The dental patient with asthma. An update and oral health considerations. JADA 2001; 132: 1229-1239. 57. Guide to children’s dental care in medicaid. 2004; http://www.aapd.org/assets/1/7/Periodicity-DentalGuide.pdf. 58. Pitts N, Duckworth RM, Marsh P et al.: Post-brushing rinsing for the control of dental caries: exploration of the available evidence to establish what advice we should give our patients. Br Dent J 2012; 212(7): 315-320. 59. Korporowicz E, Rożniatowski P, Sobiech P, Kochman K: Rodzaj i ilość past do zębów używanych przez rodziców u dzieci w wieku od 1 do 7 lat. Nowa Stomatol 2014; 3: 124-126. 60. Walsh T, Worthington HV, Glenny AM et al.: Fluoride toothpastes of different concentrations for preventing dental caries in children and adolescents. Cochrane Database Syst Rev 2010; 20(1): CD007868. doi: 10.1002/14651858.CD007868.pub2. 61. Wong MCM, Glenny A?M, Tsang BWK et al.: Topical fluoride as a cause of dental fluorosis in children. Cochrane Database Syst Rev 2010 Jan 20; 1: CD007693. doi: 10.1002/14651858.CD007693.pub2. 62. Lewis CL: Fluoride and Dental Caries Prevention in Children. Pediatrics in Review 2014; 35: 3. doi: 10.1542/pir.35-1-3. 63. Al-Mulla A, Karlsson L, Kharsa S et al.: Combination of high-fluoride toothpaste and no post-brushing water rinsing on enamel demineralization using an in situ caries model with orthodontic bands. Acta Odontol Scand 2010; 68(6): 323-328. 64. Nordström A, Birkhed D: Preventive effect of a high-fluoride dentifrice (5,000 ppm) in caries-active adolescents – a 2-year clinical trial. Caries Res 2010; 44: 323-333. 65. Alexander SA, Ripa LW: Effects of self-applied topical fluoride preparations in orthodontic patients. Angle Orthod 2000; 70: 424-430. 66. O’Reilly MM, Featherstone JD: Demineralization and remineralization around orthodontic appliances: an in vivo study. Am J Orthod Dentofacial Orthop 1987; 92: 33-40. 67. Marinho VC, Higgins JP, Logan S, Sheiham A: Fluoride mouthrinses for preventing dental caries in children and adolescents. Cochrane Database Syst Rev 2003; 3: CD002284. 68. Sköld UM, Birkhed D, Borg E, Petersson, LG: Approximal caries development in adolescents with low to moderate caries risk after different 3-year school-based supervised fluoride mouth rinsing programmes. Caries Res 2005; 39: 529-535. 69. Twetman S, Petersson L, Axelsson S et al.: Caries preventive effect of sodium fluoride mouthrinses: a systematic review of controlled clinical trials. Acta Odontol Scand 2004; 62: 223-230. 70. Adair SM: Evidence-based Use of Fluoride in Contemporary Pediatric Dental Practice. Pediatr Dent 2006; 28: 133-142. 71. Zero DT, Fu J, Espeland MA, Featherstone JD: Comparison of fluoride concentrations in unstimulated whole saliva following the use of a fluoride dentifrice and a fluoride rinse. J Dent Res 1988; 67: 1257-1262. 72. Duckworth RM, Horay C, Huntington E, Mehta V: Effects of flossing and rinsing with a fluoridated mouthwash after brushing with a fluoridated toothpaste on salivary fluoride clearance. Caries Res 2009; 43: 387-390. 73. Driscoll WS, Swango PA, Horowitz AM, Kingman A: Caries-preventive effects of daily and weekly fluoride mouthrinsing in a fluoridated community: final results after 30 months. J Am Dent Assoc 1982; 105: 1010-1013. 74. Heifetz SB, Meyers RJ, Kingman A: Comparison of the anticaries effectiveness of daily and weekly rinsing with sodium fluoride solutions: findings after three years. Pediatr Dent 1983; 4: 300-303. 75. Marinho VCC, Higgins J, Logan S, Sheiham A: Fluoride gels for preventing dental caries in children and adolescents. Cochrane Db Syst Rev 2002; 2. DOI: 10.1002/14651858.CDO002280. 76. Marinho VCC, Worthington HV, Walsh T, Chong LY: Fluoride gels for preventing dental caries in children and adolescents. Cochrane Clinical Answers, 2015; http://cochraneclinicalanswers.com/doi/10.1002/cca.876/full. 77. Ekstrand J, Koch G, Petersson LG: Plasma fluoride concentration and urinary fluoride excretion in children following application of the fluoride-containing varnish Duraphat. Caries Res 1980; 14(4): 185-189. 78. Ekstrand J, Koch G, Lindgren LE, Petersson LG: Pharmacokinetics of fluoride gels in children and adults. Caries Res 1981; 15(3): 213-220. 79. Whitford GM: The metabolism and toxicity of fluoride. Monogr Oral Sci 1989; 13: 1-160. 80. Pendrys DG, Haugejorden O, Bårdsen A et al.: The risk of enamel fluorosis and caries among Norwegian children: implications for Norway and the United States. J Am Dent Assoc 2010; 141(4): 401-414. 81. Browne D, Whelton H, O’Mullane D: Fluoride metabolism and fluorosis. J Dent 2005 Mar; 33(3): 177-186. 82. Holve S: An observational study of the association of fluoride varnish applied during well child visits and the prevention of early childhood caries in American Indian children. Matern Child Health J 2008; 12 (suppl. 1): 64-67.


