© Borgis - Postępy Nauk Medycznych 7-8/2007, s. 304-308
*Joanna Kamińska1, Edyta Klimczak-Jajor1, Urszula Bany-Łaszewicz1, Janusz Skierski2,
Ewa Zdebska1, Jerzy Kościelak1
Wpływ inhibitora kinaz Src, SU6656, na komórki linii megakarioblastycznej Meg-01 (pbsz Ph+)
Influence of Src kinases inhibitor, SU6656, on megakaryoblasic cell line Meg-01 (CML Ph+)
1Zakład Biochemii Instytutu Hematologii i Transfuzjologii w Warszawie
Kierownik Zakładu: doc. dr hab. Ewa Zdebska
2Pracownia Cytometrii Przepływowej, Narodowego Instytutu Zdrowia Publicznego
Kierownik Pracowni: dr n. med. Janusz S. Skierski
Streszczenie
Wstęp. Komórki linii megakarioblastycznej Meg-01 (pbsz Ph+) mogą być przydatne jako model do badania procesu megakariocytopoezy. Na powierzchni komórek Meg-01 jest eksponowana glikoproteina GpIIb/IIIa (CD41a), charakterystyczna dla megakariocytów (Mk) i płytek. W syntezie komponenty cukrowej GpIIb/IIIa uczestniczy α1,6-fukozylotransferaza (6FucT). W megakariocytopoezie in vitro aktywność enzymu 6FucT koreluje z ekspresją antygenu CD41a. Wiadomo, że białka z rodziny kinaz tyrozynowych Src hamują różnicowanie Mk. A zatem inhibitor kinaz Src, SU6656, może być użyteczny jako czynnik indukujący różnicowanie Mk. Celem pracy była ocena wpływu SU6656 na komórki linii Meg-01.
Materiał i metody. Komórki linii Meg-01 hodowano w podłożu RPMI 1640 z 10% FBS. SU6656 stosowano w stężeniu końcowym 1 μM oraz 2,5 μM w 0,1% DMSO. W wybranych dniach hodowli oceniano żywotność, gęstość, fenotyp (FACS), morfologię i ploidię (FACS) komórek oraz oznaczano aktywność enzymu 6FucT (metoda izotopowa).
Wyniki. W komórkach linii Meg-01 hodowanych w obecności SU6656 obserwowano hamowanie proliferacji przy równoczesnej indukcji różnicowania komórek. Analiza morfologiczna uwidoczniła pojawianie się w hodowli dużych komórek z wielopłatowym jądrem oraz licznymi ziarnistościami w cytoplazmie. Fenotypowanie komórek potwierdziło zmiany w ekspresji, takich antygenów powierzchniowych Meg-01, jak CD41a, GPA, CD36, CD71. Inhibitor stymulował proces endomitozy. Obserwowane przemiany w komórkach Meg-01, w tym również wzrost aktywności 6FucT, były zależne od stężenia oraz od czasu ekspozycji na działanie SU6656.
Wnioski. Selektywny inhibitor kinaz Src, SU6656, hamuje proliferację komórek linii megakarioblastycznej Meg-01 a jednocześnie indukuje zmiany w morfologii, fenotypie, ploidii oraz aktywności 6FucT świadczące o różnicowaniu i dojrzewaniu komórek.
Summary
Introduction. Megakaryoblastic cell line Meg-01 (CML Ph+) may provide a useful model for the study of megakaryocytopoiesis. Glikoprotein GpIIb/IIIa (CD41a), characteristic for megakaryocytes (Mks) and platelets, appears on the surface on Meg-01 cells. Synthesis of the glycans of the GpIIb/IIIa complex involves α1,6-fucosyltransferase (6FucT). The activity of 6FucT correlates with the expression of antigen CD41a in ex vivo megakaryocytopoiesis. It is a known fact that the Src protein family tyrosine kinases blocks Mks differentiation. Therefore, SU6656, inhibitor of Src kinases may be used as differentiation-inducing agent for Mks. The aim of the study was to analyse the effect of SU6656 on cell line Meg-01.
Material and methods. The cells of Meg-01 line were cultured in RPMI 1640 with 10% FBS. SU6656 was used in final concentration of 1 μM and 2.5 μM in 0.1% DMSO. The cells were monitored for vitality, density, phenotype (FACS), morphology, ploidy (FACS) and activity of 6FucT (isotopic method).
Results. In Meg-01 cells grown in the presence of SU6656 the proliferation was blocked and simultaneously the differentiation of cells was induced. The analysis of morphology showed the presence in culture of large cells with multiplicated of nuclei and greater number of granules in cytoplasm. The changes in the expression of surface antigens Meg-01 cells, such as CD41a, GPA, CD36, CD71 were confirmed by the phenotyping. The inhibitor induced the process of endomitosis. The observed changes in Meg-01 cells, as well the increased the activity of 6FucT, depended on the concentration and time of exposure to SU6656.
Conclusions. SU6656 the selective inhibitor of Src kinases, inhibits the proliferation of megakaryoblasic cell line Meg-01 and simultaneously induces changes in morphology, phenotype, ploidy and the activity of 6FucT which confirm the differentiation and maturation of cells.

Wstęp
Komórki linii megakarioblastycznej Meg-01 mogą być przydatne jako model do badania procesu megakariocytopoezy oraz do analizy biosyntezy białek unikalnych dla linii megakariocytarnych. Komórki linii Meg-01 zostały pozyskane ze szpiku kostnego pacjenta w przełomie blastycznym przewlekłej białaczki szpikowej (pbsz) Ph+ (chromosom Filadelfia). Na powierzchni megakarioblastów Meg-01 jest obecna glikoproteina GpIIb/IIIa (CD41a), charakterystyczna dla megakariocytów (Mk) i płytek (1). Wiadomo, że antygen CD41a jest wczesnym markerem progenitorów Mk (2). W syntezie komponenty cukrowej glikoproteiny GpIIb/IIIa uczestniczy α1,6-fukozylotransferaza (6FucT) (3). Obserwowana korelacja aktywności 6FucT z ekspresją antygenu CD41a+ w procesie megakariocytopoezy in vitro sugeruje, że aktywność tego enzymu może stanowić wskaźnik różnicowania i dojrzewania komórek CD34+ w kierunku Mk (4). W procesie megakariocytopoezy kluczową rolę w morfologii, proliferacji, ruchliwości oraz przeżyciu komórki pełnią białka z rodziny kinaz tyrozynowych Src (5). Potwierdzono obecność sześciu kinaz Src w Mk, przy czym dwie z nich: Fyn i Lyn, wyróżniały się wysokim poziomem ekspresji. Obie kinazy były aktywowane w Mk w obecności trombopoetyny (TPO), co wskazywało na istotną rolę Fyn i Lyn w procesie megakariocytopoezy (6). Wiadomo, że kinazy Src hamują różnicowanie Mk (7). Lannutti i wsp. wykazali efekt inhibitora kinaz Src, SU6656, na indukowane TPO dojrzewanie Mk (8). W obecności SU6656 obserwowano zahamowanie podziałów komórek linii megakariocytarnej UT-7/TPO, przy jednoczesnej kontynuacji akumulacji DNA w procesie endomitozy. Inhibitor stymulował także wzrost ekspresji antygenu CD41(GpIIb) oraz CD61(GpIIIa). Podobny efekt na poliploidyzację i różnicowanie Mk był obserwowany w czasie ekspansji pierwotnych Mk, w komórkach szpiku kostnego pacjentów z zespołami mielodysplastycznymi oraz innych liniach komórkowych K562 i HEL, posiadających potencjał Mk. A zatem SU6656 jest użyteczny, nie tylko, jako czynnik indukujący różnicowanie Mk, ale również może być stosowany w badaniach prowadzących do zrozumienia molekularnych podstaw endomitozy Mk (8).
Celem pracy była ocena wpływu SU6656 na komórki linii Meg-01. W wybranych dniach hodowli komórki poddawano analizie morfologicznej, fenotypowej, ploidii a także oznaczano aktywność 6FucT.
Materiał i metody
Warunki hodowli linii komórkowej Meg-01
Meg-01 jest megakarioblastyczną linią komórkową (ATCC) wyprowadzoną, w 1983 roku przez M. Ogura i wsp. (1) w Nagoya University School of Medicine, Nagoya, Japan, ze szpiku kostnego pacjenta w kryzie blastycznej przewlekłej białaczki szpikowej Ph+. Komórki Meg-01 hodowano w gęstości 2,5 x 105 komórek/ml, w podłożu RPMI 1640 zawierającym glutamax (Gibco), 10% FBS (Gibco) i antybiotyk (SIGMA). Hodowle prowadzono w butelkach hodowlanych 25 cm2 w inkubatorze CO2 w 37°C, 5%CO2 i 95% wilgotności. W wybranych dniach hodowli oceniano żywotność, gęstość, fenotyp, morfologię i ploidię komórek oraz oznaczano aktywność enzymu 6FucT. SU6656 (CalBiochem), inhibitor kinaz Src, rozpuszczano w DMSO i dodawano do podłoża w końcowym stężeniu 1 μM oraz 2,5 μM w 0,1% DMSO.
Analiza fenotypu komórek
Oceny fenotypowej komórek dokonywano metodą FACS (w cytometrze FACSCalibur, BD Biosciences) z użyciem przeciwciał anty: CD3-FITC, CD14-PE, CD15-PE, CD19-PE, CD36-FITC, CD41a-FITC, CD42b-PE, CD71-PE, GPA-PE (glikoforyna A-PE) z zastosowaniem odpowiednich kontroli izotypowych (BD Pharmingen).
Analiza ploidii komórek
Ploidię komórek oceniano pomiarem zawartości DNA metodą FACS (w cytometrze przepływowym Becton Dicinson; Vantage) z użyciem przeciwciał anty-CD41a-FITC (BD Pharmingen) oraz DAPI (Molecular Probe), stosując odpowiednią kontrolę izotypową (BD Pharmingen).
Oznaczanie aktywności 6FucT w komórkach
Aktywność enzymu 6FucT oznaczano w komórkach, poddanych solubilizacji, metodą izotopową. Preparat enzymu inkubowano z substratami GDP [14C] fukozą (Amersham) i asialoagalaktotransferyną glikopeptydem, a następnie produkt reakcji izolowano metodą chromatograficzną i analizowano przy użyciu licznika scyntylacyjnego (9).
Analiza morfologii komórek
Morfologię komórek Meg-01 analizowano w mikroskopie świetlnym po uprzednim barwieniu komórek metodą May-Grünwalda Giemsy.
Wyniki
Komórki linii Meg-01, wczesne formy megakarioblastów, hodowano w podłożu RPMI z 10% FBS w obecności 1,0 μM i 2,5 μM selektywnego inhibitora kinaz Src, SU6656. W wybranych dniach hodowli analizowano żywotność, gęstość, morfologię, fenotyp, ploidię komórek oraz oznaczano aktywność enzymu 6FucT. Inhibitor, w sposób zależny od stężenia, hamował proliferację komórek Meg-01 w hodowli (ryc. 1).
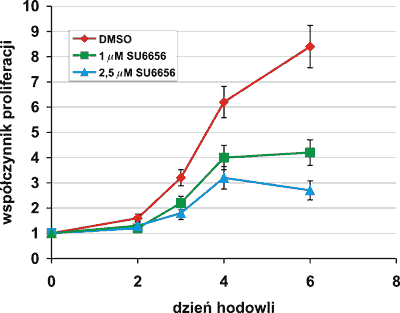
Ryc. 1. Hamowanie proliferacji komórek Meg-01 hodowanych w obecności inhibitora kinaz Src, SU6656. Warunki hodowli opisane są w części Materiały i metody. Przedstawione wyniki są wartościami średnimi z trzech niezależnych eksperymentów ± odchylenie standardowe.
Ocena morfologiczna komórek uwidoczniła różnicowanie i dojrzewanie komórek Meg-01 w obecności SU6656 (ryc. 2). W preparatach obserwowano duże komórki, których średnica osiągała nawet 60 μm (12 μm – 60 μm), z wielopłatowym jądrem wskazującym na indukcję podziałów endomitotycznych. Średnica komórek w hodowli kontrolnej z DMSO wynosiła od 12 μm do 20 μm. Komórki pod wpływem inhibitora zwiększały swoją średnicę nawet pięciokrotnie. W cytoplazmie obserwowano pojawianie się licznych ziarnistości.
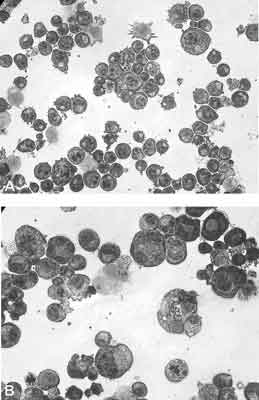
Ryc. 2. Ocena morfologiczna komórek Meg-01 hodowanych 4 dni w podłożu RPMI zawierającym 10% FBS w obecności: (A) 0,1% DMSO; (B) 2,5 μM SU6656 w 0,1% DMSO (powiększenie 400x). Komórki barwiono metodą May-Grünwalda Giemsy.
W trakcie hodowli Meg-01 badano ekspresję antygenów powierzchniowych linii megakariocytarnej (CD41a, CD42b) oraz antygenów innych linii hematopoetycznych: linii erytroidalnej (GPA, CD36), limfoidalnej (CD3, CD19), mieloidalnej (CD14, CD15) (tab. 1). W obecności inhibitora kinaz Src obserwowano zmiany w fenotypie komórek Meg-01. Wyraźny wzrost odsetka komórek CD41a+ przy jednoczesnym spadku odsetka komórek GPA+, CD36+ oraz brak obecności antygenów limfoidalnych CD3 i CD19 oraz mieloidalnych CD14 i CD15 na powierzchni komórek świadczył o różnicowaniu komórek w kierunku Mk. Antygen CD42b (GpIb), marker dojrzalszych form Mk, nie był obecny na powierzchni komórek Meg-01 w hodowli z SU6656. Wcześniejsza charakterystyka Meg-01 potwierdziła, że glikoproteina GpIb jest obecna tylko w cytoplazmie większych komórek Meg-01 oraz, że komórki te nie posiadają markerów zarówno limfocytów B i T, jak i komórek mieloidalnych (1). Obecność antygenu CD71, receptora dla transferyny, jest charakterystyczna dla dzielących się komórek. W związku z tym obserwowany spadek odsetka komórek CD71+ świadczy o hamowaniu proliferacji komórek Meg-01 przez SU6656 (tab. 1). Mk są unikalnymi komórkami hematopoetycznymi ze względu na poliploidalność jądra komórkowego, które powstaje w wyniku procesu endomitozy. Wcześniejsze badanie kariotypu komórek Meg-01 ujawniło, że posiadają one hyperdiploidalny kariotyp ze średnią liczbą chromosomów 56-58 (od 50 do 113) (1). Analiza ploidii komórek Meg-01 hodowanych w obecności SU6656 potwierdziła wpływ inhibitora na stymulację procesu endomitozy (ryc. 3). Obserwowany na histogramach wzrost odsetka komórek Meg-01 o fenotypie CD41a+ charakteryzujących się podwyższoną ploidią zależał od stężenia SU6656 w hodowli.
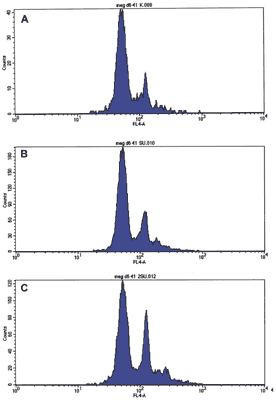
Ryc. 3. Analiza ploidii komórek Meg-01 o fenotypie CD41a+ hodowanych w obecności inhibitora SU6656. Hodowlę prowadzono w podłożu RPMI uzupełnionym 10% FBS w obecności: (A) 0,1% DMSO; (B) 1,0 μM SU6656 w 0,1% DMSO;(C) 2,5 μM SU6656 w 0,1% DMSO. Ploidię komórek oceniano pomiarem zawartości DNA metodą FACS z użyciem przeciwciał anty-CD41a-FITC oraz DAPI, stosując odpowiednią kontrolę izotypową. Warunki przeprowadzonego doświadczenia opisano w części Materiały i metody. Wyniki są reprezentatywne dla trzech niezależnych doświadczeń.
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
24 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
59 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
119 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 28 zł
Piśmiennictwo
1. Ogura M., et al.: Establishment of a novel human megakaryoblastic leukemia cell line, MEG-01, with positive Philadelphia chromosome. Blood 1985; 66: 1384-1392.
2. Long M.: Megakaryocyte differentiation events. Semin. Hematol., 1998; 35: 192-199.
3. Tsuji T., Osawa T.: Structures of the carbohydrate chains of membrane glycoproteins IIb and IIIa of human platelets. J. Biochem., 1986; 100: 1387-1389.
4. Bany-Łaszewicz U, et al.: The activity of α1,6-fucosyltransferase during human megakaryocytic differentiation. Cell Mol. Biol. Lett., 2004; 9: 145-152.
5. Roskowski Jr R.: Src kinase regulation by phosphorylation and dephosphorylation. Biochem. Biophys. Res. Commun., 2005; 331: 1-14.
6. Lannutti B.J, et al.: Identification and activation of Src family kinases in primary megakaryocytes. Exp. Hematol., 2003; 31: 1268-1274.
7. Lannutti B.J., Drachman J.G.: Lyn tyrosine kinase regulates thrombopoietin-induced proliferation of hematopoietic cell lines and primary megakaryocytic progenitors. Blood 2003; 103: 3736-3743.
8. Lannutti B.J, et al.: Induction of polyploidization in leukemic cell lines and primary bone marrow by Src kinase inhibitor SU6656. Blood 2005; 105: 3875-3878.
9. Kamińska J, et al.: Purification and characterisation of GDP-L-Fuc: N-acetyl β-D-glucosaminide α1→6fucosyltransferase from human blood platelets. Glycoconjugate J. 1998; 15: 783-788.
10. Cortes J, et al.: Dasatinib induces complete hematologic and cytogenetic responses in patients with imatinib-resistant or intolerant chronic myeloid leukemia in blast crisis. Blood 2007; 109: 3207-3213.
11. Blake R.A, et al.: SU6656, a selective Src family kinase inhibitor, used to probe growth factor signaling. Mol. Cell. Biol., 2000; 20: 9018-9027.
12. Wilson M.B, et al.: Selective pyrrolo-pyrimidine inhibitors reveal a necessary role for Src. family kinases in Bcr-Abl signal transduction and oncogenesis. Oncogene 2002; 21: 8075-8088.
13. Kościelak J, et al.: Activity of platelet alpha-6-fucosyltransferase is inversely related to blood platelet concentration. Acta Biochimica Polonica 1995; 42: 35-40.



