© Borgis - Postępy Nauk Medycznych 2/2015, s. 82-87
*Krzysztof Pyra1, Sławomir Woźniak2, Piotr Czuczwar2, Anna Drelich-Zbroja1, Tomasz Roman1, Łukasz Światłowski1, Tomasz Paszkowski1, Tomasz Jargiełło1
Ocena skuteczności wewnątrznaczyniowej embolizacji żył jajnikowych w leczeniu zespołu przekrwienia biernego miednicy
Assessment of efficacy of intravascular ovarian vein occlusion for the treatment of pelvic congestion syndrome
1Department of Interventional Radiology and Neuroradiology, Medical University, Lublin
Head of Department: prof. Małgorzata Szczerbo-Trojanowska, MD, PhD
2Third Gynecology Department, Medical University, Lublin
Head of Department: prof. Tomasz Paszkowski, MD, PhD
Streszczenie
Wstęp. Przewlekły ból miednicy (CPP) jest przyczyną 20% ginekologicznych wizyt ambulatoryjnych. Częstym powodem CPP jest zespół przekrwienia biernego narządów miednicy mniejszej (PCS). Jest on powodowany przez żylaki przymacicza i niewydolne żyły jajnikowe. Zmiany tego typu mogą rozwijać się u około 10-15% kobiet, głównie w wieku poniżej 45 lat.
Cel pracy. Celem pracy jest ocena skuteczności i wyników wewnątrznaczyniowej embolizacji żył jajnikowych w leczeniu zespołu przekrwienia biernego miednicy mniejszej.
Materiał i metody. W prospektywnym badaniu obserwacyjnym przeprowadzonym w okresie od stycznia do września 2014 roku u 35 pacjentek została zaplanowana embolizacja żył jajnikowych. U wszystkich występował chroniczny ból miednicy przynajmniej od roku. Ból został oceniany za pomocą skali wzrokowej VAS (0 – brak bólu, 10 – ból nie do zniesienia). U zakwalifikowanych pacjentek podczas flebografii oceniano zakres wstecznego napływu do żył jajnikowych. Flebografię przeprowadzano podczas próby Valsalvy z cewnika umieszczonego w lewej żyle nerkowej, a po prawej stronie – z ujścia żył jajnikowych. Żyły jajnikowe zamykano za pomocą spiral 0,035 i 0,018 lub zamykaczem naczyniowym EOS. W przypadku bogatej siatki żylnej dodatkowym materiałem obliterującym był aethoxysklerol.
Wyniki. Zabieg skutecznie wykonano u 34 z 35 pacjentek. W jednym przypadku nie udało się selektywnie zacewnikować żył jajnikowych. W 27 przypadkach zastosowano spirale, a w 7 zamykacz naczyniowy EOS. W 9 przypadkach dodatkowo zastosowano aethoxysklerol. Za techniczny sukces uznawano bezpieczne zamknięcie żył/żyły i brak napływu środka cieniującego do żył jajnikowych podczas próby Valsalvy. Skuteczność techniczna została oceniona na 97%. W 4 przypadkach embolizacja okazała się nieskuteczna. Skuteczność kliniczną zabiegu oceniano w oparciu o skalę VAS. W 97% ból znacznie zmniejszył się, a w 3% przypadkach ustąpił całkowicie.
Wnioski. Zabieg wewnątrznaczyniowej embolizacji żył jajnikowych wydaje się bezpieczną i skuteczną metodą w leczeniu PCS. Przemawia za tym wysoki wskaźnik skuteczności zarówno technicznej, jak i klinicznej. Jednakże wymagane są dalsze badania tej metody leczenia. Konieczna jest ścisła współpraca ginekologa z radiologiem zabiegowym przy kwalifikacji chorej do zabiegu.
Summary
Introduction. Chronic pelvic pain (CPP) is responsible for 20% of gynaecological outpatient visists. Pelvic congestion syndrome (PCS) is a common cause of CPP, which is underlain by the varicose and incompetent veins within the pelvis minor. According to estimates, such changes can develop in about 10-15% of women, predominantly under the age of 45 years.
Aim. Assessment of efficacy of intravascular occlusion of ovarian veins for the treatment of pelvic congestion syndrome.
Material and methods. In the prospective observational study carried out between January and September of 2014, 35 patients were scheduled for ovarian vein embolisation. Each patient experienced pelvic pain for at least one year – the visual analogue score (VAS) (0 – no pain, 10 – the most severe pain). The qualified patients were referred to phlebography to assess the extent of retrograde inflow to ovarian veins and occlusion of the appropriate ovarian veins. Phlebographies were carried out during the Valsalva manoeuvre from the catheter placed in the left renal vein; on the right side – at the ovarian vein ostium. Ovarian veins were occluded using detachable coils 0.035, 0.018 or a vascular occluder EOS. in cases of numerous collaterals, the obliterating material was additionally used, i.e. aethoxysclerol foam.
Results. The procedures were performed in 34 out of 35 patients. In one cases, none of the ovarian veins was successfully selectively catheterised. In 7 patients embolisations were performed using a vascular occluder EOS, in the remaining 27 using coils. In 9 cases additionally were used aethoxysclerol. A technical success was considered safe closure of veins/vein and lack of contrast medium inflow in follow-up phlebography using the Valsalva manoeuvre. The technical efficacy was found to be 97%. In 4 cases embolisation was ineffective. The clinical efficacy of the procedure was assessed using VAS and was considered as the pain score 2 or less. It was found to be 97% including 3 cases in which the pain subsided completely.
Conclusions. PCS embolisation seems to be an effective and safe treatment measure characterised by a high rate of clinical and technical success. However, further research is required on this method. In addition, an essential element is a good cooperation of gynaecologists and interventional radiologists in qualification of the patient for the treatment.

INTRODUCTION
Chronic pelvic pain (CPP) remains a diagnostic and therapeutic challenge. CPP can occur in 1/3 of women and be responsible for 20% of gynaecological outpatient visists (1). The diagnostic procedures and treatment of this syndrome account for 35% of diagnostic laparoscopies and 15% of hysterectomies (2). Apart from pelvic varices, the causes of CPP are likely to include pelvic inflammatory diseases, endometriosis, structural uterine tube abnormalities and many others. Before establishing the diagnosis of pelvic congestion syndrome (PCS), it is essential to eliminate all the remaining possible diseases.
Pelvic congestion syndrome (PCS) is a common cause of CPP, which is underlain by the varicose and incompetent veins within the pelvis minor. According to estimates, such changes can develop in about 10-15% of women, predominantly under the age of 45 years. However, not all the women of this group report symptoms of CPP (3).
Pathophysiology
The aetiology of PCS has not been fully known. The first theory regarding pain due to dilated venous vessels and slowed down flow in pelvic vessels was put forward by Taylor in 1949. One of the PCS factors is likely to be incompetence or lack of the valvular apparatus in the ovarian and parametrial veins. The anatomical defect of vessels results in retrograde flow in the ovarian veins, which causes visible dilatations of veins and varices. The lack of valves at the ostium of ovarian veins can be found in about 15% of women whereas incompetent valves are diagnosed in 40% of cases on the left side and in 35% on the right side. The development of painis affected not only by physical blood volume and retrograde pressure but also by the resultant venous ischaemia. This impairs trophism of the epithelial and smooth muscle cells, which react by secreting substance P and neurokinin A and B. The predisposing factors include multiparity, family history of CPP or genital prolapse (4).
Clinical symptoms
In the majority of women, PCS manifests with non-cyclic abdominal or pelvic pain occurring for at least half a year. PCS is characterized by chronic, dull and continuous pain (can last for many hours or days). The symptoms usually intensify after prolonged time in the standing position, during menstruation, after sexual intercourses and during pregnancy. The non-specific symptoms include headaches, flatulence, nausea, general fatigue and low mood. Some patients with the diagnosis of PCS report only slight episodes of pain within the abdomen or lack of them and complain of hip pain or perineal and lower limb varices (5).
Diagnosis
In order to find a characteristic syndrome of clinical symptoms, imaging examinations are required to differentiate the causes of their occurrence. The examinations in question can be divided into non-invasive – ultrasound, magnetic resonance and those of low invasiveness – CT or dynamic tests, i.e. phlebography, thanks to which the function of valves and competence of the venous system can be assessed. The transvaginal pelvic ultrasound examination combined with Doppler imaging is preferable. The examination enables to visualize pelvic venous plexuses with dynamic evaluation of blood flow. Veins ofunaffected plexuses are < 4 mm in diameter (6). Most patients with the clinical suspicion of PCS have dilated veins > 4/6 mm, slowed down or reverse blood flow (particularly during the Valsalva manoeuvre), dilated arcuate veins running through the uterine muscle continuous with the varices on the opposite side. Moreover, the ovarian vein can be dilated > 8 mm. Interestingly, in over 50% of cases polycystic ovaries are observed (7). The development of ovarian cysts is unclear, although the theories of excessive estrogen stimulation in women with PCS are repeatedly suggested (4).
For the majority of interventional radiologists treating PCS, MRI is the best imaging method. The examination is non-invasive, patients are not exposed to radiation, no contrast media are used, yet the method is extremely accurate. MRI enables to asses ovarian vein ostia, which helps during the procedure, and local anatomy, which facilitates the differential diagnosis of CPP. Our experiences show that it is optimal to perform MRI in the afternoon or evening hours. After the day activity, congestion is much better visible. The intravascular examination – phlebography – allows assessing functionally retrograde blood reflux to the affected plexuses and is a gold standard of management (8). The painless examination and procedure are carried out under local anaesthesia by puncturing the right common femoral vein and introducing the 5 Fr guiding catheter. Phlebography is performed during the Valsalva manoeuver from the catheter left in the left renal vein; in the case of the right side, in the ovarian vein ostium.
The diagnosis of PCS is confirmed by the following phlebography results: ovarian vein diameter > 6, retrograde free inflow to the ovarian vein or/and parametrial plexuses, presence of several tortuous vessels of the collateral circulation and delayed outflow or contrast medium retention after the injection has been completed. Free retrograde inflow to ovarian veins and parametrial plexuses evidences incompetence of the valvular apparatus. Diagnostic phlebography immediately visualizes the dynamics of venous low and can be performed in various positions. After completing the diagnostic part, the radiologist can smoothly initiate the occlusion of varicose veins (fig. 1). However, the radiologic examination should be finally assessed with reference to the clinical presentation.
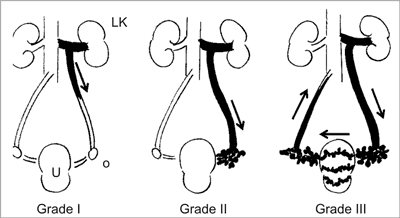
Fig. 1. Three grades of reflux are distinguished.
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
29 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
69 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
129 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 78 zł
Piśmiennictwo
1. Phillips D, Deipolyi AR, Hesketh RL et al.: Pelvic congestion syndrome: etiology of pain, diagnosis, and clinical management. J Vasc Interv Radiol 2014 May; 25(5): 725-733.
2. Association of Professors of Gynecology and Obstetrics (APGO). APGO Educational Series on Women’s Health Issues. Chronic Pelvic Pain: An Integrated Approach. APGO DC: Washington 2000.
3. Liddle AD, Davies AH: Pelvic congestion syndrome: chronic pelvic pain caused by ovarian and internal iliac varices. Phlebology 2007; 22(3): 100-104.
4. Siskins GP (ed.): Interventional radiology in women’s health. Thieme Medical Publishers, New York 2009; 90-105.
5. Jung SC, Lee W, Chung JW et al.: Unusual causes of varicose veins in the lower extremities: CT venographic and Doppler US findings. Radiographics 2009 Mar-Apr; 29(2): 525-536.
6. Park SJ, Lim JW, Ko YT et al.: Diagnosis of pelvic congestion syndrome using transabdominal and transvaginal sonography. AJR Am J Roentgenol 2004 Mar; 182(3): 683-688.
7. Coakley FV, Varghese SL, Hricak H: CT and MRI of pelvic varices in women. J Comput Assist Tomogr 1999 May-Jun; 23(3): 429-434.
8. Yang DM, Kim HC, Nam DH et al.: Time-resolved MR angiography for detecting and grading ovarian venous reflux: comparison with conventional venography. Br J Radiol 2012 Jun; 85(1014): e117-122.
9. Farquhar CM, Rogers V, Franks S et al.: A randomized controlled trial of medroxyprogesterone acetate and psychotherapy for the treatment of pelvic congestion. Br J Obstet Gynaecol 1989 Oct; 96(10): 1153-1162.
10. Laborda A, Medrano J, de Blas I et al.: Endovascular treatment of pelvic congestion syndrome: visual analog scale (VAS) long-term follow-up clinical evaluation in 202 patients. Cardiovasc Intervent Radiol 2013 Aug; 36(4): 1006-1014. doi: 10.1007/s00270-013-0586-2. Epub 2013 Mar 2.
11. Ball E, Khan KS, Meads C: Does pelvic venous congestion syndrome exist and can it be treated? Acta Obstet Gynecol Scand 2012 May; 91(5): 525-528. doi: 10.1111/j.1600-0412.2012.01368.x.
12. Rozenblit AM, Ricci ZJ, Tuvia J, Amis ES Jr: Incompetent and dilated ovarian veins: a common CT finding in asymptomatic parous women. AJR Am J Roentgenol 2001 Jan; 176(1): 119-122.
13. Nascimento AB, Mitchell DG, Holland G: Ovarian veins: magnetic resonance imaging findings in an asymptomatic population. J Magn Reson Imaging 2002 May; 15(5): 551-556.
14. Belenky A, Bartal G, Atar E et al.: Ovarian varices in healthy female kidney donors: incidence, morbidity, and clinical outcome. AJR Am J Roentgenol 2002 Sep; 179(3): 625-627.

