© Borgis - Medycyna Rodzinna 3/2016, s. 146-151
Grzegorz K. Jakubiak
Leki hipoglikemizujące z grupy gliflozyn i ich zastosowanie w farmakoterapii cukrzycy
Antidiabetic drugs from group of gliflozins and their role in pharmacotherapy of diabetes
Wydział Lekarski z Oddziałem Lekarsko-Dentystycznym w Zabrzu, Śląski Uniwersytet Medyczny w Katowicach
Summary
Diabetes is a frequent disease and is characterized by chronic hyperglycemia. Diabetes is a cause of severe complications (neuropathy, angiopathy). Canagliflozin and dapagliflozin are representatives of selective and competitive SGLT2 inhibitors – the latest class of oral antidiabetic drugs. Sodium glucose linked transporter type 2 as target for gliflozins is located in a proximal renal tubule. These medicaments reduce reabsorption of glucose from primary urine, increase glucose concentration in urine and decrease glucose concentration in plasma. SGLT2 is responsible for 90% of renal glucose reabsorption. SGLT2 inhibitors improve glycemic control in people with type 2 diabetes. Gliflozins have a positive influence on loss of weight and reduction of blood pressure. Because of enhancement of glycosuria SGLT2 inhibitors increase risk of genital and urine infection in people with diabetes and risk of dehydration. SGLT2 inhibitors in monotherapy don’t increase risk of hypoglycemia. Dapagliflozin was the first agent in the group in the world. Dapagliflozin and canagliflozin are agents from the group, which are available in routine clinical practice in Poland. Other substances are in clinical trials.

Wstęp
Cukrzyca jest chorobą, której rozpowszechnienie na świecie ocenia się na 9,2% wśród kobiet powyżej 25. roku życia i 9,8% wśród mężczyzn w tym samym wieku (1). Szacuje się, że do roku 2030 liczba chorych na cukrzycę na całym świecie przekroczy 552 miliony. Pacjenci cierpiący na cukrzycę typu 2 stanowią 95% wszystkich osób z rozpoznaną cukrzycą (2). Cukrzyca cechuje się przewlekłą hiperglikemią, która prowadzi do powikłań neuropatycznych, mikroangiopatycznych (obejmujących nefropatię i retinopatię cukrzycową) oraz makroangiopatycznych, polegających na przyspieszeniu rozwoju zmian miażdżycowych tętnic ze wszystkimi tego konsekwencjami klinicznymi (choroba niedokrwienna serca, zawał serca, przewlekłe niedokrwienie kończyn dolnych, zwężenie tętnic szyjnych i kręgowych, przemijające napady niedokrwienne TIA, udary niedokrwienne mózgu i in.). Powikłania cukrzycy są przyczyną obniżenia długości i jakości życia. Skutkują również rosnącymi kosztami dla systemów opieki zdrowotnej państw i zmniejszeniem zdolności do pracy. W 2011 roku wydatki systemów opieki zdrowotnej związane z cukrzycą wyniosły globalnie 465 miliardów dolarów, co stanowiło 11% całkowitych wydatków na opiekę zdrowotną (2). Stąd poszukiwanie coraz skuteczniejszych metod kontrolowania glikemii u pacjentów z cukrzycą ma duże znaczenie.
Gliflozyny to nowa grupa leków przeciwcukrzycowych, których mechanizm działania polega na selektywnej, odwracalnej, kompetycyjnej inhibicji transportera SGLT2 (3). Białko SGLT2 jest kotransporterem sodowo-glukozowym, znajdującym się w początkowym odcinku cewki nerkowej bliższej (segment S1) na powierzchni luminalnej komórek nabłonkowych, który odpowiada za zwrotną reabsorpcję glukozy z moczu pierwotnego do krwi (4-6). U osoby zdrowej glukoza w moczu ostatecznym jest nieobecna, ponieważ cała glukoza przesączona w kłębuszkach nerkowych zostaje zwrotnie zreabsorbowana – głównym efektorem tego zjawiska jest właśnie białko SGLT2 (4). Za reabsorpcję glukozy w 10% odpowiada również SGLT1, znajdujący się w końcowym odcinku (segment S3) cewki nerkowej bliższej (6). Co do ekspresji receptorów SGLT1 i SGLT2 w błonie luminalnej komórek nabłonkowych cewki proksymalnej w segmencie S2 są rozbieżności w cytowanych pracach: niektórzy autorzy nie wspominają o segmencie S2 (7), niektórzy określają lokalizację SGLT1 jako segmenty S2/S3 (8), a niektórzy określają lokalizację transportera SGLT2 jako segmenty S1/S2 (5, 6). Białko SGLT1 występuje w większej ilości na powierzchni komórek nabłonkowych jelita cienkiego, w sercu oraz w tchawicy (1, 3, 7). Glukoza staje się obecna w moczu ostatecznym, gdy stężenie glukozy we krwi jest wyższe od wartości zwanej progiem nerkowym dla glukozy, której wartość wynosi 180-200 mg/dl u osób zdrowych, natomiast u pacjentów z cukrzycą typu 2 może być nawet wyższa na skutek zwiększonej ekspresji białka SGLT2, co dodatkowo predysponuje do wyższych wartości glikemii (3, 6).
Ciekawostką wartą wspomnienia jest, iż mutacja genu SLC5A2, który koduje białko SGLT2, skutkująca dysfunkcją tego transportera odpowiada za stan zwany rodzinną glikozurią nerkową. Objawia się on jedynie glikozurią, której nie towarzyszy hiperglikemia, poza nielicznymi przypadkami zwiększonej podatności na zakażenia układu moczowo-płciowego, poliurii czy też zwiększonej aktywności układu renina-angiotensyna-aldosteron (9).
Przedstawiciele grupy gliflozyn
Amerykańska Agencja ds. Żywności i Leków (FDA) dopuściła do użytku klinicznego kanagliflozynę w marcu 2013 roku, dapagliflozynę w styczniu 2014 roku, zaś empagliflozynę w sierpniu 2014 roku. Natomiast w Europie dapagliflozyna stała się dostępna już w 2012 roku, co uczyniło ją pierwszym na świecie inhibitorem SGLT2 stosowanym w rutynowej praktyce klinicznej (1). Trwają również badania nad kolejnymi lekami z tej grupy, takimi jak: ipragliflozyna, luseogliflozyna, tofogliflozyna, ertugliflozyna (10). W Polsce są dostępne kanagliflozyna oraz dapagliflozyna, przy czym dapagliflozyna zarówno w postaci preparatu prostego, jak i preparatu złożonego z metforminą.
Rys historyczny
Pierwszą substancją o podobnych właściwościach, na którą zwrócono uwagę, była floryzyna – substancja otrzymana z jabłoni w 1835 roku. Testowano ją na zwierzętach jako lek przeciwmalaryczny, przeciwgorączkowy i przeciwko infekcjom. Zaobserwowano, że przewlekłe podawanie floryzyny powodowało polidypsję, poliurię oraz glikozurię, której towarzyszyła normoglikemia. Zainteresowanie floryzyną zmniejszyło się na skutek jej niekorzystnych właściwości farmakokinetycznych oraz działań niepożądanych, wynikających z zablokowania transportera SGLT1 – upośledzenie wchłaniania węglowodanów w jelitach, biegunka, odwodnienie (7). W 1987 roku Rossetti i wsp. opublikowali dane, z których wynikało, że hiperglikemia rozwijająca się po częściowej pankreatektomii u zwierzęcia laboratoryjnego może być zmniejszona przez podskórne wstrzykiwanie floryzyny. To odkrycie zwróciło uwagę na możliwość poszukiwania nowej drogi farmakoterapii cukrzycy (11). W 1999 roku grupa badaczy z Japonii (Oku i wsp.) opisała substancję nazwaną T-1095, która po zmetabolizowaniu do T-1095A wykazywała działanie hipoglikemizujące poprzez hamowanie nerkowej reabsorpcji glukozy. T-1095 był syntetyczną pochodną floryzyny (12). W 2000 roku opublikowano wyniki badań wpływu T-1095 na wartości glikemii u szczurów z cukrzycą wyindukowaną za pomocą antybiotyku o właściwościach cytostatycznych – streptozotocyny. Z wyników tych badań wynikało, że T-1095 zwiększa wrażliwość komórek mięśni szkieletowych na działanie insuliny i poprawia kontrolę glikemii (13). W 2010 roku inna grupa badaczy japońskich opisała odkrycie substancji bardziej stabilnej metabolicznie oraz wiążącej się silniej i bardziej selektywnie z transporterem SGLT2 niż T-1095 – kanagliflozynę. Modyfikacja chemiczna prowadząca do otrzymania kanagliflozyny polegała m.in. na dodaniu pierścienia tiofenowego (14). Na rycinie 1 przedstawiono strukturę chemiczną kanagliflozyny.
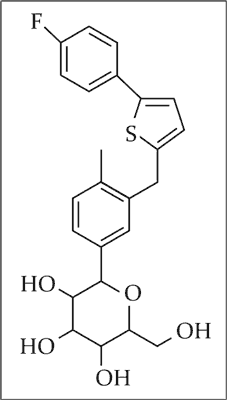
Ryc. 1. Struktura chemiczna kanagliflozyny
Dawkowanie
Zarówno kanagliflozynę, jak i dapagliflozynę przyjmuje się doustnie w pojedynczej dawce dobowej. Kanagliflozynę początkowo stosuje się w dawce 100 mg, a w razie konieczności lepszego kontrolowania glikemii można ją zwiększyć u pacjentów z eGFR > 60 ml/min/1,73 m2 do 300 mg. Kanagliflozyna jest przeciwwskazana, gdy eGFR < 45 ml/min/1,73 m2 (5, 7). Rekomendowana w USA dawka początkowa dapagliflozyny to 5 mg, którą można zwiększyć do 10 mg, zaś w Europie zaleca się dawkę 10 mg jako początkową i docelową. Nie zaleca się stosowania dapagliflozyny u pacjentów z eGFR < 60 ml/min/1,73 m2 (15).
Farmakodynamika
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
29 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
69 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
129 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 78 zł
Piśmiennictwo
1. Lin HW, Tseng CH: A review on the relationship between SGLT2 inhibitors and cancer. Int J Endocrinol 2014; vol. 2014, Article ID 719578, 6 pages, 2014. DOI: 10.1155/2014/719578. 2. International Diabetes Federation. Global diabetes plan 2011-2021; http: //www.idf.org/sites/default/files/Global_Diabetes_Plan_Final.pdf (dostęp 20.02.2016). 3. Triplitt C, Cornell S: Canagliflozin treatment in patients with type 2 diabetes mellitus. Clin Med Insights Endocrinol Diabetes 2015; 8: 73-81. 4. Devineni D, Curtin CR, Polidori D et al.: Pharmacokinetics and pharmacodynamics of canagliflozin, a sodium glucose co-transporter 2 inhibitor, in subjects with type 2 diabetes mellitus. J Clin Pharmacol 2013; 53(6): 601-610. 5. Nasser M: Place of sodium-glucose co-transporter type 2 inhibitors for treatment of type 2 diabetes. World J Diabetes 2014; 5(6): 854-859. 6. Cersosimo E, Solis-Herrera C, Triplitt C: Inhibition of renal glucose reabsorption as a novel treatment for diabetes patients. J Bras Nefrol 2014; 36(1): 80-92. 7. Bhatia J, Gamad N, Bharti S, Arya DS: Canagliflozin-current status in the treatment of type 2 diabetes mellitus with focus on clinical trial data. World J Diabetes 2014; 5(3): 399-406. 8. Sha S, Devineni D, Ghosh A et al.: Pharmacodynamic effects of canagliflozin, a sodium glucose co-transporter 2 inhibitor, from a randomized study in patients with type 2 diabetes. PLoS One 2014; 9(9): e110069. DOI: 10.1371/journal.pone.0110069. 9. Ottosson-Laakso E, Tuomi T, Forsèn B et al.: Influence of familial renal glycosuria due to mutations in the SLC5A2 gene on changes in glucose tolerance over time. PLoS One 2016; 11(1): e0146114. DOI: 10.1371/journal.pone.0146114. 10. Jung CH, Jang JE, Park JY: A novel therapeutic agent for type 2 diabetes mellitus: SGLT2 inhibitor. Diabetes Metab J 2014; 38(4): 261-273. 11. Rossetti L, Smith D, Shulman GI et al.: Correction of hyperglycemia with phlorizin normalizes tissue sensitivity to insulin in diabetic rats. J Clin Invest 1987; 79(5): 1510-1515. 12. Oku A, Ueta K, Arakawa K et al.: T-1095, an inhibitor of renal Na+-glucose cotransporters, may provide a novel approach to treating diabetes (Abstract). Diabetes 1999; 48(9): 1794-1800. 13. Oku A, Ueta K, Arakawa K et al.: Correction of hyperglycemia and insulin sensitivity by T-1095, an inhibitor of renal Na+-glucose cotransporters, in streptozotocin-induced diabetic rats. Jpn J Pharmacol 2000; 84(3): 351-354. 14. Nomura S, Sakamaki S, Hongu M et al.: Discovery of canagliflozin, a novel C-glucoside with thiophene ring, as sodium-dependent glucose cotransporter 2 inhibitor for the treatment of type 2 diabetes mellitus (Abstract). J Med Chem 2010; 53(17): 6355-6360. 15. Hinnen D: Glucuretic effects and renal safety of dapagliflozin in patients with type 2 diabetes. Ther Adv Endocrinol Metab 2015; 6(3): 92-102. 16. Eguchi K: Blood pressure management in patients with type 2 diabetes. Intern Med 2015; 54(18): 2285-2289. 17. Inagaki N, Goda M, Yokota S et al.: Effects of baseline blood pressure and low-density lipoprotein cholesterol on safety and efficacy of canagliflozin in Japanese patients with type 2 diabetes mellitus. Adv Ther 2015; 32(11): 1085-1103. 18. Filippatos TD, Liberopoulos EN, Elisaf MS: Dapagliflozin in patients with type 2 diabetes mellitus. Ther Adv Endocrinol Metab 2015; 6(1): 29-41. 19. Carlson GF, Tou CK, Parikh S et al.: Evaluation of the effect of dapagliflozin on cardiac repolarization: a thorough QT/QTc study. Diabetes Ther 2011; 2(3): 123-132. 20. Tahrani AA, Barnett AH: Dapagliflozin: a sodium glucose cotransporter 2 inhibitor in development for type 2 diabetes. Diabetes Ther 2010; 1(2): 45-56. 21. Fleming JW, Fleming LW, Davis CS: Fixed-dose combinations in type 2 diabetes – role of the canagliflozin metformin combination. Diabetes Metab Syndr Obes 2015; 8: 287-294. 22. Obermeier M, Yao M, Khanna A et al.: In vitro characterization and pharmacokinetics of dapagliflozin (BMS-512148), a potent sodium-glucose cotransporter type II inhibitor, in animals and humans. Drug Metab Dispos 2010; 38(3): 405-414. 23. Mamidi RN, Cuyckens F, Chen J et al.: Metabolism and excretion of canagliflozin in mice, rats, dogs, and humans. Drug Metab Dispos 2014; 42(5): 903-916. 24. Geerlings S, Fonseca V, Castro-Diaz D et al.: Genital and urinary tract infections in diabetes: impact of pharmacologically-induced glucosuria. Diabetes Res Clin Pract 2014; 103(3): 373-381. 25. James R, Hijaz A: Lower urinary tract symptoms in women with diabetes mellitus: a current review (Abstract). Curr Urol Rep 2014; 15(10): 440. DOI: 10.1007/s11934-014-0440-3. 26. Johnsson KM, Ptaszynska A, Schmitz B et al.: Vulvovaginitis and balanitis in patients with diabetes treated with dapagliflozin (Abstract). J Diabetes Complications 2013; 27(5): 479-484. 27. Srivali N, Thongprayoon C, Cheungpasitporn W, Ungprasert P: Acute pancreatitis in the use of canagliflozin: a rare side-effect of the novel therapy for type 2 diabetes mellitus. J Basic Clin Pharm 2015; 6(3): 101-102. 28. Chowdhary M, Kabbani AA, Chhabra A: Canagliflozin-induced pancreatitis: a rare side effect of a new drug. Ther Clin Risk Manag 2015; 11: 991-994. 29. Kaur A, Winters SJ: Severe hypercalcemia and hypernatremia in a patient treated with canagliflozin. Endocrinol Diabetes Metab Case Rep 2015; 2015: 150042. DOI: 10.1530/EDM-15-0042. 30. Kasichayanula S, Chang M, Liu X et al.: Lack of pharmacokinetic interactions between dapagliflozin and simvastatin, valsartan, warfarin, or digoxin (Abstract). Adv Ther 2012; 29(2): 163-177. 31. Polskie Towarzystwo Diabetologiczne: Zalecenia kliniczne dotyczące postępowania u chorych na cukrzycę 2015. Clinical Diabetology 2015; 4 (supl. A): 1-73.

