*Robert Kubina
Przeciwnowotworowy efekt kurkuminy oraz jej pochodnych w stosunku do komórek raka języka linii SCC-25**
Anticancer effect of curcumin and its derivatives againt oral squamous carcinoma cells (SCC-25) in vitro
Katedra i Zakład Patologii, Wydział Farmaceutyczny z Oddziałem Medycyny Laboratoryjnej w Sosnowcu, Śląski Uniwersytet Medyczny w Katowicach
Kierownik Katedry: dr hab. n. med. Barbara Stawiarska-Pięta
Streszczenie
Wstęp. W ostatnich latach zaobserwowano znaczny wzrost zachorowalności oraz śmiertelności spowodowanej nowotworami złośliwymi, w tym rejonu głowy i szyi. Dotychczasowe wyniki wskazują, że polifenole mogą wspomagać standardową chemioterapię nowotworów. Korzystne działanie wykazano po zastosowaniu kurkuminy oraz jej pochodnych.
Cel pracy. Celem pracy była ocena cytotoksycznego oraz proapoptotycznego wpływu kurkuminy oraz jej pochodnych na komórki raka płaskonabłonkowego języka linii SCC-25.
Materiał i metody. Komórki hodowane były zgodne z zaleceniami producenta przy użyciu podłoża DMEM:F12 (1:1) suplementowanego 10% surowicą FBS, 400 ng/ml hydrokortyzonu oraz dodatkiem 100 IU/ml penicyliny, 100 μg/ml streptomycyny oraz 0,25 μg/ml amfoterycyny B. W celu zbadania aktywności cytotoksycznej badanych związków zastosowano test MTT, a w celu wyznaczenia potencjalnego działania proapoptotycznego zastosowano cytometrię przepływową z wykorzystaniem testu Muse Annexin V and Dead Cell Assay Kit.
Wyniki. Wyznaczone wartości IC50 wynosiły 41,18 μmol/L dla kurkuminy, 36,67 μmol/L dla demetoksykurkuminy oraz 27,13 μmol/L dla bisdemetoksykurkuminy po 24 godz. inkubacji komórek. Analiza cytometryczna z użyciem barwienia aneksyny V wykazała, że kurkumina i jej pochodne aktywują proces fizjologicznej śmierci komórek.
Wnioski. Wykazana aktywność cytotoksyczna oraz proapoptotyczna kurkuminy oraz jej pochodnych była zależna od dawki oraz czasu ekspozycji.
Summary
Introduction. In recent years, a significant increase in morbidity and mortality from cancer including head/neck region, have been seen. The present results indicate that the polyphenols may support standard chemotherapy of tumors. The beneficial effects demonstrated for the use of curcumin and its derivatives.
Aim. The aim of this study was to evaluate the cytotoxic and proapoptotic effect of curcumin and its derivatives on cell line squamous cell carcinoma of tongue SCC-25.
Material and methods. Cells were cultured as recommended by the manufacturer using DMEM:F12 (1:1) supplemented with 10% FBS serum, 400 ng/mL hydrocortisone and the addition of 100 IU/mL penicillin, 100 μg/mL streptomycin, and 0.25 μg/mL amphotericin B. In order to investigate cytotoxic activity of test compounds an MTT assay was used, in order to determine the potential proapoptotic activity flow cytometry using Annexin V assay Muse and Dead Cell assay kit was used.
Results. The values of IC50 amounted to 41.18 μM for curcumin, 36.67 μM for demetexycurcumin and 27.13 μM for bisdemetoxycurcumin after 24 hours of incubation of the cells. Cytometric analysis using Annexin V staining revealed that curcumin and its derivatives activate physiological cell death process.
Conclusions. The demonstrated cytotoxic and proapoptotic activity of curcumin and its derivatives was dependent on the dose and duration of exposure.

Wprowadzenie
Większość nowotworów głowy i szyi oraz górnych dróg oddechowych to nowotwory pochodzenia płaskonabłonkowego. Raki płaskonabłonkowe regionu głowy i szyi zajmują szóste miejsce pod względem częstości występowania na świecie. Każdego roku wykrywanych jest 600 000 nowych przypadków tych raków i są one przyczyną 350 000 zgonów. Pod względem budowy histologicznej w około 95% występuje rak płaskonabłonkowy, zaś inne, takie jak rak brodawkowy, gruczołowy czy nabłonkowy występują znacznie rzadziej. Głównym czynnikiem powstawania nowotworów głowy i szyi, w tym raka języka, są powszechnie znane kancerogeny, wśród których największe znaczenie odgrywają substancje zawarte w dymie tytoniowym oraz wysokoprocentowe alkohole. Bardzo istotnymi z epidemiologicznego punktu widzenia czynnikami kancerogennymi są także higiena jamy ustnej oraz zakażenia wirusowe, takie jak zakażenie onkogennym typem wirusa brodawczaka ludzkiego (HPV) oraz zakażenia wirusem Epsteina-Barr (EBV). Wirusowy czynnik etiologiczny odgrywa jednak istotną rolę w przypadku raka krtani oraz nosogardzieli.
Rak języka stanowi poważny problem zdrowotny w niektórych krajach Azji Południowo-Wschodniej. Rosnącą liczbę przypadków obserwuje się także w Stanach Zjednoczonych, lecz liczba zgonów jest tam ograniczona przede wszystkim poprzez szczególny nacisk na wczesne wykrywanie tej choroby.
Dużym problemem klinicznym jest ograniczenie chemioterapii z powodu małej chemiowrażliwości tego typu nowotworów. Obecnie poszukuje się nowych związków pochodzenia naturalnego lub związków, które poddane modyfikacji chemicznej wykażą bardziej selektywną aktywność chemioterapeutyczną lub które będą mogły wspomagać standardową chemioterapię (1-4).
Do związków tych możemy zaliczyć kurkuminę oraz jej pochodne (ryc. 1). Sproszkowana kurkuma jest substancją koloru żółtego i zawiera kurkuminoidy, w tym 77% kurkuminy, 17% demetoksykurkuminy i 3% bisdemetoksykurkuminy.
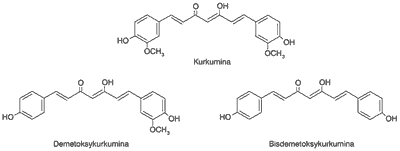
Ryc. 1. Budowa chemiczna kurkuminy oraz jej pochodnych: demetoksykurkuminy oraz bisdemetoksykurkuminy
Kurkumina jest uważana za substancję pomocną w leczeniu wielu chorób, takich jak: nowotwory, choroby neurodegeneracyjne, choroby zakaźne oraz cukrzyca. Zastosowanie tego związku w leczeniu jest utrudnione ze względu na słabą rozpuszczalność w wodzie, nietrwałość w środowisku wodnym oraz niski wychwyt komórkowy (5-8).
Liczne badania potwierdzają, że kurkumina i jej pochodne wykazują działanie przeciwnowotworowe, przeciwutleniające oraz przeciwzapalne (7). Wśród wszystkich właściwości, jakimi cechuje się kurkumina, naukowcy szczególnie zwracają uwagę na wpływ kurkuminy na cykl komórkowy, powodowanie apoptozy oraz zahamowanie proliferacji i migracji komórek nowotworowych. W ostatnim czasie prowadzone są badania mające na celu możliwości wykorzystania kurkuminy oraz jej pochodnych do leczenia chorób proliferacyjnych i zespołów metabolicznych. Badania wskazują, że polifenol ten odznacza się różnorodną aktywnością biologiczną, jednak mechanizmy biochemiczne nie w pełni zostały poznane. Potwierdzono, że kurkumina może oddziaływać z różnymi białkami, np. z czynnikami transkrypcyjnymi, enzymami, receptorami i czynnikami wzrostu. Jest ona także powszechnie znanym przeciwutleniaczem. Jednak ze względu na aktywację wielu szlaków biochemicznych trudno jednoznacznie określić, która z jej aktywności biologicznych odpowiada za efekt przeciwnowotworowy, gdyż działanie to może być wynikiem aktywności przeciwutleniającej, przeciwzapalnej oraz cytotoksycznej (9).
Cel pracy
Celem prezentowanej pracy była ocena właściwości cytotoksycznych kurkuminy oraz jej pochodnych (demetoksykurkuminy oraz bisdemetoksykurkuminy) w zależności od użytych stężeń oraz czasu działania powyższych substancji na komórki raka płaskonabłonkowego języka linii SCC-25 w badaniach in vitro.
Materiał i metody
Związki chemiczne
W badaniach wykorzystano kurkuminę, demetoksykurkuminę, bisdemetoksykurkuminę, bromek 3-(4,5-dimetylo-tiazol-2-ilo)-2,5-difenylotetrazolu (MTT) (Sigma-Aldrich). W badaniach wykorzystano roztwór antybiotyk/antymykotyk, trypsynę, roztwór PBS, płodową surowicę bydlęcą FBS i L-glutaminę (GE Healthcare) oraz etanol i dimetylosulfotlenek (Avantor Performance Materials).
Hodowla komórkowa
Linię komórkową SCC-25 ludzkiego raka płaskonabłonkowego języka (ATCC CRL-1628) hodowano zgodnie z zaleceniami producenta z zastosowaniem mieszaniny podłoża Dulbecco Modified Eagle Medium (DMEM) i Ham F12 (w stosunku 50:50) z dodatkiem 10% surowicy płodowej bydlęcej inaktywowanej termicznie. Pożywkę suplementowano 400 ng/ml hydrokortyzonu oraz roztworami antybiotyków o stężeniu końcowym: 100 UI/ml penicyliny, 100 μg/ml streptomycyny i 0,25 mg/ml amfoterycyny B.
Komórki nowotworowe hodowano w temp. 37°C w atmosferze wzbogaconej 5% dwutlenku węgla (CO2) w inkubatorze Panasonic MCO-170AICUV-PE. Hodowle komórkowe pasażowano za pomocą 0,25% roztworu trypsyny z EDTA i wysiewano do nowego naczynia hodowlanego w stosunku 1:4.
Ocena aktywności cytotoksycznej w teście MTT
Jako wskaźnik aktywności cytotoksycznej kurkuminy oraz jej pochodnych zastosowano test MTT z bromkiem 3-(4,5-dimetylotiazolo-2-ilo)-2,5-dimetylotetrazolu. Jest to metoda kolorymetryczna oceniająca aktywność metaboliczną komórek nowotworowych, oparta na konwersji soli tetrazoliowej do nierozpuszczalnego formazanu. Ilość utworzonego formazanu jest proporcjonalna do ilości żywych komórek. W celu oceny właściwości cytotoksycznych badanych związków w stosunku do komórek linii SCC-25 komórki wysiewano na płytki 96-stanowiskowe w liczbie 5000 komórek na studzienkę, a następnie dodawano odpowiedniej pożywki hodowlanej w ilości 0,2 ml. Komórki nowotworowe pozostawiono na 72 godz. w celu osiągnięcia wzrostu logarytmicznego. Po upływie tego czasu pożywkę usuwano i na płytki do odpowiednich stanowisk dodano badane substancje w określonych stężeniach.
Komórki hodowano przez 24, 48 i 72 godz. w celu oceny wpływu cytotoksycznego badanych kurkuminoidów. Po upływie tego czasu do każdej studzienki dodawano roztwór MTT (Sigma-Aldrich) w pożywce hodowlanej o końcowym stężeniu 2 mg/ml. Komórki pozostawiono z roztworem barwnika na 4 godz. Po tym czasie pożywkę usuwano znad komórek i do każdej studzienki dodawano po 200 μl dimetylosulfotlenku w celu rozpuszczenia powstałych kryształów formazanu. Odczytu absorbancji dokonywano przy użyciu czytnika do mikropłytek (Bio-Tek Instruments) przy długości fali 570 nm. Stopień cytotoksyczności obliczono według następującego wzoru: procent cytotoksyczności (martwe komórki) = (1 - [absorbancja badanej próbki/absorbancja kontroli]) x 100%.
Ocena procesu apoptozy z zastosowaniem cytometrii przepływowej
Apoptozę oraz nekrozę komórek raka języka linii SCC-25 traktowanych kurkuminą oraz jej pochodnymi oceniano przy użyciu zestawu Muse Annexin V and Dead Cell Assay Kit (Millipore) zgodnie z instrukcją obsługi i instrukcją producenta. Po zakończonej ekspozycji komórek na badane związki komórki nowotworowe trypsynizowano i przemywano dwukrotnie jałowym roztworem PBS. Sporządzano zawiesinę komórek w podłożu, tak aby końcowe stężenie wynosiło 1 x 105 komórek/ml. Protokół barwienia obejmował dodanie 100 μl zawiesiny komórek do 100 μl odczynnika Muse Annexin V and Dead Cell Assay Kit i wymieszanie roztworu. Próbki inkubowano przez 20 min w temp. pokojowej bez dostępu światła. Odsetek komórek apoptotycznych analizowano metodą cytometrii przepływowej przy użyciu systemu Muse Cell Analyzer (Millipore) i wyrażono jako udział procentowy komórek apoptotycznych. Jako kontrolę negatywną użyto czystego podłoża z dodatkiem surowicy FBS. Jako kontrolę pozytywną zastosowano pożywkę z dodatkiem paklitakselu w stężeniu 100 nmol. Test ten pozwala na rozróżnienie czterech populacji komórek: nieapoptotycznych (żywe) o fenotypie aneksyna V (–) i 7-AAD (–), wczesnoapoptotycznych o fenotypie aneksyna V (+) i 7-AAD (–), późnoapoptotycznych i martwych o fenotypie aneksyna V (+) i 7-AAD (+) oraz nekrotycznych o fenotypie aneksyna V (–) i 7-AAD (+).
Analiza statystyczna
Do utworzenia bazy danych posłużył program Microsoft Excel 2003 for Macbook. Analizę statystyczną uzyskanych wyników wykonano za pomocą programu Statistica wersja 8.0 (StatSoft). W celu sprawdzenia normalności rozkładu zastosowano test Shapiro-Wilka. Uzyskane wyniki przedstawiono jako średnią oraz odchylenie standardowe z trzech niezależnych eksperymentów, każdy w 12 pow-tórzeniach (*p < 0,05; **p < 0,01 test ANOVA Friedman.
Wyniki
Aktywność cytotoksyczna kurkuminy oraz jej pochodnych
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
24 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
59 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
119 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 28 zł
Piśmiennictwo
1. Anandharaj A, Ekshyyan O, Jia Y i wsp. EBV and not HPV sensitizes tobacco-associated head and neck cancer cell line FaDu to radiotherapy. Acta Otolaryngol 2016; 136(4):354-62.
2. Kruk-Zagajewska A, Wierzbicka M. Rak języka i dna jamy ustnej – rozpoznawanie i postępy w leczeniu. Wspol Onkol 2003; 7(4):264-74.
3. Ali H, Sinnott SJ, Corcoran P i wsp. Oral cancer incidence and survival rates in the Republic of Ireland, 1994-2009. BMC Cancer 2016; 16(1):950.
4. García-Kass AI, Herrero-Sánchez A, Esparza-Gómez G. Oral tongue cancer in public hospitals in Madrid, Spain (1990-2008). Med Oral Patol Oral Cir Bucal 2016; 21(6):658-e64.
5. Nagahama K, Utsumi T, Kumano T i wsp. Discovery of a new function of curcumin which enhances its anticancer therapeutic potency. Sci Rep 2016; 6:30962.
6. Deptuła T, Gruber B, Krówczyński A. Kurkumina i jej pochodne – zastosowanie w terapii przeciwnowotworowej i chemoochronnej. Post Fitoter 2014; (3):155-65.
7. Qadir MI, Naqvi ST, Muhammad SA. Curcumin: a polyphenol with molecular targets for cancer control. Asian Pac J Cancer Prev 2016; 17(6):2735-9.
8. Liu W, Zhai Y, Heng X i wsp. Oral bioavailability of curcumin: problems and advancements. J Drug Target 2016; 24(8):694-702.
9. Jankowski J. Kurkuma jako lek przeciwzapalny i przeciwnowotworowy. Post Fitoter 2004; (2):89-90.
10. Rak języka – wywiad z prof. zw. dr hab. med. Aliną Morawiec-Sztandera; http://publicznecentraonkologii.pl/pacjent/rak-jezyka-prof-zw-dr-hab-med-alina-morawiec-sztandera-wojewodzki-szpital-specjalistyczny-im-m-kopernika-w-lodzi/.
11. Khazaei-Koohpar Z, Entezari M, Movafagh A i wsp. Anticancer activity of curcumin on human breast adenocarcinoma: role of Mcl-1 gene. Iran J Cancer Prev 2015; 8(3):e2331.
12. Ding L, Ma S, Lou H i wsp. Synthesis and biological evaluation of curcumin derivatives with water-soluble groups as potential antitumor agents: an in vitro investigation using tumor cell lines. Molecules 2015; 20(12):21501-14.
13. Ye H, Wei X, Wang Z i wsp. A novel double carbonyl analog of curcumin induces the apoptosis of human lung cancer H460 cells via the activation of the endoplasmic reticulum stress signaling pathway. Oncol Rep 2016; 36(3):1640-8.
14. Bond? ML, Emma MR, Botto C i wsp. Biocompatible lipid nanoparticles as carriers to improve curcumin efficacy in ovarian cancer treatment. J Agric Food Chem 2017 Feb 7. DOI: 10.1021/acs.jafc.6b04409.
15. Dasiram JD, Ganesan R, Kannan J i wsp. Curcumin inhibits growth potential by G1 cell cycle arrest and induces apoptosis in p53-mutated COLO 320DM human colon adenocarcinoma cells. Biomed Pharmacother 2017; 86:373-80.
16. Pimentel-Gutièrrez HJ, Bobadilla-Morales L, Barba-Barba CC i wsp. Curcumin potentiates the effect of chemotherapy against acute lymphoblastic leukemia cells via downregulation of NF-κB. Oncol Lett 2016; 12(5):4117-24.
17. Klippstein R, Bansal SS, Al-Jamal KT. Doxorubicin enhances curcumin's cytotoxicity in human prostate cancer cells in vitro by enhancing its cellular uptake. Int J Pharm 2016; 514(1):169-75.
18. Zhou X, Su J, Feng S i wsp. Antitumor activity of curcumin is involved in down-regulation of YAP/TAZ expression in pancreatic cancer cells. Oncotarget 2016; 7(48):79076-88.
19. Marslin G, Sarmento BF, Franklin G i wsp. Curcumin encapsulated into methoxy poly(ethylene glycol) poly(ε-caprolactone) nanoparticles increases cellular uptake and neuroprotective effect in glioma cells. Planta Med 2016 (Epub ahead of print).
20. Yu X, Zhong J, Yan L i wsp. Curcumin exerts antitumor effects in retinoblastoma cells by regulating the JNK and p38 MAPK pathways. Int J Mol Med 2016; 38(3):861-8.
21. Xi Y, Gao H, Callaghan MU i wsp. Induction of Bcl-2 interacting Killer, BiK, is mediated for anti-cancer activity of curcumin in human head and neck squamous cell carcinoma cells. J Cancer 2015; 6(4):327-32.
22. Tsang RK, Tang WW, Gao W i wsp. Curcumin inhibits tongue carcinoma cells migration and invasion through downregulation of matrix metallopeptidase 10. Cancer Invest 2012; 30(7): 503-12.
23. Ip SW, Wu SY, Yu CC i wsp. Induction of apoptotic death by curcumin in human tongue squamous cell carcinoma SCC-4 cells is mediated through endoplasmic reticulum stress and mitochondria-dependent pathways. Cell Biochem Funct 2011; 29(8):641-50.
24. Masloub SM, Elmalahy MH, Sabry D i wsp. Comparative evaluation of PLGA nanoparticle delivery system for 5-fluorouracil and curcumin on squamous cell carcinoma. Arch Oral Biol 2016; 64:1-10.
25. Guan F, Ding Y, Zhang Y i wsp. Curcumin suppresses proliferation and migration of MDA-MB-231 breast cancer cells through autophagy-dependent akt degradation. PLoS One 2016; 11(1):e0146553.

