Urszula Kaczmarek1, Teresa Jackowska2, Maria Mielnik-Błaszczak3, Anna Jurczak4, *Dorota Olczak-Kowalczyk5
Indywidualna profilaktyka fluorkowa u dzieci i młodzieży – rekomendacje polskich ekspertów
Individualised caries prevention with fluoride in children and adolescents – recommendations of Polish experts
Streszczenie
Obok właściwej diety profilaktyka fluorkowa jest podstawową i skuteczną metodą zapobiegania próchnicy zębów mlecznych i stałych. Warunkiem zapewnienia jej bezpieczeństwa i skuteczności jest znajomość i przestrzeganie aktualnych zasad stosowania różnych metod i środków zawierających związki fluoru.
W ramach działalności Grupy Roboczej ds. Profilaktyki Fluorkowej Polskiego Oddziału Sojuszu dla Przyszłości Wolnej od Próchnicy (ACFF) powołano zespół ekspertów w dziedzinie stomatologii dziecięcej i pediatrii w celu aktualizacji stanowiska dotyczącego indywidualnej profilaktyki fluorkowej u dzieci i młodzieży w Polsce.
Dokonano przeglądu piśmiennictwa dotyczącego poziomu wiedzy na temat profilaktyki fluorkowej, korzystania z niej przez osoby w wieku rozwojowym w Polsce, skuteczności i bezpieczeństwa stosowania środków profilaktycznych zawierających związki fluoru oraz zaleceń w zakresie profilaktyki fluorkowej organizacji i towarzystw naukowych w różnych krajach na świecie. Pierwsza wersja dokumentu była dyskutowana i zaakceptowana przez zespół ekspertów w dziedzinie pediatrii i stomatologii dziecięcej w dniu 4 kwietnia 2019 roku. Aktualizację zaplanowano nie później niż po 5 latach od jego publikacji.
Dokument zawiera podstawowe informacje dotyczące poziomu wiedzy o profilaktyce fluorkowej rodziców, dzieci i młodzieży, mechanizmu przeciwpróchnicowego działania fluoru, bezpieczeństwa i skuteczności różnych metod indywidualnej profilaktyki fluorkowej i zasad jej stosowania w zależności od wieku i poziomu ryzyka próchnicy.
Summary
In addition to proper diet, the use of fluoride is the primary and effective method for the prevention of dental caries in primary and permanent dentition. Knowledge and compliance with the current guidelines for the use of different strategies and agents containing fluoride compounds is crucial for ensuring safety and efficacy of prevention.
A panel of experts in paediatric dentistry and paediatrics was established as part of the working group of the Polish Branch of Alliance for a Cavity-Free Future (ACFF) to update the position on individual fluoride prevention in children and adolescents in Poland.
We conducted a literature review on the knowledge of fluoride prevention, its use in the paediatric population in Poland, efficacy and safety of fluoride-containing preventive agents, as well as recommendations on fluoride prophylaxis issued by academic organisations and societies in different countries worldwide. The first version of the document was discussed and accepted by the panel of experts on paediatrics and paediatric dentistry on the 4th of April 2019. Update was scheduled for not later than 5 years after publication.
This document includes basic data on the knowledge of fluoride prevention in parents, children and adolescents, the anticariogenic mechanism of fluoride, the safety and efficacy of different methods for individual fluoride prophylaxis, and the principles for its use depending on age and the risk of caries.

Wstęp
Filarami zapobiegania chorobie próchnicowej są: prawidłowe odżywianie, dbałość o higienę jamy ustnej oraz stosowanie środków profilaktycznych zawierających fluorki. Fluorki wykorzystywane są w masowych, grupowych oraz indywidualnych metodach zapobiegania. Światowa Organizacja Zdrowia i Światowa Federacja Dentystyczna rekomendują ich profilaktyczne stosowanie, podkreślając ich skuteczność i bezpieczeństwo. Zwracają jednocześnie uwagę na konieczność monitorowania ekspozycji i oceny ich efektywności działania (1-3).
W profilaktyce indywidualnej fluor może być dostarczany:
– doustnie (tabletki lub krople) – metoda endogenna (suplementacja), wówczas wpływa na mineralizację powstających twardych tkanek zęba,
– zewnętrznie – metoda egzogenna, przez miejscową aplikację na wyrznięte zęby.
Pasty do zębów, płukanki, pianki, żele i lakiery zawierają różne stężenia związków fluoru. Mogą być stosowane w domu samodzielnie przez pacjenta (profilaktyka domowa) lub w gabinecie stomatologicznym (profilaktyka profesjonalna). Warunkiem skuteczności i bezpieczeństwa profilaktyki fluorkowej jest przestrzeganie zasady indywidualnego doboru metod profilaktycznych, z uwzględnieniem ekspozycji na związki fluoru pochodzące z różnych źródeł, wieku dziecka oraz poziomu ryzyka próchnicy. Zgodnie z wynikami badań ankietowych przeprowadzonych w 2014 roku 14,0% lekarzy dentystów w Polsce nie dokonuje oceny ryzyka próchnicy przed wyborem metody profilaktycznej. Ponad połowa ankietowanych uważa, że profilaktyka fluorkowa powinna być stosowana u każdego pacjenta, 38,9% – przy wysokim ryzyku próchnicy niezależnie od wieku, a według 21,3% – tylko w okresie uzębienia mlecznego i mieszanego (4).
Należy podkreślić, że w Polsce profilaktyka fluorkowa w podstawowym zakresie może być realizowana w ramach świadczeń gwarantowanych, finansowanych ze środków publicznych („Wykaz świadczeń ogólnostomatologicznych dla dzieci i młodzieży do ukończenia 18. roku życia” oraz „Wykaz świadczeń stomatologicznych dla dzieci od 6. miesiąca życia do ukończenia 19. roku życia w formie 13 zróżnicowanych dla wieku pakietów działań zapobiegawczych”).
W latach 2013 i 2015 opublikowano stanowiska Niezależnego Panelu Ekspertów na temat indywidualnej profilaktyki fluorkowej (5, 6). Rozpowszechniane nieprawdziwe informacje o szkodliwości profilaktyki fluorkowej i jednocześnie pojawiające się nowe badania naukowe dotyczące bezpieczeństwa i skuteczności środków profilaktycznych zawierających fluorki zobowiązują do zaktualizowania ww. dokumentów.
Metodyka
Grupa Robocza ds. Profilaktyki Fluorkowej Polskiego Oddziału Sojuszu dla Przyszłości Wolnej od Próchnicy (ACFF) dokonała przeglądu aktualnego piśmiennictwa dotyczącego potrzeb profilaktycznych dzieci i młodzieży w Polsce, mechanizmu działania, skuteczności i bezpieczeństwa stosowania związków fluoru w zapobieganiu próchnicy zębów w tej grupie wiekowej oraz analizy zaleceń dotyczących profilaktyki fluorkowej towarzystw naukowych, m.in. Amerykańskiej Akademii Stomatologii Dziecięcej (AAPD), Europejskiej Akademii Stomatologii Dziecięcej (EAPD), Amerykańskiego Towarzystwa Stomatologicznego (ADA) i Światowej Federacji Dentystycznej (FDI) (1, 2, 7-9). Uzyskane informacje pozwoliły na opracowanie dokumentu dyskutowanego i zaakceptowanego w dniu 4 kwietnia 2019 roku w czasie panelu ekspertów złożonego z przedstawicieli Polskiego Towarzystwa Stomatologii Dziecięcej, Sekcji Stomatologii Dziecięcej Polskiego Towarzystwa Stomatologicznego oraz konsultantów krajowych w dziedzinach stomatologii dziecięcej i pediatrii. Kolejną aktualizację zaplanowano nie później niż po 5 latach od publikacji.
Wyniki
Potrzeby w zakresie zapobiegania próchnicy polskich dzieci
Na potrzeby w zapobieganiu chorobie próchnicowej u polskich dzieci wskazują wyniki badań epidemiologicznych realizowanych od 1987 roku we współpracy ze Światową Organizacją Zdrowia (6-9). Aktualne wyniki badań monitoringowych wskazują, że u dzieci w wieku od 3 do 6 lat 2,5-krotnie wzrasta średnia liczba zębów dotkniętych próchnicą (z 1,85 do 4,66) i o ok. 40% częstość występowania próchnicy (z 41,1 do 81,9%). W wieku 12 lat próchnicą objętych jest średnio 3,75 zęba i liczba ta po upływie 3 lat wzrasta o 1,08 (w wieku 15 lat wynosi 4,88), a po następnych 3 latach zwiększa się dalej o 1,62 (w wieku 18 lat osiąga wartość 6,50) (10-12). Niepokojąca jest obecność próchnicy w wyrzynających się zębach stałych pierwszych trzonowych – u 8 dzieci w wieku 5 lat i 19 dzieci w wieku 6 lat oraz u 59 w wieku 7 lat na 100 zbadanych dzieci. Rozpatrując trend choroby próchnicowej u dzieci 12-letnich w okresie 27 lat (1987-2016), stwierdzono nieznaczną tendencję spadkową frekwencji (z 89,9 do 85,4%) i intensywności próchnicy (z 4,4 do 3,75) ze znacznymi fluktuacjami wartości w tym okresie (10-12).
Aktualne badania epidemiologiczne ujawniły także niewystraczający poziom korzystania dzieci w Polsce z profilaktyki fluorkowej, zbyt późne jej wprowadzanie oraz niewystarczający poziom wiedzy rodziców odnośnie zasad jej stosowania (10-13).
W 2017 roku zaledwie co drugie dziecko w wieku 3 lat miało oczyszczane zęby co najmniej 2 razy dziennie, 36,4% jeden raz dziennie, a 8,8% 1-3 razy w tygodniu. Niestety co piąty rodzic nie posiadał wiedzy, czy stosowana u dziecka pasta do zębów zawiera fluor, a 27,5% przyznało, że stosuje pastę bez fluoru. U co trzeciego dziecka 3-letniego ilość pasty nakładanej na szczoteczkę była zbyt duża i zaledwie co trzecie dziecko miało oczyszczane zęby przez osobę dorosłą. Tylko u 10,7% dzieci zastosowano lakier fluorkowy (11). Podobnie wielu nastolatków nie wie, czy pasta do zębów, którą stosują, zawiera fluor. Wiedzy takiej nie posiadało 43,0% osób w wieku 12 lat (2016), 44,7% w wieku 15 lat (2018) i 52,1% w wieku 18 lat (2017) (10-12). Blisko połowa osób w wieku 12 i 18 lat nie wiedziała, że stosowanie środków profilaktycznych zawierających związki fluoru zapobiega próchnicy zębów i że oprócz past do zębów istnieją inne środki profilaktyczne zawierające te związki (10, 12).
Wieloletnie obserwacje wykazały, że poziom próchnicy jest związany z poziomem fluoru w wodzie pitnej. Na podstawie ponad 100 badań przeprowadzonych w 23 krajach przed 1990 rokiem redukcję próchnicy związaną z fluorkowaniem wody szacuje się na 40-50% dla zębów mlecznych i 50-60% dla zębów stałych. Zgodnie z przeglądem badań z lat 1990-2000 redukcję próchnicy zębów mlecznych oceniono na 30-59%, dla zębów stałych na 40-49% (3). Optymalny poziom fluoru w wodzie pitnej w odniesieniu do zdrowia zębów oszacowano na około 0,7 mg/l (0,5-1 mg/l) (3). Według Światowej Organizacji Zdrowia nie powinien przekraczać 1,5 mg F/l. W wielu regionach na świecie, gdzie naturalna zawartość fluoru w wodzie jest śladowa lub niska, dodawane są do niej związki fluoru do kariostatycznie optymalnego poziomu. Udowodniono, że fluorkowanie wody jest skuteczną i bezpieczną metodą zapobiegania próchnicy u dzieci i dorosłych. Stwierdzono także, że korzyści wynikające z fluorkowania wody w odniesieniu do redukcji próchnicy znacznie przewyższają ewentualne negatywne efekty estetyczne, tj. wystąpienie bardzo łagodnej lub łagodnej fluorozy zębów. W wielu innych regionach świata fluorkowane są sól (m.in. w Niemczech, Szwajcarii, Francji, w krajach Ameryki Łacińskiej) lub mleko (2, 3).
W Europie z wody sztucznie fluorkowanej korzysta 71% mieszkańców Irlandii, po 10% Wielkiej Brytanii i Hiszpanii i 3% Serbii, natomiast w USA 75%, Australii 70%, Nowej Zelandii ok. 50% i w Kanadzie 38,7% (14).
W Polsce przeważająca większość społeczeństwa korzysta z wody zawierającej poniżej 0,5 mg F/l, tj. dolnej wartości zakresu zalecanego przez Światową Organizację Zdrowia (1994). Dane dotyczące zawartości poziomu fluoru w wodzie pitnej zgromadzone na podstawie aktualnego piśmiennictwa przedstawiono na rycinie 1 (15-17).
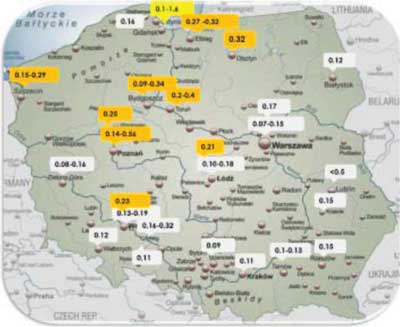
Ryc. 1. Poziom fluoru w wodzie pitnej w wybranych miejscowościach Polski na podstawie aktualnego piśmiennictwa (15-17)
Przytoczone dane epidemiologiczne oraz dotyczące ekspozycji społeczeństwa polskiego na fluor w wodzie pitnej podkreślają konieczność wzmocnienia działań profilaktycznych i edukacyjnych w zakresie bezpieczeństwa, zasad i efektywności stosowania profilaktyki fluorkowej wśród rodziców, dzieci i młodzieży w Polsce. Ważne jest także zaangażowanie w powyższe działania nie tylko personelu stomatologicznego, ale także personelu medycznego oraz wychowawców i nauczycieli. Analiza porównawcza wyników badań ankietowych przeprowadzonych wśród nauczycieli nauczania początkowego w latach 2008 i 2018 wykazała zmniejszenie się odsetka osób uważających za korzystne stosowanie profilaktyki fluorkowej z 74,5 do 53,6% (12).
Badania epidemiologiczne ujawniły także polaryzację próchnicy, tj. występowanie osób z bardzo wysoką intensywnością choroby nawet przy ogólnie niskich średnich wskaźnikach intensywności próchnicy. Dlatego zasadne jest wyodrębnienie osób z ryzykiem próchnicy ocenionym jako wysokie i stosowanie u nich intensywnych, indywidualnie ukierunkowanych działań profilaktycznych.
Ryzyko choroby próchnicowej a profilaktyka fluorkowa
Wybór metody profilaktyki fluorkowej oraz rodzaju środków profilaktycznych zawierających fluor uwarunkowany jest wieloma czynnikami, w tym: wiekiem dziecka, ogólnym stanem zdrowia, potrzebami profilaktyczno-leczniczymi, poziomem ryzyka próchnicy, ekspozycją na fluor pochodzący z różnych źródeł, a także stopniem zaangażowania i możliwościami rodziców. Zapobieganie próchnicy oparte na ocenie poziomu ryzyka próchnicy polega na intensyfikacji profilaktyki wraz ze wzrostem ryzyka choroby. Opracowanie zindywidualizowanego planu zapobiegawczego zawsze wymaga oceny poziomu ryzyka próchnicy.
Ryzyko próchnicy to prawdopodobieństwo wystąpienia nowych zmian próchnicowych w przyszłości i progresji zmian już obecnych. Zgodnie z teorią dynamicznej równowagi między demineralizacją a remineralizacją, ocena ryzyka próchnicy oparta jest na określeniu relacji między czynnikami uznanymi jako ochronne (stosowanie profilaktyki fluorkowej, środków antybakteryjnych i laków szczelinowych, właściwe nawyki dietetyczne, prawidłowe wydzielanie śliny), które sprzyjają remineralizacji a wskaźnikami próchnicy (obecność początkowych zmian próchnicowych w postaci białych plam, defektów szkliwa zwiększających retencję płytki bakteryjnej oraz wypełnień ubytków próchnicowych zębów < 3. roku życia) i czynnikami ryzyka tej choroby (obecność bakterii kariogennych, zmniejszenie wydzielania śliny, nieprawidłowe nawyki dietetyczne), które sprzyjają demineralizacji (18-20).
Istnieje kilka metod oceny ryzyka próchnicy zębów. Amerykańska Akademia Stomatologii Dziecięcej (AAPD) do oceny ryzyka próchnicy zaproponowała system CRA (Caries Risk Assessment), który składa się z trzech narzędzi oceny ryzyka próchnicy, w tym dwóch do zastosowania przez personel stomatologiczny: dla dzieci w wieku 0-5 lat oraz dla dzieci > 6 lat, oraz jedno – do stosowania przez personel medyczny niestomatologiczny, przeznaczone dla dzieci w wieku 0-3 lat (20). CRA jest systemem łatwym do zastosowania w praktyce klinicznej, który umożliwia oszacowanie ryzyka próchnicy (niskie, umiarkowane lub wysokie). Wymaga jednak przeprowadzenia wywiadu środowiskowego, ogólnomedycznego oraz badania stomatologicznego i w dużej mierze opiera się na wiedzy i doświadczeniu klinicznym lekarza. Stosowanie systemów oceny ryzyka uwidacznia dodatkowo pacjentom i opiekunom przyczyny choroby próchnicowej oraz ułatwia sformułowanie zaleceń lekarskich.
Mechanizm kariostatycznego działania fluoru
Liczne dowody naukowe potwierdzają skuteczność stosowania związków fluoru w zapobieganiu próchnicy zębów oraz w nieinwazyjnym leczeniu wczesnych zmian chorobowych.
Endogenna doustna podaż optymalnej dawki fluoru podczas rozwoju zębów powoduje wzrost zawartości fluoru w powierzchownej warstwie szkliwa, umożliwiając tworzenie stabilnej sieci krystalicznej apatytu. Fluor wpływa na pierwotną mineralizację organicznej matrycy i przederupcyjne dojrzewanie szkliwa. Katalizuje reakcję powstawania hydroksyapatytu Ca10(PO4)6(OH)2. Zastępując jony hydroksylowe (OH-), tworzy fluorohydroksyapatyt Ca5(PO4)3OH1-xFx. Sprzyja tworzeniu większych kryształów apatytów z mniejszą zawartością węglanów. Fluor uczestniczy w przederupcyjnym dojrzewaniu szkliwa, które polega na usuwaniu wody i białek z pierwotnego szkliwa (21).
Do niedawna uważano, że efektem przederupcyjnego działania fluoru jest mniejsza wrażliwość szkliwa na działanie kwasów. Zawartość fluoru w szkliwie nie wpływa jednak istotnie na poziom ryzyka choroby próchnicowej. Jego nadmierny dowóz może być natomiast przyczyną fluorozy zębów (3, 21-23). Ważniejsze jest więc działanie egzogenne fluoru zapewniające stałe dostarczanie niewielkich jego ilości do środowiska jamy ustnej po wyrznięciu zębów.
Przeciwpróchnicowe oddziaływanie fluoru po wyrznięciu zębów polega na:
1. Ograniczaniu wpływu bakterii próchnicotwórczych przez:
– zmniejszenie produkcji kwasów,
– zmniejszenie odkładania płytki bakteryjnej na powierzchni zębów (zakłócanie syntezy zewnątrzkomórkowych polisacharydów bakteryjnych),
– hamowanie przemian metabolicznych węglowodanów w komórce bakteryjnej (m.in. poprzez obniżanie aktywności enolazy i upośledzenie transportu glukozy do wnętrza bakterii, zakłócanie tworzenia wewnątrzkomórkowych zapasowych polisacharydów).
2. Wspomaganiu remineralizacji (obecność jonów fluorkowych przyciąga wapń i fosforany – powstaje nowy minerał zęba; do podwyższenia remineralizacji wystarczają bardzo niskie stężenia F w środowisku zęba – powyżej 0,03 ppm, które na takim poziomie (0,03-0,10 ppm) utrzymują się przez kilka godzin po użyciu pasty fluorkowanej) i hamowaniu demineralizacji (tworzenie fluoroapatytu/fluorohydroksyapatytu bardziej odpornego na rozpuszczanie w kwasach).
Zęby są zbudowane z hydroksyapatytu i węglanoapatytu, który łatwiej ulega rozpuszczaniu w kwasach. Częściowo zdemineralizowane kryształy węglanoapatytu stają się nukleatorami, do których adsorbują się jony fluorkowe, przyciągając jony wapnia i fosforanowe. W rezultacie na krysztale powstaje powłoka fluoroapatytopodobna (bez wbudowanych jonów węglanowych) i kryształ staje się bardziej odporny na rozpuszczanie w kwasach.
Po aplikacji na ząb preparatów zawierających < 50 ppm fluoru z pH zakwaszonym lub obojętnym (wolniejsze tworzenie) powstaje fluorohydroksyapatyt. Natomiast, gdy preparat zawiera > 100 ppm fluoru przy kwaśnym pH lub > 300 ppm F przy pH obojętnym, powstaje fluorek wapnia (tworzony z wapniem pochodzącym z uprzednio rozpuszczonego szkliwa), który stanowi rezerwuar jonów fluorkowych uwalnianych podczas kolejnego ataku kwasów bakteryjnych na ząb (ryc. 2 i 3) (21, 24, 25).

Ryc. 2. Tworzenie mniej wrażliwego na działanie kwasów fluorohydroksyapatytu z powłoką fluoroapatytopodobną przy niskich stężeniach jonów fluorkowych w środowisku jamy ustnej
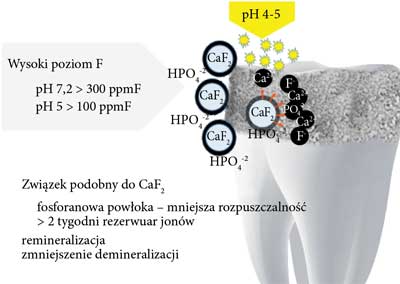
Ryc. 3. Tworzenie fluorku wapnia przy wysokich stężeniach jonów fluorkowych w środowisku jamy ustnej
Bezpieczeństwo profilaktyki fluorkowej u dzieci
Stosowanie fluoru ze względu na jego wysoką cytotoksyczność i małą różnicę między dawką toksyczną i dawką profilaktyczną wymaga bardzo rozważnego postępowania. Nieprzestrzeganie zasad profilaktyki fluorkowej może stanowić ryzyko zatruć ostrych i przewlekłych. Światowa Organizacja Zdrowia (WHO) podkreśla zasadność monitorowania ekspozycji na fluorki, polegającego na ocenie zrównoważenia ciężkości choroby próchnicowej zębów w populacji z ryzykiem rozwoju fluorozy zębów u dzieci wynikającym z kumulacji podaży fluoru pochodzącego z różnych źródeł. Światowa Federacja Dentystyczna (FDI) rekomenduje wypracowanie w danym kraju własnej polityki zdrowotnej i monitorowania skuteczności działań zapobiegających rozwojowi choroby próchnicowej (1-3).
Ryzyko wystąpienia fluorozy zębów zależy nie tylko od ekspozycji na fluorki, ale także od wrażliwości poszczególnych osób w danej populacji na fluor. Dlatego objawy łagodnej fluorozy zębów mogą występować także na obszarach, gdzie jego zawartość w wodzie pitnej mieści się w przedziale uważanym za optymalny, tj. 0,5-1,0 mg/l (3, 22, 23, 26, 27, WHO 1994).
Wyjaśnienia zjawiska fluorozy zębów poszukuje się w sumowaniu się dawek pochodzących z różnych źródeł (np. wody butelkowane, herbata, przetwory rybne, żywność importowana produkowana w rejonie fluorkowanej wody). Nadmierna ekspozycja na fluorki w tzw. krytycznym okresie, tj. od 15. do 30. miesiąca życia, jest przyczyną fluorozy zębów stałych przednich i pierwszych trzonowych, a w okresie późniejszym (do 6. roku życia) – pozostałych zębów. Przyczyną fluorozy mogą być m.in.:
– przygotowywanie mleka modyfikowanego dla niemowląt na bazie wody zawierającej zbyt duże stężenia związków fluoru. Zawartość fluoru w wodach butelkowanych w Polsce waha się od 0,1 do 1,39 mg F/l (28),
– niewłaściwe stosowanie suplementacji fluorkowej (należy uwzględnić inne składniki diety przy ustalaniu wskazań do objęcia dziecka tą formą profilaktyki) (29, 30),
– połykanie środków profilaktycznych niewłaściwie stosowanych u dzieci, np. nakładanie na szczoteczkę zbyt dużej ilości pasty do zębów oraz używanie w domu preparatów o zbyt wysokiej zawartości fluoru (31).
Szacowane dzienne spożycie fluoru z diety i past do zębów (bez stosowania suplementacji fluorkowej) przez dzieci w wieku 2 lat przy poziomie fluoru w wodzie pitnej 1 mg/l w porównaniu z wodą bez fluoru wynosi odpowiednio 0,069 i 0,046 mg F/kg m.c. (tab. 1) (32).
Tab. 1. Szacowane dzienne spożycie fluoru z diety i past do zębów przez dzieci w wieku 2 lat z uwzględnieniem suplementacji fluoru (32)
| | Szacowane dzienne spożycie (zakres) mg F/kg masy ciała |
| Poziom fluoru w wodzie pitnej mg/l (ppm) | 1 ppm | 0 ppm |
| Dieta (włączając wodę i napoje) | 0,046 (0,038-0,046) | 0,023 (0,015-0,023) |
| Pasta do zębów 1000 ppm F | 0,023 (0-0,154) | 0,023 (0-0,154) |
| Łącznie | 0,069 (0,038-0,20) | 0,046 (0,015-0,177) |
| Suplementacja fluoru | – | 0,038 |
| Łącznie z uwzględnieniem suplementacji fluoru | 0,069 (0,038-0,20) | 0,084 (0,054-0,215) |
Zawartość fluoru w dietach dzieci w wieku 1-4 lat, mieszkających w 16 miastach w różnych regionach Polski, przy jego poziomie w wodzie pitnej w przedziale 0,09-0,32 ppm F oszacowano w zakresie od 0,04 do 0,42 mg/kg (średnio 0,15 ± 0,07 mg/kg), niezależnie od pory roku. Dzienne spożycie fluoru przez dziecko w tym wieku oceniono na 0,28 mg (0,09-0,82 mg) (17). Łączne średnie pobranie fluoru z diety i past do zębów przez dzieci nie przekroczy więc odpowiedniego dziennego spożycia, które dla najmłodszych w wieku 1-3 lata wynosi 0,7 mg F/dzień (tab. 2).
Tab. 2. Wystarczające dzienne i dopuszczalne górne spożycie fluoru w zależności od wieku dziecka (33, 34)
| Wiek | Wystarczające dzienne spożycie fluoru mg/dzień (AI) | Dopuszczalne górne spożycie fluoru mg/dzień (UL) |
| 0-6 mies. | 0,01 | 0,7 |
| 6-12 mies. | 0,5 | 0,9 |
| 1-3 lata | 0,7 | 1,3 |
| 4-8 lat | 1,0 | 2,2 |
| 9-13 lat | 2,0 | – |
| 14-18 lat | 3,0 | – |
Biorąc pod uwagę zarówno bezpieczeństwo, jak i skuteczność profilaktyki fluorkowej towarzystwa naukowe, w tym EAPD, AAPD, ADA i FDI, w oparciu o dowody naukowe opracowały zasady jej stosowania u dzieci (1, 2, 7-9). Przy opracowaniu rekomendacji brano pod uwagę:
– możliwe dzienne spożycie fluoru z uwzględnieniem fluoru pochodzącego z wody, żywności i środków profilaktycznych,
– wystarczające spożycie dzienne fluoru (ang. adequate intake of fluoride – AI) (tab. 2),
– dopuszczalny górny poziom spożycia fluoru u dzieci (ang. upper intake level of fluoride – UL) niepowodujący efektów ubocznych – fluorozy zębów (ang. no-observed-adverse-effect level).
Na podstawie zależności pomiędzy dawką spożywanego fluoru a występowaniem i nasileniem fluorozy zębów wykazano, że przy spożyciu 0,1 mg F/kg m.c./dzień średnio nasilona fluoroza zębów występuje u poniżej 5% populacji (tab. 2) (33, 34).
Obecnie ogólnie przyjętymi zasadami stosowania związków fluoru w profilaktyce choroby próchnicowej są unikanie nadmiernej endogennej ekspozycji na fluor oraz intensyfikacja działań zapobiegawczych w zależności od poziomu ryzyka próchnicy. Należy unikać nadmiernego (ponadoptymalnego) endogennego spożycia fluoru w okresie ryzyka rozwoju fluorozy zębów, zwłaszcza poniżej 6. roku życia, poprzez:
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
29 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
69 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
129 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 78 zł
Piśmiennictwo
1. FDI: Promoting Oral Health through Water Fluoridation. Aktualizacja 2014. https://www.fdiworlddental.org/resources/policy-statements-and-resolutions/promoting-oral-health-through-water-fluoridation.
2. FDI: Promoting Dental Health through Fluoride Toothpaste. Aktualizacja 2018. https://www.fdiworlddental.org/resources/policy-statements/promoting-dental-health-through-fluoride-toothpaste.
3. O’Mullane DM, Baez RJ, Jones S et al.: Fluoride and Oral Health. Community Dental Health 2016; 33: 69-99.
4. Kaczmarek U, Majewska L, Olczak-Kowalczyk D: Postawa i wiedza stomatologów w zakresie profilaktyki fluorkowej. Nowa Stomatol 2015; 20(1): 23-28.
5. Adamowicz-Klepalska B, Borysewicz-Lewicka M, Dobrzańska A et al.: Aktualny stan wiedzy na temat indywidualnej profilaktyki fluorkowej choroby próchnicowej u dzieci i młodzieży. Niezależny Panel Ekspertów. J Stoma 2013; 66(4): 428-453.
6. Olczak-Kowalczyk D, Borysewicz-Lewicka M, Adamowicz-Klepalska B et al.: Stanowisko polskich Ekspertów dotyczące indywidualnej profilaktyki fluorkowej choroby próchnicowej u dzieci i młodzieży. Nowa Stomatol 2016; 21(1): 47-73.
7. AAPD: Fluoride Therapy. Aktualizacja 2018; https://www.aapd.org/globalassets/media/policies_guidelines/bp_fluoridetherapy.pdf.
8. EAPD: Guidelines on the use of fluoride in children: an EAPD policy document. Eur Archf Paediatr Dent 2009; 10(3): 129-135.
9. ADA Fluoridation Policy; https://www.ada.org/en/public-programs/advocating-for-the-public/fluoride-and-fluoridation/ada-fluoridation-policy.
10. Olczak-Kowalczyk D, Kaczmarek U, Bachanek T et al.: Monitorowanie stanu zdrowia jamy ustnej populacji polskiej w latach 2016-2020. Ocena stanu zdrowia jamy ustnej i jego uwarunkowań w populacji polskiej w wieku 5, 7 i 12 lat w 2016 roku. Dział Redakcji i Wydawnictw Warszawskiego Uniwersytetu Medycznego, Warszawa 2017.
11. Olczak-Kowalczyk D, Mielczarek A, Kaczmarek U et al.: Ocena stanu zdrowia jamy ustnej i jego uwarunkowań w populacji polskiej w wieku 3, 18 oraz 35-44 lata w 2017 roku. Dział Redakcji i Wydawnictw Warszawskiego Uniwersytetu Medycznego, Warszawa 2018.
12. Olczak-Kowalczyk D, Turska-Szybka A, Kaczmarek U et al.: Monitorowanie stanu zdrowia jamy ustnej populacji polskiej w latach 2016-2020. Ocena stanu zdrowia jamy ustnej i jego uwarunkowań w populacji polskiej w wieku 6, 10 i 15 lat w 2018 roku. Dział Redakcji i Wydawnictw Warszawskiego Uniwersytetu Medycznego, Warszawa 2019.
13. Turska-Szybka A, Świątkowska M, Walczak M, Olczak-Kowalczyk D: What do parents know about the use of fluoride products in children? A questionnaire study. Fluoride 2018; 51(2): 114-121.
14. https://en.wikipedia.org/wiki/Fluoridation_by_countr; https://www.canada.ca/en/services/health/publications/healthy-living/community-water-fluoridation-across-canada-2017.html.
15. Borysewicz-Lewicka M , Opydo-Szymaczek J: Fluoride in Polish drinking water and the possible risk of dental fluorosis. Pol J Environ Stud 2016; 25(1): 9-15.
16. Olczak-Kowalczyk D, Turska-Szybka A, Gozdowski D, Kaczmarek U: Defekty rozwojowe szkliwa u młodzieży w wieku 18 lat w Polsce: rozpowszechnienie i wybrane czynniki socjodemograficzne. Badania przekrojowe. Nowa Stomatol 2018; 23(2): 47-54.
17. Jędra M, Sawilska-Rautenstrauch D, Gawarska H, Starski A: Zawartość fluoru w całodziennych racjach pokarmowych małych dzieci w Polsce. Roczn PZH 2011; 62(3): 275-281.
18. Featherstone JD: The caries balance: The basis for caries management by risk assessment. Oral Health Prev Dent 2004; 2 (suppl. 1): 259-264.
19. Featherstone JD, Adair SM, Anderson MH et al.: Caries management by risk assessment: Consensus statement, April 2002. J Calif Dent Assoc 2003; 31(3): 257-269.
20. AAPD: Guideline on Caries-risk Assessment and Management for Infants, Children, and Adolescents 2014; http://www.aapd.org/media/policies_guidelines/g_cariesriskassessment.pdf.
21. Kaczmarek U: Mechanizmy kariostatyczne fluoru. Czas Stomatol 2005; 6: 404-413.
22. D’Hoore W, Van Nieuwenhuysen JP: Benefits and risks of fluoride supplementation: caries prevention versus dental fluorosis. Eur J Pediatr 1992; 152: 613-617.
23. Dąbrowska E, Balunowska M, Letko E: Zagrożenia wynikające z nadmiernej podaży fluoru. Nowa Stomat 2001; 4(18): 22-27.
24. ten Cate JM, Larsen MJ, Pearce EIF, Fejerskov O: Chemical interactions between the tooth and oral fluids. [In:] Fejerskov O, Kidd EAM (eds.): Dental caries. The disease and its clinical management. Blackwell Munksgaard, Oxford 2003; 49-70.
25. Ogaard B: CaF2 formation: cariostatic properties and factors of enhacing the effect. Caries Res 2001; 35 (suppl. 1): 40-44.
26. European Commision: Directorate-Deneral for Health & Consumers. Scientific Committee on Health and Environmental Risks SCHER: Critical review of any new evidence on the hazard profile, health effects, and human exposure to fluoride and the fluoridating agents of drinking water. SCHER 16.05.2011.
27. Public Health England: Water Fluoridation: Health monitoring report for England 2018; https://www.gov.uk/government/publications/water-fluoridation-health-monitoring-report-for-england-2018.
28. Borysewicz-Lewicka M, Chłapowska J, Wagner L, Trykowski J: Ocena zawartości fluorków w niektórych krajowych wodach mineralnych. Czas Stom 1999; 52(1): 29-32.
29. Opydo-Szymaczek J: Znaczenie oceny ekspozycji na fluorki w profilaktyce stomatologicznej. Stomat Współczesna 2003; 5(10): 44-48.
30. Opydo-Szymaczek J: Fluoride Exposure from Diet in Infants and Young Children Fed with the Foodstuffs for Particular Nutritional Uses. Dent Med Probl 2012; 49(2): 209-215.
31. Borysewicz-Lewicka M, Opydo-Szymaczek J, Opydo J: Fluoride ingestion after brushing with a gel containing a high concentration of fluoride. Biol Trace Elem Res 2007; 120(1-3): 114-120.
32. Mejáre I: Current guidance for fluoride intake: is it appropriate? Adv Dent Res 2018; 26: 167-176.
33. Dietary Reference intakes for Calcium, Phosphorus, Magnesium, Vitamin D, and Fluoride: Standing Committee on the Scientific Evaluation of Dietary Reference Intakes Food and Nutrition Board Institute of Medicine. National Academy Press, Washington, D.C. 1997; 288-313.
34. Opinion of the Scientific Panel on Dietetic Products, Nutrition and Allergies on a request from the Commission related to the Tolerable Upper Intake Level of Fluoride. The EFSA Journal 2005; 192: 1-65.
35. AAPD: Policy on Early Childhood Caries (ECC): Classifications, Consequences, and Preventive Strategies. 2014; http://www.aapd.org/media/policies_guidelines/p_eccclassifications.pdf.
36. Weyant RJ, Tracy SL, Anselmo TT et al.; American Dental Association Council on Scientific Affairs Expert Panel on Topical Fluoride Caries Preventive Agents: Topical fluoride for caries prevention: executive summary of the updated clinical recommendations and supporting systematic review. J Am Dent Assoc 2013; 144(11): 1279-1291.
37. Rozier RG, Adair S, Graham F et al.: Evidence-Based Clinical Recommendations on the Prescription of Dietary Fluoride Supplements for Caries Prevention. A report of the American Dental Association Council on Scientific Affairs. JADA 2010; 141(12): 1480-1489.
38. Beltran-Aguilar ED, Barker LK, Canto MT et al.: Surveillance for dental caries, dental sealants, tooth retention, edentulism, and enamel fluorosis: United States, 1988-1994 and 1999-2002. MMWR Surveill Summ 2005; 54: 1-43.
39. Wright JT, Hanson N, Ristic H et al.: Fluoride toothpaste efficacy and safety in children younger than 6 years. J Am Dent Assoc 2014; 145(2): 182-189.
40. McPherson CA, Zhang G, Gilliam R et al.: An Evaluation of Neurotoxicity Following Fluoride Exposure from Gestational Through Adult Ages in Long-Evans Hooded Rats. Neurotox Res 2018; 34(4): 781-798.
41. FDI: Topical and Systemic Fluorides in Children with Renal Diseases. Aktualizacja 2009; https://www.fdiworlddental.org/resources/policy-statements-and-resolutions/topical-and-systemic-fluorides-in-children-with-renal.
42. Tubert?Jeannin S, Auclair C, Amsallem E et al.: Fluoride supplements (tablets, drops, lozenges or chewing gums) for preventing dental caries in children. Cochrane Database Syst Rev 2011; (12): CD007592.
43. Steinbacher DM, Glick M: The dental patient with asthma. An update and oral health considerations. JADA 2001; 132: 1229-1239.
44. Iida H, Kumar JV: The association between enamel fluorosis and dental caries in U.S. schoolchildren. JADA 2009; 140: 855-862.
45. Korporowicz E, Rożniatowski P, Sobiech P, Kochman K: Rodzaj i ilość past do zębów używanych przez rodziców u dzieci w wieku od 1 do 7 lat. Nowa Stomatol 2014; 3: 124-126.
46. Walsh T, Worthington HV, Glenny AM et al.: Fluoride toothpastes of different concentrations for preventing dental caries in children and adolescents. Cochrane Database Syst Rev 2010; 20(1): CD007868.
47. American Dental Association Council on Scientific Affairs: Fluoride toothpaste use for young children. J Am Dent Assoc 2014; 145(2): 190-191.
48. Al-Mulla A, Karlsson L, Kharsa S et al.: Combination of high-fluoride toothpaste and no post-brushing water rinsing on enamel demineralization using an in situ caries model with orthodontic bands. Acta Odontol Scand 2010; 68(6): 323-328.
49. Nordström A, Birkhed D: Preventive effect of a high-flu oride dentifrice (5,000 ppm) in caries-active adolescents – a 2-year clinical trial. Caries Res 2010; 44: 323-333.
50. Marinho VCC, Higgins JP, Logan S, Sheiham A: Fluoride mouthrinses for preventing dental caries in children and adolescents. Cochrane Database Syst Rev 2003; 3: CD002284.
51. Marinho VCC: Cochrane fluoride reviews: an overview of the evidence on caries prevention with fluoride treatments. RCS 2014; 5(2): 78-83.
52. Alexander SA, Ripa LW: Effects of self-applied topical fluoride preparations in orthodontic patients. Angle Orthod 2000; 70: 424-430.
53. O’Reilly MM, Featherstone JD: Demineralization and remineralization around orthodontic appliances: an in vivo study. Am J Orthod Dentofacial Orthop 1987; 92: 33-40.
54. Twetman S, Keller MK: Fluoride Rinses, Gels and Foams: An Update of Controlled Clinical Trials. Caries Res 2016; 50 (suppl. 1): 38-44.
55. Sköld UM, Birkhed D, Borg E, Petersson LG: Approximal caries development in adolescents with low to moderate caries risk after different 3-year school-based supervised fluoride mouth rinsing programmes. Caries Res 2005; 39: 529-535.
56. Zero DT, Fu J, Espeland MA, Featherstone JD: Comparison of fluoride concentrations in unstimulated whole saliva following the use of a fluoride dentifrice and a fluoride rinse. J Dent Res 1988; 67: 1257-1262.
57. Duckworth RM, Horay C, Huntington E, Mehta V: Effects of flossing and rinsing with a fluoridated mouthwash after brushing with a fluoridated toothpaste on salivary fluoride clearance. Caries Res 2009; 43: 387-390.
58. Driscoll WS, Swango PA, Horowitz AM, Kingman A: Caries-preventive effects of daily and weekly fluoride mouthrinsing in a fluoridated community: final results after 30 months. J Am Dent Assoc 1982; 105: 1010-1013.
59. Heifetz SB, Meyers RJ, Kingman A: Comparison of the anticaries effectiveness of daily and weekly rinsing with sodium fluoride solutions: findings after three years. Pediatr Dent 1983; 4: 300-303.
60. Marinho VCC, Worthington HV, Walsh T, Chong LY: Fluoride gels for preventing dental caries in children and adolescents. Cochrane Clinical Answers 2015; http://cochraneclinicalanswers.com/doi/10.1002/cca.876/full.
61. Ekstrand J, Koch G, Lindgren LE, Petersson LG: Pharmacokinetics of fluoride gels in children and adults. Caries Res 1981; 15(3): 213-220.
62. Whitford GM: The metabolism and toxicity of fluoride. Monogr Oral Sci 1989; 13: 1-160.
63. Pendrys DG, Haugejorden O, Bårdsen A et al.: The risk of enamel fluorosis and caries among Norwegian children: implications for Norway and the United States. J Am Dent Assoc 2010; 141(4): 401-414.
64. Milgrom P, Taves DM, Kim AS et al.: Pharmacokinetics of fluoride in toddlers after application of 5% sodium fluoride dental varnish. Pediatrics 2014; 134(3): e870-874.
65. Browne D, Whelton H, O’Mullane D: Fluoride metabolism and fluorosis. J Dent 2005 Mar; 33(3): 177-186.
66. Holve S: An observational study of the association of fluoride varnish applied during well child visits and the prevention of early childhood caries in American Indian children. Matern Child Health J 2008; 12 (suppl. 1): 64-67.
67. Garcia RI, Gregorich SE Ramos-Gomez F et al.: Absence of Fluoride Varnish-Related Adverse Events in Caries Prevention Trials in Young Children, United States. Prev Chronic Dis 2017; 14: 160372.
68. Walczak M, Turska-Szybka A: The efficacy of fluoride varnishes containing different calcium phosphate compounds. Fluoride 2017; 50 (1 Pt 2): 151-160.
69. Turska-Szybka A, Soika I, Rozniatowski P et al.: Preventive effectiveness of fluoride varnishes in preschoolers: randomized controlled trials. FDI World Dental Congress, Madrid (29th August-1st September), Hiszpania 2017: S.212.



