© Borgis - Anestezjologia Intensywna Terapia 2/2004, s. 135-142
Leon Drobnik
Metamizol – lek ciągle nowoczesny
Metamizol – a drug which is still modern
Klinika Anestezjologii, Intensywnej Terapii i Leczenia Bólu;
kierownik: prof.dr hab. med. L. Drobnik – AM im. K. Marcinkowskiego w Poznaniu

Anest Inten Terap 2004; 36, 135-142
Wstęp
Ból jest odczuciem, które pojawia się pod wpływem działania na organizm czynników uszkadzających tkanki. W warunkach patologicznej nadwrażliwości układu nerwowego, odpowiedź na bodźce nocyceptywne może być niewspółmiernie wysoka (hiperalgezja) albo też odczucie bólu pojawia się w odpowiedzi na bodźce czuciowe nie towarzyszące uszkodzeniu, jak np. dotyk (allodynia).
Ból ma zasadniczo znaczenie informacji alarmowej dla organizmu i może być przez organizm modulowany przez włączenie w układzie nerwowym mechanizmów antynocycepcji i analgezji wewnętrznej. Z wytworzeniem stanu analgezji wenętrznej wiąże się efekt placebo, który podobnie jak analgezja zewnątrzpochodna, wywołana podaniem środków opioidowych, ustępuje po zastosowaniu naloksonu, antagonisty opioidów [1]. Przyjęcie przez organizm bodźców informujących o działaniu czynników zagrażających zniszczeniem uruchamia wszystkie systemy obronne organizmu; hormonalną odpowiedź stresową z podwyższoną pobudliwością układu nerwowego i zwiększoną czynnością hemodynamiczną, pobudzenie układu krzepnięcia krwi i uruchomienie systemów odporności z wywołaniem odpowiedzi zapalnej. Odczyn zapalny prowadzi do przekrwienia i obrzęku tkanek, w których się rozwija i do nasilenia bólu. Ból określony jako ostry utrzymuje się, jak to umownie przyjęto, do 3 miesięcy. Ból utrzymujący się dłużej określany jest jako przewlekły [2].
W uśmierzaniu bólu stosowane są leki o zróżnicowanej budowie i działaniu. W celu zapobiegania chao-tycznej i niekorzystnej empirii w stosowaniu środków przeciwbólowych w leczeniu bólu w chorobach nowotworowych, Światowa Organizacja Zdrowia zaleciła w roku 1986 stosowanie tzw. drabiny analgetycznej, w której wymieniono grupy środków, uporządkowanych według siły działania przeciwbólowego. Leczenie bólów nowotworowych rozpoczyna się od prostych środków analgetycznych [3].
Do grupy tej zaliczane są kwaśne analgetyko-antypyretyki, jak salicylany, arylooctany (indometacyna, diklofenak), arylopropioniany (ibuprofen, ketoprofen, naproksen, flurbiprofen) i ketoenolany (piroksykam, azapropazon, fenylobutazon) oraz analgo-antypyretyki niekwasowe, jak pochodna aniliny – paracetamol, pochodne pyrazoliny – fenazon, propyfenazon i metamizol. Słabym analgetykiem nieopioidowym jest także nefopam, lek zsyntetyzowany w czasie prób znalezienia środka przeciwdepresyjnego.
Leki z tej grupy używane były od dawna. Starożytni lekarze wojskowi greccy i rzymscy aplikowali rannym i cierpiącym artropatyczne bóle żołnierzom wywary wierzby i topoli [4]. Powszechność stosowania wymienionych środków w leczeniu przyczyniła się do znacznego poszerzenia wiedzy o ich zaletach i wadach. Zwłaszcza działania niepożądane leków oraz ich toksyczność, wzbudzają uzasadniony niepokój i często powodują odrzucenie leku, jako zbyt niebezpiecznego w działaniu klinicznym. Tak pozytywne jak i negatywne opinie o stosowanych lekach, opierają się nie tylko o wyważoną ocenę nagromadzonych na temat danego leku wiadomości ale i emocjonalną interpretację przyjmowanych informacji i niestety, czasami także o swoistą modę poglądów.
Leczenie bólu ostrego nie może opierać się o modę w stosowaniu takiego czy innego środka analgetycznego, muszą być one zatem poddawane ciągłemu sprawdzaniu i ocenie.
Metamizol
Jest jednym z najpowszechniej używanych środków przeciwbólowych. W Polsce znany jest od wielu lat jako preparat o nazwie pyralgina i stosowany szeroko w leczeniu bólu, także pooperacyjnego. Chociaż jest stosowany w praktyce lekarskiej od lat dwudziestych ubiegłego wieku (wprowadzony do leczenia w 1922 r.) mechanizm jego działania został poznany bliżej dopiero w ostatnich latach.
Metamizol jest solą sodową kwasu fenylo-dwumetylopirazolonometylaminometasulfonowego (C11H11N2O)?CH2SO3Na+H2O) (ryc. 1) – o masie cząsteczkowej 351. Substancja stanowi prawie biały, krystaliczny proszek, łatwo rozpuszczalny w wodzie i alkoholu metylowym, trudno rozpuszczalny w spirytusie i nierozpuszczalny w eterach [5]. Wykaz synonimów związków organicznych, stosowanych jako farmaceutyki Martina Negwera, wydany w roku 1978, wymienia 150 nazw, pod jakimi dostępny jest metamizol (dipyron, noramidopiryna, methampyron, methane sulfonat i inne) [6]. Współczesna wiedza na temat metamizolu została przedstawiona w przeglądowej pracy Mészáros w 2001 r. [7].
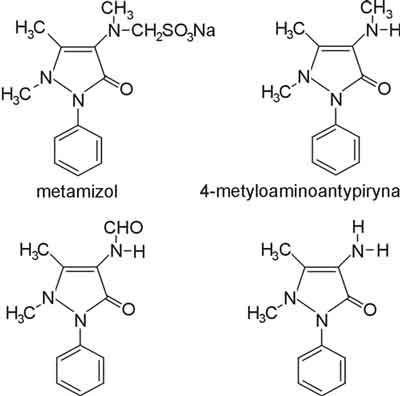
Ryc. 1. Metamizol i produkty przemiany.
Farmakokinetyka i farmakodynamika metamizolu
Po podaniu doustnym lub dożylnym metamizol ulega hydrolizie do 4-metyloaminoantypiryny (4-MAA), metabolizowanej w wątrobie do 4-formylaminoantypiryny (4-FAA) i 4-acetylaminoantypiryny (4-AAA) oraz 4-aminoantypiryny (4-AA) [8].
Te cztery czynne leczniczo metabolity metamizolu stanowią około 60% wszystkich, ponad 20 także czynnych biologicznie pochodnych (ryc. 1). Wydalane są drogą nerkową. Metyloaminoantypiryna (in. 4-metyloaminofenazon) wiąże się z białkami osocza w 58%, jej czas półtrwania wynosi 2-4 godzin, natomiast 4-AA wiąże się z białkami osocza w 48%, a jej okres półtrwania wynosi 4 do 5,5 godziny. Dostępność terapeutyczna metabolitów metamizolu jest zależna od wielu uwarunkowań, jak wiek chorego, przyjmującego ten lek, stan wydolności wątroby i nerek oraz genotyp [9]. W czasie ostrego wirusowego zapalenia wątroby oczyszczanie z metamizolu drogą utleniania zmniejsza się o 35-70%, a podobne zmniejszenie metabolizmu tego leku w wątrobie jest spostrzegane w innych zakażeniach wirusowych jak grypa czy AIDS, prawdopodobnie wskutek wzmożonego wytwarzania interferonu. W przewlekłym wirusowym zapaleniu wątroby nie ma istotnych odchyleń od prawidłowej eliminacji leku, a osobnicze różnice farmakokinetyczne wynikały ze zróżnicowania szlaków metabolicznych i polimorfizmu genetycznego [10]. U chorych z cukrzycą stężenia 4-MAA w surowicy po podaniu metamizolu były podwyższone, wskutek indukcji izoenzymu cytochromu P450 – CYP2B, przy niedostatecznej regulacji metabolizmu [11, 12].
Czynne farmakologicznie produkty rozpadu metamizolu hamują aktywność cyklooksygenazy typu 3 (COX 3). Wykryty niedawno w korze mózgu psów izoenzym został ostatnio wyizolowany i przebadany przez biochemików z Uniwersytetu Brigham w Provo w stanie Utah (USA) [13]. COX-3 występuje w większych ilościach w mózgowiu i rdzeniu kręgowym. Metamizol bardzo łatwo przechodzi przez bariery mózgowe do ośrodkowego układu nerwowego. Jego pochodna 4-MAA osiąga stężenie w surowicy krwi 104 mM a w tkankach mózgowia 86 mM, wystarczające do pełnego zahamowania aktywności tego enzymu [14]. Zmniejszenie aktywności cyklooksygenazy w OUN, podobnie jak ma to miejsce w obwodowych częściach organizmu, zapobiega wytwarzaniu prostaglandyn w odpowiedzi na odczyn zapalny, czy powtarzającą się stymulację aferentną bodźcami nocyceptywnymi. Ponieważ prostaglandyny PGE2 i PGI2 zwiększają pobudliwość receptorów i ułatwiają przewodnictwo w nerwach czuciowych, zahamowanie COX-3 zniesie to działanie, wywierając skutek analgetyczny [4]. Metamizol może także hamować aktywność COX-1 i COX-2, jednakże w stężeniu co najmniej sześciokrotnie wyższym niż w przypadku COX-3, przy czym większe powinowactwo wykazuje w stosunku do COX-2, która występuje w układzie nerwowym w postaci konstytutywnej. Jeszcze przed odkryciem cyklooksygenazy, Dembińska-Kiec i wsp. wskazywali na możliwość hamowania przez metamizol syntezy prostaglandyn w mózgowiu, chociaż przeciwzapalne działanie tego środka jest słabe w porównaniu z innymi niesteroidowymi lekami przeciwzapalnymi (NLPZ) [15, 16].
Metamizol wywiera również wpływ na inne enzymy. W badaniach in vitro metamizol zwiększał aktywność I i II izoenzymu anhydrazy węglanowej w błonach ludzkich erytrocytów, natomiast w badaniach in vivo na szczurach hamował aktywność tych enzymów [17]. Trudno więc ocenić znaczenie kliniczne tego mechanizmu. Nie jest też dotychczas jasne znaczenie ekspresji genów odpowiedzialnych za syntezę enzymu dehydrogenazy fosfoglicerolu (GPDH), pośredniczącego w przejściu fosforanu dihydroacetonu w fosfoglicerol, prekursor fosfolipidów i trójglicerydów, wykorzystywanych w budowie lub regeneracji błon komórkowych. Wzmożona ekspresja genu GPDH ma miejsce po zadziałaniu bodźców wywołujących odpowiedź stresową, jak ból, oparzenie lub wywołane podaniem odpowiednich toksyn drgawki (pentylenetetrazol, kainian). Wzmożona ekspresja genów ma miejsce także po podaniu analgetyków, jak morfina, salicylany lub metamizol. Wzmożona ekspresja genu i synteza GPDH jest widoczna po godzinie w istocie białej różnych struktur mózgu (w móżdżku nie ma zmian) i osiąga maksimum aktywności w 4 godziny po zadziałaniu bodźca lub podaniu metamizolu. Po czterech godzinach aktywność enzymu słabnie w mózgowiu lecz znacznie dłużej (do 6-8 godzin) utrzymuje się w rdzeniu kręgowym. Opisane zjawisko występuje głównie w komórkach gleju skąpowypustkowego i jest zależne od zwiększonego stężenia glukokortykoidów, stymulujących wewnątrzkomórkową syntezę białka. Uważa się, że ekspresja genu GPDH stanowi część odpowiedzi adaptacyjno-naprawczej organizmu na stres.
Metamizol, podobnie jak i inne analgetyki, może wpływać pobudzająco na syntezę endogennej substancji o przeciwbólowym działaniu [18-20]. Doretto i wsp. ze szkoły medycznej uniwersytetu w Sao Paulo stwierdzili w badaniach na zwierzętach przeciwdrgawkowe działanie metamizolu, którego nie wykazywały niesteroidowe leki przeciwzapalne i inne antypyretyki, które albo nie wpływały na pobudzenia drgawkowe, albo je nasilały, (salicylan sodu, fenylbutazon). Badacze wiązali przeciwdrgawkowy wpływ metamizolu z prawdopodobnym zahamowaniem zwrotnego wchłaniania adenozyny, której zwiększone stężenie nasila procesy hamowania w układzie nerwowym, czego fizjologicznym wyrazem może być wygaszenie pobudzeń drgawkowych oraz zmniejszenie napięcia mięśni gładkich, co wyjaśniałoby także spazmolityczne działanie metamizolu [21]. Inni badacze z tego samego uniwersytetu w Sao Paulo, wspólnie z kolegami z Narodowego Instytutu Zdrowia USA w Bethesda, wykazali cytoprotekcyjne oddziaływanie metamizolu na krwinki białe człowieka w stężeniu tego środka w zakresie 150-600 mM i działanie cytotoksyczne w wyższych stężeniach. Inne leki z grupy NLPZ nie tylko nie mają właściwości cytoprotekcyjnych, ale wręcz nasilają apoptozę poprzez zniesienie antyapoptotycznego wpływu prostaglandyn. Hamowanie przez metamizol apoptozy krwinek białych, poddanych działaniu czynników uszkadzających, tłumaczy się jego hamującym wpływem na aktywność kaspazy i przeciek cytochromu C [22]. Aktywność DNA w limfocytach T ulegała zmniejszeniu pod wpływem metamizolu w badaniach in vivo, przeprowadzonych u szczurów z użyciem znakowanej trytem urydyny [23]. Znaczenie kliniczne tego faktu nie jest do tej pory wyjaśnione.
Zastosowanie kliniczne metamizolu
Metamizol jest od wielu dziesięcioleci chętnie wykorzystywany w leczeniu takich objawów stanu zapalnego, jak ból, gorączka oraz bólów trzewnych o charakterze spastycznym.
Działanie przeciwgorączkowe metamizolu, związane z hamowaniem syntezy prostaglandyn i wyłączeniem ich wpływu na ośrodki termoregulacji w podwzgórzu oraz zmianą czynności mitochondrialnego łańcucha oddechowego w komórkach różni się w swym mechanizmie od działania NLPZ [24]. Nic więc dziwnego, że wskazania do stosowania leczniczego środków przeciwgorączkowych z grupy niekwasowych analgetyków przeciwzapalnych są zróżnicowane. W bólach głowy, migrenie i bólach nowotworowych wskazane są zarówno metamizol, propyfenazon jak i paracetamol, w zaburzeniach towarzyszących zakażeniom wirusowym – propyfenazon i paracetamol; w ostrych i przewlekłych silnych bólach oraz bólach występujących z wysoką gorączką zalecane są metamizol i propyfenazon a nie paracetamol, natomiast w bólach kolkowych tylko metamizol [25]. Mimo iż podwyższona temperatura ciała jest częstym objawem szeregu schorzeń, w których dochodzi do uwalniania pyrogenów, mediatorów stanu zapalnego jak i zmienionej odpowiedzi termoregulacyjnej, wskutek zaburzenia czynności OUN przez uraz, niedokrwienie, wpływ anestetyków lub toksyn, mediatorów stanu zapalnego i obecności krwi w płynie mózgowo-rdzeniowym, niewiele jest badań poświęconych w ostatnich latach lekom przeciwgorączkowym. Oborilova i wsp. ze szpitala uniwersyteckiego w czeskim Brnie porównali skuteczność działania przeciwgorączkowego metamizolu, diklofenaku i paracetamolu u chorych z nowotworami, przeważnie wywodzącymi się z układu krwiotwórczego. Leki były podawane we wlewach dożylnych. Metamizol (2500 mg i 1000 mg) oraz diklofenak (75 mg) okazały się skuteczniejsze od paracetamolu (2000 mg i 1000 mg). Większość chorych (87%) odczuło obniżenie temperatury ciała jako znaczną ulgę i poprawę samopoczucia [26]. Ajgaonkar i Pinto Pereira poddali ocenie przeciwgorączkowy wpływ metamizolu u chorych z paradurem w przebiegu zakażenia salmonellą t., którego endemiczne ognisko znajduje się w Bombaju, gdzie przeprowadzono badania. Wpływ metamizolu, podawanego doustnie w dawce 1000 mg, porównywali autorzy z efektem placebo. Znamienne obniżanie podwyższonej temperatury ciała rejestrowano od pierwszej do szóstej godziny po podaniu badanego leku [27].
Działanie przeciwbólowe metamizolu w kolkach jest od dawna znane i wykorzystywane w praktyce klinicznej. Przez dziesięciolecia zespoły pogotowia ratunkowego stosowały w bólach, towarzyszących kamicy moczowodów lub dróg żółciowych klasyczne połączenie metamizolu (Pyralgina), aminofenazonu (Pabialgina) i papaweryny, czasami łącznie z atropiną. Ponieważ w medycynie opartej na dowodach doświadczenie poparte nawet wieloletnią tradycją musi być weryfikowane, poddano kilkakrotnie badaniu skuteczność metamizolu w leczeniu kolki nerkowej. W wieloośrodkowych badaniach (13 ośrodków) na terenie Hiszpanii porównano u 451 chorych z kolką nerkową skuteczność leczenia petydyną, metamizolem i diklofenakiem. Jeśli skutek przeciwbólowy badanego środka był w ciągu 30 minut niewystarczający, podawano domięśniowo 100 mg petydyny. Nie stwierdzono istotnych różnic w skuteczności przeciwbólowej diklofenaku, metamizolu i petydyny [28]. Niestety, pod względem statystycznym te wieloośrodkowe badania miały niewielką moc dowodności, zwłaszcza w zakresie porównania efektu analgetycznego metamizolu i diklofenaku. Oba te środki porównano w innych, dokładniej zaprogramowanych badaniach randomizowanych, z użyciem podwójnie ślepej próby, u 293 chorych, cierpiących na kolkę nerkową [29]. Chorym podawano losowo, domięśniowo lub dożylnie metamizol 1 g lub 2 g albo też diklofenak 75 mg, domięśniowo lub dożylnie. Autorzy stwierdzili większą skuteczność przeciwbólową dwugramowej dawki metamizolu, w porównaniu z podaniem taką samą drogą 1 g metamizolu lub 75 mg diklofenaku.
Lloret i wsp. porównali w badaniach randomizowanych, z podwójnie ślepą próbą, wpływ zastosowania metamizolu w dawce 2,5 g oraz 1 g hyoscyny, oddzielnie lub w połączeniu z metamizolem, na zniesienie kolki nerkowej [30]. Najskuteczniejszym sposobem zniesienia bólu u 96 badanych chorych z kolką nerkową okazało się dożylne podanie 2,5 g metamizolu. Hyoscyna nie powodowała zniesienia bólu i nie zwiększała analgetycznego efektu metamizolu. Stosowanie od lat 50. ubiegłego stulecia w leczeniu kolki nerkowej środków wagolitycznych wynikało z przekonania, że bóle spastyczne w przebiegu kamicy są spowodowane zmianami napięcia przeciwstawnie działających części autonomicznego układu nerwowego. Ponieważ leczenie to nie było skuteczne, wcześnie włączono do leczenia metamizol i acetaminofen. Od lat siedemdziesiątych wiadomo, że źródłem bólu w kolce nerkowej jest wzrost napięcia i wydłużenie włókien mięśni gładkich moczowodu, w czym uczestniczą prostaglandyny, zwłaszcza PGE2 [31, 32]. Wysoka skuteczność metamizolu w leczeniu kolki nerkowej jest więc dobrze uzasadniona w badaniach klinicznych a mechanizm działania poznany.
Leczenie bólu ostrego i przewlekłego przy użyciu metamizolu, podawanego w formie doustnej lub parenteralnej było wielokrotnie poddawane ocenie klinicznej. Wydaje się, że tradycyjnie od dziesięcioleci metamizol jest jednym z najczęściej stosowanych doustnie środków przeciwbólowych przez chorych w ramach samoleczenia. Jak leczenie okazjonalnych, objawowych bólów głowy nie stanowi większego problemu, tak problemem jest leczenie bólów migrenowych. Bigal i wsp, z Kolegium Alberta Einsteina w Nowym Jorku, w randomizowanych badaniach z podwójnie ślepą próbą u 44 chorych z migreną bez aury i u 30 chorych migrenowych, u których występowała aura przed pojawieniem się bólów migrenowych, stwierdzili skuteczność przeciwbólową metamizolu, podawanego dożylnie w dawce 1 g w porównaniu z placebo, które stanowił fizjologiczny roztwór soli [33].
Z bólami obszaru unerwienia przez nerwy trójdzielne kojarzą się bóle uzębienia. Planas i wsp., w oparciu o wieloośrodkowe badania randomizowane z podwójnie ślepą próbą u 253 chorych, wykazali większą skuteczność analgetyczną 2 g metamizolu podanego doustnie, po leczeniu trzeciego zęba trzonowego dolnego, w porównaniu z dawką 1 g tego środka lub 600 mg ibuprofenu. Ibuprofen i metamizol 1 g miały podobną skuteczność przeciwbólową u chorych stomatologicznych [34]. Większą skuteczność stosowania metamizolu w leczeniu rwy kulszowej, w porównaniu z diklofenakiem i placebo wykazały wieloośrodkowe, kontrolowane badania niemieckie [35].
W leczeniu bólów nowotworowych stosowanie doustnych preparatów morfiny ma ustaloną pozycję w standardach leczenia. Jak każda metoda leczenia, tak i doustne stosowanie preparatów morfiny wiąże się z występowaniem szeregu objawów niepożądanych, co przy długotrwałym stosowaniu może być uciążliwe dla chorego. Porównywalność efektu przeciwbólowego metamizolu, stosowanego doustnie co 8 godzin w dawce 2 g, stwierdzona w badaniach Rodrigueza i wsp., otwiera możliwość okresowej zamiany leczenia morfiną na leczenie metamizolem, celem wyrównania zaburzeń ogólnoustrojowych, wynikających z przewlekłego stosowania morfiny [36].
Ból w okresie pooperacyjnym, jeśli jest silny i uporczywy, stanowi duży problem dla chorego jak również całego zespołu leczącego. Bólowe ograniczenie oddychania przyczyniać się może do większego prawdopodobieństwa niedodmy płuc i wystąpienia w nich zmian zapalnych. Odpowiedź na ból ze strony układu krążenia krwi, z tachykardią i obkurczaniem naczyń krwionośnych może prowadzić do zmian niedokrwiennych w obszarze serca i innych narządów. Ból w okresie pooperacyjnym opóźnia rehabilitację, wydłuża czas leczenia i pogarsza jakość życia chorego. Nic zatem dziwnego, że wiele badań klinicznych poświęcono ocenie różnych metod znoszenia bólu u chorych w okresie pooperacyjnym.
Przy wielu zaletach opioidowych środków przeciwbólowych, ich działanie psychotropowe i zmieniające równowagę autonomicznego układu nerwowego sprawiają, że poszukiwano i nadal poszukuje się środków analgetycznych, które mogłyby zastąpić lub znacznie zmniejszyć stosowanie leków opioidowych. Przed dwudziestu laty opublikowano wyniki kontrolowanych badań nad skutecznością leczenia bólu pooperacyjnego przez zastosowanie doustnie podawanych NLPZ. W badaniach, które obejmowały grupy 299 i 267 chorych po operacji epifizjotomii, stosowano przeciwbólowo aspirynę (0,5 g), paracetamol (0,5 g) i metamizol (0,5 g). W obu badaniach wykazano wyższą skuteczność metamizolu [37, 38].
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
29 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
69 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
129 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 78 zł
Piśmiennictwo
1. Jasmin L, Burkey A: Molecular biology of pain; in: Molecular basis of neurosurgical disease (ed.: Raffel C,Harsh IV GR), William&Wilkins, Baltimore 1996.
2. Duda K: Znieczulenie/analgezja a odpowiedź ustroju na uraz; w: Ból ostry (red.: Wordliczek J, Dobrogowski J), Wydawnictwo UJ, Kraków 2002.
3. Hilgier MOI: Ostry ból w chorobie nowotworowej (bóle przebijające); w: Ból ostry (red. Wordliczek J, Dobrogowski), Wydawnictwo UJ, Kraków 2002.
4. Brune K, Yaksh TL: Antypyretic-analgesic drugs; in: Anesthesia. Biologic foundations (ed.: Yaksh TL), Lippincott-Raven, Philadelphia 1998.
5. Novalgin; in: Hagers Handbuch der Pharmazeutischen Praxis (ed.: Frerichs G, Arends G, Zőrnig), Springer Vg., Berlin 1938, 528.
6. Negwer M: Organisch-Chemische Arzneimittel und ihre Synonima, Akademie Verlag, Berlin 1978, 410.
7. Mészáros J: Metamizol: skuteczność przeciwbólowa i bezpieczeństwo stosowania. Terapia i Leki 2001; 19: 40-45.
8. Levy M, Zylber-Katz E, Rosenkranz B: Clinical pharmacokinetics of dipyrone and ist metabolites, Clin Pharmacokinet, 1995; 28: 216-234.
9. Levy M, Safadi R, Zylber-Katz E, Granit L, Caraco J: Impairment of the metabolism of dipyrone in asymptomatic carriers of the hepatitis-B virus does not occur in rapid acetylators. Eur J Clin Pharmacol 2001; 57: 461-465.
10. Renton KW, Knickle KL: Regulation of hepatic cytochrome P450 during infectious diseases. Can J Physiol Pharmacol 1989; 68: 771-781.
11. Kraul H, Pasanen M, Sigusch H, Stenbäck F, Park SS, Gelboin HV, Pelkonen O: Immunohistochemical properties of dipyrone-induced cytochromes P450 in rats. Human ExpToxicol 1996; 15: 45-50.
12. Lautenschlager MT, Viktor S, Müller UA, Hoffmann A: Vergleich der Serumkonzentration von Coffein, 4-Monomethylaminoantipyrin, Sulfamethazin und Debrisoquin nach oraler Verabreichung dieser Substanzen als Cocktail bei Typ-II-Diabetikern vor und nach umstellung auf Insulin. Pharmazie 1996; 51: 750-753.
13. Chandrasekharan NV, Dai H, Roos LT, Evanson NK, Tomsik J, Elton TS, Simmons DL: COX-3, a cyclooxygenase-1 variant inhibited by acetaminophen and other analgesic/antipyretic drugs: Cloning, structure, and expression. PNAS 99: 13926-13931.
14. Wickelgren I: Enzym might relieve research headache. Science 2002; 297: 1976.
15. Campos C, de Gregorio R, Garcia-Nieto R, Gago F, Ortiz P, Alemany S: Regulation of cyclooxygenase activity by metamizol. Eur J Pharmacol 1999; 378: 339-347.
16. Dembińska-Kiec A, Żmuda A, Kupińska J: Inhibition of prostaglandine synthetase by aspirin-like drugs in different microsomal preparations; in: Advances in Prostaglandin and Thromboxane Research, vol. 1, (eds. Samuesson, Poolenti R), Raven Press, New York 1976.
17. Beydemir S, Ciftci M, Özmen I, Buyuk ME, Özdemir H, Küfrevioglu: Effects of some medical drugs on enzyme activities of carbonic anhydrase from human erytrocytes in vitro and from rat erythrocytes in vivo. Pharmacol Res 2002; 42: 187-191.
18. Lin ECC: Glycerol utilization and its regulation in mammals, Ann Rev Biochem 1977; 46: 765-795.
19. Link WA, Kauselmann G, Mellstrőm B, Kuhl D, Naranjo JR: Induction of glycerol phosphate dehydrogenase gene expression during seizure and analgesia. J Neurochem 2000; 75: 1419-1428.
20. Walker JS: NSAID: an update of their analgesic effects. Clin Exp Pharmacol Physiol 1995; 22: 855-860.
21.Doretto MC, Garcia-Cairasco, Pimenta NJG, Souza DA, Tatsuo MAKF: Dipyrone, a novel anticonvulsant agent? Insights from three experimental epilepsy models. Neuro Report 1998; 9: 2415-2421.
22. Pompeia C, Cury Boaventura MF, Curi R: Antiapoptotic effect of dipyrone on HL-60, Jurkat and Raji cell lines submitted to UV irradiation, arachidonic acid and cycloheximide treatments. Internat Immunopharmacol 2001; 1: 2173-2182.
23. Golikow PP, Nikolajewa NYu. Alekseejewa EA: Izmienienie matricznoj aktiwnosti dnk timocytow pod wlijaniem sriedstw, diejstwujuszczich na centralnuju nierwnuju sistiemu. Pat Fizjol Experim Ter 1989; 33: 18-21.
24. Souza GEP, Cardoso RA, Lora M, Brum-Fernandez AJ, Ferreira SH: Comparison of antipyretics profiles of indomethacin and dipyrone. Naunyn-Schmiedeberg Arch Pharmacol 1998; 30A: 584-587.
25. Yaksh TL, Malmberg AB: Interaction of spinal modulatory receptor systems; in: Progress in pain research and management, vol. (eds Fields HL, Libeskind JC) 1 Seattle IASP Press 1994,
26. Oborilova A, Mayer J, Pospisil Z, Koristek Z: Symptomatic intravenous antipyretic therapy; efficacy of metamizol, diclofenac and paracetamol. J Pain Symptom Manage 2002; 24: 608-615.
27. Ajagonkar VS, Pinto Pereira LM: Patient study of antipyretic drug efficacy. Current Ther Res 1985, 37: 440-445.
28. Collaborative Group of the Spanish Society of Clinical Pharmacology: Comparative study of the efficacy of dipyrone, diclofenac sodium and pethidine in acute renal colic, Eur J Clin Pharmacol 1991,40: 543-546.
29. Muriel-Villoria C, Zungri-Telo E, Diaz-Curiel M, Fernandez-Guerrero M, Moreno J, Puerta J, Ortiz P: Comparison of the onset and duration of the analgesic effect of dipyrone, 1 or 2g, by the intramuscular or intravenous route in acute renal colic. Eur J Pharmacol, 1995; 48: 103-107.
30. Lloret J, Muňoz J, Monmany J, Puig X, Bonastre M, Brau J, Sola J, Domingo P, Jane F: Treatment of renal colic with dipyrone, Current Ther Res 1987, 42: 1119-1128.
31. Flanningan GM, Clifford RPC, Carver RA: An alternative to pethidine in ureteric colitis, Br J Urol, 1983, 55: 6-9.
32. Gaudio KM, Siegel NJ, Hayslett JP, Kashgarian M: Changes in renal blood flow and proximal tubular pressure during ureteral occlusion. Kidney Int 1978, 14: 724 abstr.
33. Bigal ME, Bordini CA, Tepper SJ, Speciali JG: Intravenous dipyrone in the acute treatment of migraine without aura and migraine with aura: a randomized, double blind, placebo kontrolled study. Headache 2002, 42:862-871.
34. Planas ME, Gay-Escoda C, Bagán JV, Santamaria J, Peňarrocha M, Donado M, Puerta JL: Oral metamizol (1g and 2g) versus ibuprofen and placebo in the treatment of lower third molar surgery pain: randomized double-blind multi-centre study. Eur J Clin Pharmacol 1998, 53:405-409.
35. Babej-Dőlle R, Freytag S, Eckmeyer J, Zerle G, Schnizel S, Schmieder G, Stankov G: Parenteral dipyrone versus diclofenac and placebo in patients with acute lumbago or sciatic pain: randomized observer-blind multicenter study. Int J Clin Pharmacol Ther 1994, 32: 204-209.
36. Rodriguez M, Barutell C, Rull M, Gálvez R, Pallarés J, Vidal F, Aljaga J, Moreno J, Puerta J, Ortiz P: Efficacy and tolerance of oral dipyrone versus oral morphine for cancer pain. Eur J Cancer 1994, 30A: 584-587.
37. Daftary SN, Mehta AC, Nanavati M: A controlled comparison od dipyrone and paracetamol in post-episiotomy pain. Curr Med Res Opinion 1979, 6: 6146-18.
38. Mukherjee S, Sood S: A controlled evaluation of orally administered aspirin, dipyrone and placebo in patients with post-operative pain. Curr Med Res Opinion 1980, 6: 619-623.
39. Steffen P, Kunz R, Schubmacher I, Georgieff M: Postopera-tive Analgesie nach laparoskopischen abdominellen Operationen. Chirurg 1997, 68: 806-810.
40. Montes A, Warner W, Puig M: Use of intravenous patient-controlled analgesia for the documentation of synergy between tramadol and metamizol. Br J Anaesth 2000, 85: 217-223.
41. Sittl R, Griessinger N, Märkert D: Lernprogramm Schmerz-therapie Universitaet Erlangen-Nürnberg, Erlangen 2002.
42. Andrade SE, Martinez C, Walker AM: Comparative safety evaluation of non-narcotic analgesics. J Clin Epidemiol 1998, 51: 1357-1365.
43. Kelly JP, Kaufman DW, Shapiro S: Risk of agranulocytosis and aplastic anemia in relation to the use of cardiovascular drugs. Clin Pharmacol Ther 1991; 49: 330-341.
44. Van der Klauw MM, Goudsmit R, Halie R, van´t Veer M, Herings RMC, Wilson JHP, Stricker BHCh: A population-based case-cohort study of drug associated agranulocytosis. Arch Intern Med 1999, 159: 369-374.
45. Martinez C: The adverse public health impact from short-term use of non-narcotic analgesics and non-steroidal antiinflammatory drugs from an epidemiologic perspective, Klin Pharmakol 1996, 7: 38-40.
46. Palmblad J, Papadaki H, Eliopoulos G: Acute and chronic neutropenias. What is new? J Intern Med 2001, 250: 476-491.
47. The Extra Pharmacopoeia Martindale. The Pharmaceutical Press, London 1952; 1: 832.
48. The Extra Pharmacopoeia Martindale. The Pharmaceutical Press, London 1958; 1: 28-29.
49. Sanchez S, Alarcon de la Lastra C, Ortiz P, Motilva V, Martin MJ: Gastrointestinal tolerability of metamizol, acetaminophen and diclofenac in subchronic treatment in rats. Digestive Dis Sci 2002, 42: 2791-2798.
50. Arellano F, Sacristan JA: Metamizole: reasessment of its therapeutic role, Eur J Clin Pharmacol 1990, 38: 617-619.

