© Borgis - Postępy Nauk Medycznych 11/2016, s. 831-835
*Szymon Kawecki1, Łukasz Nyk1, Przemysław Szostek1, Jakub Dobruch1, 2
Zwężenie moczowodu w następstwie guza włókniakowatego przestrzeni zaotrzewnowej
Ureteral stenosis following retroperitoneal desmoid tumor
1I Zespół Dydaktyki, Klinika Urologii, Centrum Medyczne Kształcenia Podyplomowego, Europejskie Centrum Zdrowia Otwock
Kierownik Kliniki: dr hab. med. Jakub Dobruch
2II Zespół Dydaktyki, Klinika Urologii, Centrum Medyczne Kształcenia Podyplomowego, Samodzielny Publiczny Szpital Kliniczny im. prof. W. Orłowskiego, Warszawa
Kierownik Kliniki: dr hab. med. Jakub Dobruch
Streszczenie
Włókniakowatość (łac. fibromatosis, ang. desmoid tumor) jest bardzo rzadko występującą chorobą, charakteryzującą się proliferacją tkanki łącznej włóknistej. Przedstawiamy przypadek 40-letniego mężczyznę, u którego na podstawie ultrasonografii przezpowłokowej wykonanej z powodu bólów w prawej okolicy lędźwiowej stwierdzono prawostronne wodonercze i poszerzenie lędźwiowego odcinka moczowodu. Tomografia komputerowa wykazała, że utrudnienie odpływu moczu z nerki było wywołane przez guz przestrzeni zaotrzewnowej obejmujący moczowód w okolicy stawu krzyżowo-biodrowego. Chorego poddano operacji polegającej na wycięciu guza, który rozlegle naciekał ścianę moczowodu oraz, szerząc się w kierunku dogłowowym, obejmował ścianę zagięcia dolnego dwunastnicy. Wobec nacieczenia moczowodu zdecydowano śródoperacynie o potrzebie usunięcia nerki wraz z całym moczowodem. Badanie histopatologiczne specymenu operacyjnego wykazało desmoid tumor.
Summary
Fibromatosis (desmoid tumor) is a rare disease that is characterized by proliferation of fibrous tissue. We present a case of 40 year-old man with whom on the basis of ultrasound made because of pain in the right lumbar area found right-sided hydronephrosis and extension of the lumbar ureter. Computed tomography showed that obstruction the outflow of urine from the kidney was caused by retroperitoneal tumor involving the ureter around the sacroiliac joint. Patient underwent surgery involving the excision of the tumor, which extensively infiltrated the wall of the ureter and, spreading towards the rostral covered the wall bends the lower duodenum. In view of the invasion of the ureter it was decided on the need to remove the kidney together with the whole ureter. Histopathological examination showed desmoid fibromatosis.

Opis przypadku
Mężczyzna 40-letni zgłosił się z powodu nawracających bólów w prawej okolicy lędźwiowej. Ultrasonografia przezpowłokowa (TAUS) ujawniła prawostronne wodonercze. Tomografia komputerowa (TK) (ryc. 1a, b) oraz rezonans magnetyczny (MRI) (ryc. 3a, b) potwierdziły jego istnienie i wykazały poszerzenie górnego odcinka prawego moczowodu sięgające do miejsca, w którym uwidoczniły lity guz o wymiarach 30 x 14 x 20 mm znajdujący się w przestrzeni zaotrzewnowej.

Ryc. 1a, b. Tomografia komputerowa: (a) przed podaniem kontrastu oraz (b) faza wydalnicza
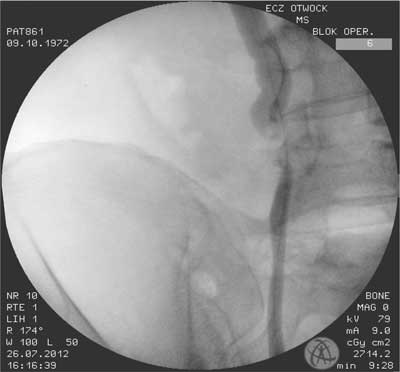
Ryc. 2. Pielografia wstępująca
Scyntygrafia wykazała, że czynność nerki prawej i nerki lewej stanowi odpowiednio 21 i 79% globalnej czynności wydzielniczej nerek. Badanie cytologiczne osadu moczu nie wykazało komórek nowotworowych.
Badanie przedmiotowe przeprowadzone w dniu przyjęcia chorego do szpitala nie ujawniło nieprawidłowości. Wykonano prawostronną ureteropielografię wstępującą (UPG) (ryc. 2) – badanie wykazało, że moczowód jest drożny do poziomu dolnego brzegu stawu krzyżowo biodrowego.
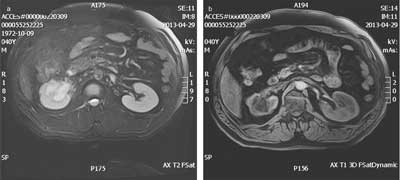
Ryc. 3a, b. Rezonans magnetyczny (MRI)
Wobec tego wprowadzono do moczowodu ureteroskop i pobrano wycinki ze ściany moczowodu w pobliżu zwężenia. Badanie histopatologiczne (H-P) wykazało: „prawidłowe utkanie błony śluzowej bez zmian nowotworowych” (badanie histopatologiczne nr 4070/2012). Ze względu na nasilenia bólów prawej nerki wprowadzono cewnik DJ do górnych dróg moczowych po tej stronie.
Po upływie około miesiąca chorego przyjęto do szpitala. Usunięto cewnik DJ i ponownie wykonano UPG i ureteroskopię (URS) – na poziomie nieco powyżej górnego brzegu stawu krzyżowo-biodrowego stwierdzono krytyczne zwężenie moczowodu spowodowane przez guz, który sprawiał wrażenie raka urotelialnego. Badanie H-P wycinków pobranych z guza wykazało: „ureteritis chronica non specifica activa; dysplasia reactiva minoris gradus urothelii superficialis” (badanie histopatologiczne nr 5133/1-3/2012).
Z wywiadu ustalono, że w przeszłości pacjent doznał poważnego urazu, który spowodował powstanie krwiaka w przestrzeni zaotrzewnowej po stronie prawej. Założywszy zatem, że guz zaotrzewnowy powodujący zwężenie moczowodu może być zwłóknieniem związanym z przebytym krwiakiem, zaniechano biopsji guza i poddano chorego operacji, której zakres miał być określony w zależności od zmian okołomoczowodowych, przy czym nie wyłączono konieczności wykonania nefroureterektomii. Badanie cytologiczne osadu moczu było prawidłowe.
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
29 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
69 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
129 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 78 zł
Piśmiennictwo
1. Sakorafas GH, Nissotakis Ch, Peros G: Review. Abdominal desmoid tumors. Surg Oncol 2007; 16: 131-142.
2. Peerlinck I, Amini-Nik S, Phillips R et al.: Therapeutic Potential of Replication-Selective Oncolytic Adenoviruses on Cells from Familial and Sporadic Desmoid Tumors. Clin Cancer Res 2008 Oct 1; 14(19): 6187-6192.
3. Khorsand J, Karakousis CP: Desmoid tumors and their management. Am J Surg 1985; 149: 215-218.
4. Paszkowski J, Drews M, Krokowicz P et al.: Fibroma desmoides managed in Third Chair and Department of Surgery of University School of Medical Sciences in Poznań. Współcz Onkol 1999; 2: 57-59.
5. Allen PW: The fibromatoses: a clinicopathologic classification based on 140 cases. Am J Surg Pathol 1977; 1: 255-270.
6. Kasper B, Ströbel P, Hohenbergera P: Desmoid Tumors: Clinical Features and Treatment Options for Advanced Disease. Oncologist 2011; 16(5): 682-693.
7. Reitamo JJ, Häyry P, Nykyri E, Saxèn E: The desmoid tumor. I. Incidence, sex-, age- and anatomical distribution in the Finnish population. Am J Clin Pathol 1982; 77(6): 665-673.
8. Suit HD: Radiation dose and response of desmoid tumors. Int J Radiat Oncol Biol Phys 1990; 19(1): 225-227.
9. Taylor LJ: Musculoaponeurotic fibromatosis. A report of 28 cases and review of the literature. Clin Orthop Relat Res 1987; 224: 294-302.
10. Nuyttens JJ, Rust PF, Thomas CR, Turrisi AT: Surgery versus radiation therapy for patients with aggressive fibromatosis or desmoid tumors: A comparative review of 22 articles. Cancer 2000; 88(7): 1517-1523.
11. Ferenc T, Sygut J, Kopczynski J et al.: Aggressive fibromatosis (desmoid tumors): definition, occurrence, pathology, diagnostic, problems, clinical behavior, genetic background. Polish Journal of Pathology 2006; 57: 5-15.
12. Lahat G, Nachmany I, Itzkowitz E et al.: Surgery for Sporadic Abdominal Desmoid Tumor: Is Low/No Recurrence an Achievable Goal? Isr Med Assoc J 2009; 11: 398-402.
13. Enzinger FM, Weiss SW: Fibromatosis. [In:] Enzinger FM, Weiss SW (eds.): Soft Tissue Tumors. MO: Mosby, St Lewis 1995: 201-229.
14. Latchford AR, Sturt NJ, Neale K et al.: A 10-year review of surgery for desmoid disease associated with familial adenomatous polyposis. Brtish Journal of Surgery 2006; 93: 1258-1264.
15. Lewis JJ, Boland PJ, Leung DHY et al.: The enigma of desmoid tumors. Annals of Surgery 1999; 229: 866-873.
16. Rodriguez-Bigas MA, Mahoney MC, Karakousis CP et al.: Desmoid tumors in patients with familial adenomatous polyposis. Cancer 1994; 74: 1270-1274.
17. Deyrup AT, Tretiakova M, Montag AG: Estrogen receptor-beta expression in extraabdominal fibromatosis: An analysis of 40 cases. Cancer 2006; 106: 208-213.
18. Wheeler M, Mercer D, Grant W et al.: Surgical Treatment of Intra-Abdominal Desmoid Tumors Resulting In Short Bowel Syndrome. Cancers (Basel) 2012 Mar; 4(1): 31-38.
19. Church J, Berk T, Boman BM et al.: Collaborative Group of the Americas on Inherited Colorectal Cancer. Staging intra-abdominal desmoid tumors in familial adenomatous polyposis: A search for a uniform approach to a troubling disease. Dis Colon Rectum 2005; 48: 1528-1534.
20. Melis M, Zager J, Sondak K: Multimodality management of desmoid tumors: How important is a negative surgical margin? J Surg Oncol 2008; 15: 594-602.



