© Borgis - Anestezjologia Intensywna Terapia 3/2007, s. 152-155
*Barbara Barteczko, Agnieszka Zamirowska, Andrzej Kübler
Stężenie glukozy we krwi chorych z ciężkš sepsš i wstrzšsem septycznym
Serum glucose concentration in septic shock
Klinika Anestezjologii i Intensywnej Terapii AM we Wrocławiu
kierownik: prof. dr hab. n. med. A. Kübler
Summary
Background.Hyperglycemia is a common finding in septic shock, and is associated with an increased morbidity. Strict glucose control in ITU patients has been recommended by several authors. The latest consensus conference recommended that glucose concentration in these patients should be kept within the normal range, and if possible, below 8.3 mmol l -1. Since an objective measure of hyperglycemia for assessing glucose control in acutely ill patients should reflect the magnitude and duration of hyperglycemia, the hyperglycemic index (HGI) was proposed, defined as the area under the curve above the upper limit of normal glucose level (6.0 mmol l -1), divided by the total length of stay.
Methods. This retrospective study included all patients with severe sepsis and septic shock, admitted to the ITU. Admission type, sex, age, APACHE II score and outcome were recorded. HGI, serum glucose (at admission, mean, maximal and minimal concentrations), and insulin requirement were noted for each patient.
Results. Sixty five septic shock patients (61% males, 39% females), aged 19-96 (mean 62) years, were enrolled in the study. The mortality rate was 62%. Median HGI was 2.75 mmol l -1 in survivors versus 3.94 mmol l -1 in non-survivors (p<0.05). Median daily insulin requirement was 50 IU in survivors, vs. 38 IU in non-survivors (p<0.05).
Conclusion. We conclude that HGI is a useful index of severity in septic shock. The highest mortality rate was associated with an increased HGI which may indicate inadequate control of serum glucose concentration in septic patients.

Sepsa to zespół uogólnionej reakcji zapalnej organizmu w odpowiedzi na zakażenie, które może prowadzić do postępujšcej niewydolno?ci wielu narzšdów, wstrzšsu i ?mierci. Pomimo coraz większej wiedzy na temat patomechanizmu oraz ustalonych wytycznych postępowania, ?miertelno?ć w sepsie sięga ponad 50%.
Podwyższone stężenie glukozy we krwi występuje często u chorych z ciężkš sepsš i wstrzšsem septycznym leczonych w oddziałach intensywnej terapii, którzy nie sš obcišżeni cukrzycš. W badaniach klinicznych, obejmujšcych chorych po zabiegach chirurgicznych wykazano znaczšce zwiększenie przeżywalno?ci w grupie, w której utrzymywano stężenie glukozy we krwi w granicach 4,4-6,1 mmol l-1, stosujšc cišgły wlew insuliny [1, 2].
W przebiegu ciężkiej sepsy i wstrzšsu septycznego dochodzi do złożonych zaburzeń gospodarki węglowodanowej. W stanie hipermetabolizmu ma miejsce przyspieszenie wytwarzania glukozy, wskutek podwyższonego stężenia hormonów antyregulacyjnych. Hiperglikemia jest czynnikiem niekorzystnym, działajšcym prozapalnie przez stymulację tworzenia się cytokin, wolnych rodników i lipidowych mediatorów reakcji zapalnej. Jednakże w trakcie przebiegu sepsy wysokiemu stężeniu glukozy w osoczu często towarzyszy wysokie stężenie insuliny. Takš sytuację można wytłumaczyć swoistš indukcjš czynno?ciowej oporno?ci na insulinę wskutek depresji mitochondrialnych enzymów glikolitycznych lub też działaniem na same receptory. Z kolei insulina, przełamujšc insulinooporno?ć podnosi zdolno?ć do wykorzystania glukozy przez komórkę, poprawiajšc tym samym stan energetyczny; ma również działanie przeciwzapalne przez hamowanie produkcji TNF, czšsteczek adhezyjnych, przylegania leukocytów do ?ródbłonka, hamowanie poniedokrwiennej apoptozy i zapobieganie niszczeniu tkanek.
Standardem postępowania w ciężkiej sepsie jest obecnie jak najszybsza likwidacja hiperglikemii oraz utrzymanie normoglikemii. Istotne znaczenie ma unikanie hipoglikemii. Międzynarodowe wytyczne leczenia ciężkiej sepsy zalecajš utrzymanie stężenia glukozy we krwi poniżej 8,3 mmol l-1 [3].
U chorych w OIT dla oceny stężenia glukozy można posłużyć się kilkoma wska?nikami: warto?ciš przy przyjęciu, warto?ciš ?redniš, najwyższš czy najniższš. Majš one tę wadę, że każdy z nich opiera się na pojedynczym pomiarze bšd? jest sumš poszczególnych, a nie odzwierciedla rzeczywistego stężenia glukozy pomiędzy pomiarami. W 2004 r. wykazano, że jednym z obiektywnych parametrów okre?lajšcych stężenia glukozy jest tzw. wska?nik hiperglikemiczny (HGI – Hyperglycemic Index) [4]. Pozwala on na ocenę porównawczš, ponieważ okre?la nierównomierny czas dystrybucji pomiędzy kolejnymi pomiarami stężenia glukozy. Nie jest fałszywie zaniżany w przypadku niskich warto?ci. HGI został zdefiniowany jako pole powierzchni poniżej krzywej stężenia glukozy, a powyżej prostej jej stężenia dopuszczalnego, podzielone przez czas badania [4] (ryc. 1).
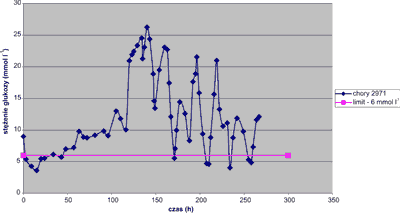
Ryc. 1. Przykładowe obliczanie wska?nika hiperglikemicznego (HGI) – warto?ć 5,64 mmol l-1.
Celem pracy była analiza zmian stężenia glukozy u chorych z rozpoznaniem ciężkiej sepsy i wstrzšsu septycznego oraz próba odpowiedzi na pytanie czy istnieje zależno?ć pomiędzy przebiegiem ciężkiej sepsy a jej stężeniem. Oceniono również ilo?ć insuliny potrzebnej do normalizacji stężenia glukozy.
Metodyka
Badaniom retrospektywnym poddano chorych z ciężkš sepsš i wstrzšsem septycznym, hospitalizowanych w Klinice Anestezjologii i Intensywnej Terapii AM we Wrocławiu. Chorzy byli leczeni standardowo zgodnie z wytycznymi. Dane dotyczšce leczenia były wprowadzane do rejestru Polskiej Grupy Roboczej ds. Sepsy www.sepsa.pl.
Wszystkie informacje dotyczšce chorych: wiek, płeć, przyczyna przyjęcia, punktacje w skalach oceny ciężko?ci stanu klinicznego uzyskano z zasobów archiwalnych szpitala.
Żywienie pozajelitowe stosowano w przypadkach przeciwwskazań do żywienia dojelitowego. Wlew insuliny otrzymywali chorzy z cukrzycš oraz ze stężeniem glukozy powyżej 10 mmol l-1.
Krew do badań była pobierana z centralnego dostępu dożylnego lub cewnika tętniczego. Stężenie glukozy oznaczano w surowicy krwi metodš enzymatycznš, za pomocš oksydazy glukozowej.
Rejestrowano stężenie glukozy przy przyjęciu do oddziału intensywnej terapii, jej najwyższe i najniższe stężenie w czasie leczenia oraz obliczano stężenie ?rednie (?rednia arytmetyczna wszystkich wykonanych pomiarów).
W celu okre?lenia HGI analizie poddano wszystkie wyniki pomiarów stężenia glukozy wykonane w czasie trwania sepsy oraz odpowiadajšcy im czas pobrania próbek. Następnie obliczono pole powierzchni pomiędzy wyznaczonš krzywš stężenia glukozy a dopuszczalnym jej stężeniem. Za dopuszczalnš warto?ć stężenia glukozy przyjęto 6 mmol l-1.
Uzyskane wyniki poddano analizie statystycznej za pomocš testu U Manna-Whitneya oraz t-Studenta. Jako poziom istotno?ci przyjęto p<0,05.
Wyniki
Badaniem objęto 65 chorych w ?rednim wieku 62 (19-96) lat; 61,5% stanowili mężczy?ni. Najczęstszym powodem przyjęcia do OIT były przyczyny niezabiegowe (47,7%) oraz nagłe operacje (36,9%). 22 chorych (33,84%) w momencie przyjęcia do OIT miało rozpoznanš cukrzycę typu 2.
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
29 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
69 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
129 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 78 zł
Piśmiennictwo
1. Van den Berghe G, Wouters PJ, Weekers F, Verwaest C, Schetz M, Vlassealaers D, Ferdinande P, Lauwers P, Bouillon R:Intensive insulin therapy in the critically ill patients. N Engl J Med 2001; 345: 1359-1367.
2. Krinsley JS:Effect of intensive glucose management protocol and the mortality in critically ill adult patients. Mayo Clin Proc 2004; 79; 992-1000.
3. Dellinger RP, Carlet JM, Masur H, Gerlach H, Calandra T, Cohen J, Gea-Banacloche J, Keh D, Marshall JC, Parker MM, Ramsay G, Zimmerman JL, Vincent JL, Levy MM:Surviving Sepsis Campaign guidelines for management of severe sepsis and septic sock. Crit Care Med 2004; 32: 858-873.
4. Volgezang M, van der Horst I, Nijesten WNM:Hyperglycemic index as tool to assess glucose control: a retospective study. Crit Care 2004; 8: 122-127.
5. Van de Berghe G, Wouters PJ, Bouillon R, Weekers F, Verwaest C, Schetz M, Vlassealaers D, Ferdinande P, Lauwers P:Outcome benefit of intensive insulin therapy in the critically ill: insulin dose versus glycemic control. Crit Care 2003; 31: 359-366.
6. Finney SJ, Zekveld C, Elia A, Evans TW:Glucose control and mortality in critically ill patients. JAMA 2003; 290: 2041-2047.
7. Van der Berghe G, Wouters PJ, Kasteloot K:Analysis of healthcare resource utilization with intensive insulin therapy in critically ill patients. Crit Care Med 2006; 34: 612-616.
8. Brunkhorst FM, Kuhnt E, Engel C:Intensive insulin therapy in patients with severe sepsis and septic shock is associated with an increased rate of hypoglicemia-results from a randomized multicenter study (VISEP). Infection 2005; 33 (Suppl. 1): 19-20.

