© Borgis - Postępy Fitoterapii 2/2011, s. 127-143
*Agnieszka Gryszczyńska1, Bogna Gryszczyńska2, Bogna Opala1
Karotenoidy. Naturalne źródła, biosynteza, wpływ na organizm ludzki
Carotenoids. natural sources, biosynthesis, influence on human body
1Instytut Włókien Naturalnych i Roślin Zielarskich w Poznaniu
Dyrektor Instytutu: prof. dr hab. Grzegorz Spychalski
2Uniwersytet Medyczny w Poznaniu, Katedra Chemii i Biochemii Klinicznej, Zakład Chemii Ogólnej
Kierownik Zakładu: prof. dr hab. Maria Iskra
Summary
Carotenoids belong to a group of compounds characterized by a general ability to protect the body against many serious diseases, such as impaired growth of children, the occurrence of many types of cancer, eye damage. Protective effect of carotenoids is associated mainly with the ability to scavenger free radicals and reactive oxygen species. These compounds are common in many plants, which are components of daily diet. Due to lack of synthesis of the resulting cycle of those compounds in animals, these substances are extremely important for the proper functioning of the body. Only consume large amount of plant in our daily diet can help protect the body against many irreversible consequences of disease.

Wstęp
W świadomości przeciętnego konsumenta roślinnych produktów spożywczych (zarówno warzyw, owoców, jak i suplementów diety) pod nazwą karotenoidy kryje się β-karoten, witamina A (retinol), z pewnością rzadziej likopen. Jednakże klasa tych związków jest bardzo liczna (zidentyfikowano już ponad 600 związków (1, 2)), a ich prozdrowotny wpływ na organizm ludzki jest nieograniczony. Takie właściwości posiadają m.in. α-karoten, luteina, kantaksantyna czy zeaksantyna. Najważniejszą cechą karotenoidów jest działanie antyoksydacyjne wobec reaktywnych form tlenu, jak i wolnych rodników. Dzięki tej właściwości karotenoidy chronią organizm przed wieloma ciężkimi, przewlekłymi chorobami. Częste stosowanie w diecie produktów bogatych w te związki skutecznie przeciwdziała rozwojowi nowotworów oraz miażdżycy.
Ogólna charakterystyka karotenoidów
Dotychczas zidentyfikowano ponad 600 karotenoidów, z czego 60 z nich występuje w codziennej diecie, a 20 można wykryć we krwi (3, 4). Karotenoidy to substancje nadające barwę od żółtej do czerwonej zarówno roślinom, jak i zwierzętom (2, 4-7). Aby karotenoidy dawały zabarwienie od żółtego po czerwone, muszą mieć w łańcuchu minimum 7 wiązań podwójnych. Takie substancje jak fitoen czy fitofluen, mające jedynie 3 i 5 wiązań podwójnych, są bezbarwne. W połączeniu z niektórymi białkami (zwanych karotenoproteinami) mogą przyjmować inne zabarwienie – od niebieskiego do purpurowego, czy zielonego. Tego typu kompleksy karotenoidów można odnaleźć u morskich bezkręgowców (8). To właśnie karotenoidy nadają piękną barwę piórom, łuskom i skórze zwierząt. W przeciwieństwie do roślin, zwierzęta nie potrafią samodzielnie syntetyzować ich na drodze procesów biochemicznych. Dlatego też substancje te muszą być dostarczane do organizmu wraz z dietą (5, 7, 9).
Najpopularniejszymi karotenoidami występującymi w diecie są: α- i β-karoten, β-kryptoksantyna, luteina, likopen i zeaksantyna. Karotenoidy wchłaniane są przez jelita do krwi, która za pomocą lipoprotein, transportuje je do różnych tkanek w organizmie. Można odnaleźć badania, które mówią, że receptory zmiatające klasy B typu 1 (SR-B1) oraz różnicowania białka błonowego (CD 36), odpowiedzialne za transport cholesterolu, ułatwiają wchłanianie karotenoidów przez jelita. Receptory transportujące mogą również ułatwić wchłanianie karotenoidów poprzez warstwę naskórka. Ze względu na powszechność występowania tkanki tłuszczowej w organizmach zwierzęcych, jest ona głównym miejscem kumulacji dużej ilości karotenoidów. Karotenoidy obecne w tkance ludzkiej uważane są za substancje markerowe stosowanej diety. Ze względu na większą stabilność tkanki tłuszczowej, obecne w niej karotenoidy są łatwiejsze do wykrycia w porównaniu do karotenoidów we krwi, gdzie szybkość ich połowicznego rozpadu jest wyższa (10). Jedną z ważniejszych właściwości karotenoidów obecnych w organizmach zwierzęcych jest fakt, iż są one miernikiem stanu zdrowia danego osobnika. Poza prozdrowotnym działaniem na organizmy, odgrywają one ważną rolę w wabieniu osobników płci przeciwnej (5, 7).
Karotenoidy rozpuszczają się w tłuszczach. Proces ten ma wpływ na wiele biologicznych procesów, takich jak fotosynteza, zdolność widzenia, czy zmiatanie wolnych rodników i tlenu singletowego (1, 7, 11, 12).
Budowa
Patrząc na strukturę chemiczną tych związków widać układ 11 sprzężonych wiązań podwójnych (ryc. 1), dzięki którym można je zaklasyfikować do grupy poliizoprenoidów (3, 4, 12, 13). Związki te są nierozpuszczalne w wodzie, natomiast bardzo dobrze rozpuszczają się w tłuszczach, z którymi często tworzą estry. Ze względu na różnice w łańcuchu poliizoprenoidowym, karotenoidy można podzielić na 2 grupy. Pierwsza to związki zawierające jedynie atomy węgla i wodoru o wzorze sumarycznym C40H56, najczęściej to izomery all-trans, które są termodynamicznie bardziej stabilne (3, 13). Zmiana izomerii na cis-trans jest możliwa w podwyższonej temperaturze i/lub w obecności intensywnego promieniowania. Izomery cis można odnaleźć w warzywach i owocach, są to też produkty przemiany metabolicznej pożywienia (11). Ze względu na taką budowę karotenoidy są substancjami mało polarnymi, absorbują promieniowanie o wyższej długości fali (2). Do pierwszej grupy karotenoidów zalicza się również związki, które mają krótsze łańcuchy węglowe, ale wyposażone w centralny fragment karotenu z 4 grupami metylowymi (np. biksyna) (ryc. 2) (3).
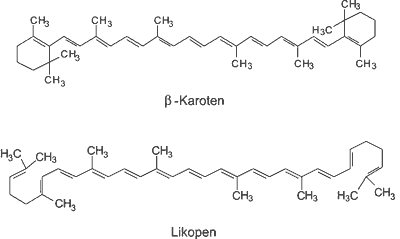
Ryc. 1. Struktura chemiczna β-karotenu i likopenu.
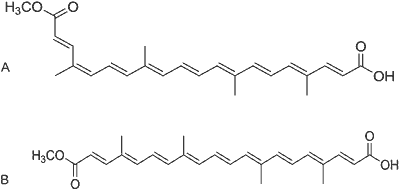
Ryc. 2. Biksyna: A – izomer cis, B – izomer trans.
Druga grupa związków zawiera minimum jeden atom tlenu, znajdujący się np. w grupie hydroksylowej, karbonylowej, karboksylowej czy hydroksymetylowej. Tę drugą grupę karotenoidów określa się mianem ksantofili (ryc. 3). Ksantofile są szeroko występującą w naturze grupą związków, wykazującą podobieństwo zarówno chemiczne, biochemiczne, jak również fizykochemiczne (3, 13). Ksantofile są to związki bardziej polarne, absorbujące promieniowanie o niższych długościach fali niż większość karotenoidów (2).
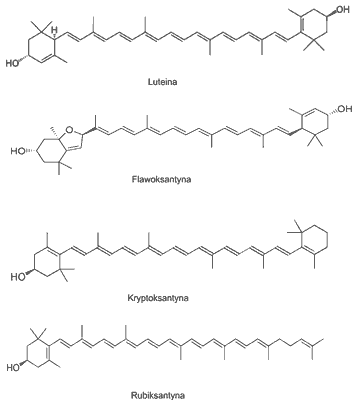
Ryc. 3. Budowa chemiczna związków ksantofilowych.
Biosynteza karotenoidów
Naukowcy od lat 60. XX wieku prowadzili liczne eksperymenty, aby zrozumieć biochemiczne procesy prowadzące do powstania cząsteczek karotenoidów (14). Grupa karotenoidów C40 jest najbardziej zróżnicowana i rozpowszechniona. Różnego rodzaju związki z tej grupy można znaleźć w wielu organizmach, tj. bakterie, archebakterie, algi, grzyby, czy rośliny. Związki te syntetyzowane są w dwojaki sposób. Duża większość, bo aż 95% z nich, powstaje w wyniku procesu kondensacji 2 cząsteczek difosforanu digeranylu (GGPP, C20PP), konsekwencją czego jest symetryczny szkielet fitoenu C40 (1). Proces ten zachodzi w obecności syntazy fitoenu (PSY). Powstały w ten sposób fitoen ulega 4-stopniowej przemianie w reakcjach katalizowanych oksydazami, czego następstwem jest powstanie cząsteczki likopenu. W wyniku reakcji cyklizacji powstaje α-karoten i β-karoten. W kolejnych etapach β-karoten w reakcji hydroksylacji przekształcany jest w zeaksantynę, natomiast α-karoten – w luteinę. Enzym epoksydaza zeaksantynowa w 2-stopniowej reakcji przekształca zeaksantynę w anteraksantynę i wiolaksantynę. Finalnie u roślin wyższych wiolaksantyna przekształcana jest za sprawą syntazy neoksantynowej w neoksantynę. Przy udziale dużej ilości światła wiolaksantyna może ulec powrotnej przemianie w anteraksantynę za sprawą aktywnej deepoksydazy wiolaksantynowej (VDE).
Przemiana wiolaksantyny i zeaksantyny nazywana jest cyklem ksantofilowym (ryc. 4). Jest ona mechanizmem przystosowawczym rośliny do zmian (w szczególności intensywności światła) zachodzących w otoczeniu. Przy częściowym niedoborze światła lub w ciemności przemiana zeaksantyny do wiolaksantyny jest faworyzowana, konsekwencją czego jest wysoka zawartość wiolaksantyny. Natomiast gdy roślina przebywa w silnie nasłonecznionym miejscu, wiolaksantyna przekształcana jest w zeaksantynę, zwiększając jej zawartość w tkankach. Stosunek zeaksantyny i wiolaksantyny jest miarą stresu, wywołanego np. zmianą temperatury otoczenia, czy dostępności wody (14). Oprócz nasłonecznienia i temperatury, ważnym czynnikiem wpływającym bezpośrednio na skład chemiczny liści jest napromieniowanie.

Ryc. 4. Cykl ksantofilowy biosyntezy karotenoidów.
Dla przykładu, ważnym parametrem fizycznym dla procesu biosyntezy likopenu w pomidorach jest temperatura. Zaobserwowano wzrost zawartości tej substancji w temperaturze 12-21°C, natomiast powyżej 30°C następowało spowolnienie tego procesu (2).
Druga grupa karotenoidów powstaje na drodze syntezy 2 cząsteczek difosforanu farnezylu (FPP, C15PP). W wyniku tego procesu tworzy się łańcuch zawierający 30 atomów węgla. Powszechność tej grupy cząsteczek ogranicza się do bakterii z rodziny Staphylococcus, Streptococcus, Methylobacterium oraz Heliobacterium (1).
Charakterystyka podstawowych karotenoidów
Karotenoidy od wielu lat były interesującym tematem dla naukowców. Prowadzone liczne eksperymenty miały nie tylko na celu ich identyfikację, ale również, a może przede wszystkim, wyjaśnienie ich enzymatycznego i genetycznego wpływu na organizmy. U roślin karotenoidy często znajdują się w niefotosyntetyzujących organach, tj. owoce, nasiona czy kwiaty. Są to najczęściej produkty drugorzędowych reakcji metabolicznych, czyli oksydacji, rozpadu łańcucha polienowego i izomeryzacji (Z/E i cis-trans) (15).
Karotenoidy pełnią bardzo ważne funkcje w świecie roślin. Odpowiadają za stabilność błon lipidowych, biorą udział w gromadzeniu światła w procesie fotosyntezy, jak również ochronie przed procesem fotooksydacji wywołanym przez reaktywne formy tlenu powstające podczas wzbudzenia chlorofilu w procesie fotosyntezy (2, 14).
Działanie przeciwutleniające karotenoidów na błony lipidowe zależy od ich orientacji, lokalizacji oraz organizacji w błonach. Polarne i niepolarne karotenoidy w różny sposób oddziaływują na strukturę i fizjologię tkanek. Na przykład astaksantyna, będąca substancją polarną, ogranicza peroksydację lipidów poprzez utrzymywanie sztywnej struktury błony (11). Ochronne działanie karotenoidów na roślinę może być zaburzone przez mutacje genetyczne, czy stosowanie środków ochrony roślin (w szczególności herbicydu – norflurazonu) (14). Działanie przeciwrodnikowe karotenoidów opiera się na dwóch mechanizmach; pierwszy polega na przenoszeniu elektronów (NO2?, CCl3?, Br2?), drugi – na tworzeniu adduktów z rodnikami (nadtlenkowymi oraz tiolowymi). Są jednak takie rodniki, które do neutralizacji przez karotenoidy wymagają zajścia obu tych procesów. Do tej grupy należą rodniki sulfonowe oraz fenoksylowe (3).
Karotenoidy charakteryzują się wysoką aktywnością wobec reaktywnych form tlenu, jak i wolnych rodników (2, 6). Porównując β-karoten z innymi antyoksydantami, witaminą C i E, wykazuje on wyższą aktywność antyoksydacyjną wobec tlenu singletowego, powstającego w procesie fotosyntezy (16). β-karoten hamuje fazę początkową, jak również etap propagacji peroksydacji lipoprotein (3). Równoczesne stosowanie β-karotenu oraz witamin C i E powoduje cofanie się miażdżycy. α-Karoten chroni komórki przed nadmiernym rozrostem. Stosowanie diety bogatej w luteinę, czy zeaksantynę, zapobiega powstaniu zaćmy i zwyrodnieniu plamki żółtej. Prowadzone są badania nad wykorzystaniem syntetycznego β-karotenu w walce ze stanem przedrakowym jamy ustnej, płuc i szyjki macicy.
Inny karotenoid – likopen jest dwukrotnie efektywniejszy w walce z rodnikiem tlenku azotu NO2? odpowiedzialnym za uszkodzenia limfocytów. Badania potwierdzają jego zapobiegawcze właściwości wobec raka prostaty i szyjki macicy (16). Potwierdzono również skuteczne działanie ochronne β-karotenu na skórę u pacjentów chorych na protoporfirię erytropoetyczną, którzy są nadwrażliwi na światło słoneczne. Badania kontrolne nad karotenoidami, a w szczególności nad β-karotenem, potwierdzają jego działanie zapobiegające oparzeniom skóry u osób zdrowych, choć jego współczynnik ochrony przeciwsłonecznej jest stosunkowo niski (SPF ≈ 2). Dodatkowo meta-analiza suplementacji β-karotenem w porównaniu z placebo również wskazuje na ochronę przed powstaniem poparzeń słonecznych. Wiąże się to z właściwościami zmiatającymi wolne rodniki i reaktywne formy tlenu, powstające w wyniku ekspozycji skóry na promieniowanie UVA.
Karotenoidy w ludzkim organizmie magazynowane są przede wszystkim w wątrobie, nadnerczach i tkance tłuszczowej. Liczne eksperymenty mówią o zależności wchłaniania karotenoidów od ilości lipoprotein o niskiej gęstości (LDL), receptorów klasy B typu 1 (SR-B1) i degradacji lipoprotein przez enzymy. Można również odnaleźć badania, które wskazują na preferencję tkanek do przyswajania poszczególnych izomerów geometrycznych karotenoidów (10).
Niektóre karotenoidy, oprócz prowitaminy A, wzmacniają odporność immunologiczną organizmu. Część z nich bierze udział w komunikacji międzykomórkowej. Badania epidemiologiczne wskazują na korzystny związek pomiędzy spożyciem dużych ilości warzyw, a zmniejszającym się ryzykiem wystąpienia chorób przewlekłych tj. nowotwory, czy choroby układu krążenia oraz związanym z procesem starzenia się zwyrodnieniem plamki żółtej (3, 4, 6, 13, 17, 18). Potwierdzono także spowalniający wpływ karotenoidów na proliferację komórek nowotworowych (6, 17, 19).
Prawidłowe stężenie β-karotenu we krwi na czczo wynosi 0,9-5,58 μmol/L (50-300 mg/dL) (20).
Karotenoidy pochodzenia roślinnego
Likopen występuje w pożywieniu w postaci izomeru cis. Postać ta sprzyja wchłanianiu przez układ pokarmowy, ponieważ nie wykazuje tendencji do krystalizacji i agregacji. Izomery cis ksantofili występują we krwi i tkankach człowieka. Na agregację trans-ksantofili wpływa płynność warstwy lipidowej (11).
Zidentyfikowane (15) w papryce kapsantyna i kapsarubina wykazują bardzo istotną dla organizmu aktywność neutralizującą tlen singletowy, jak również inhibicyjny wpływ na peroksydację lipidów. Dodatkowo mogą być stosowane jako substancje przeciwdziałające rozwojowi nowotworów (15).
Astaksantyna (9) jest karotenoidem występującym dość często w organizmach morskich, np. w łososiu. Należy ona do grupy karotenoidów charakteryzujących się niską zdolnością redukującą. W jednorodnych roztworach jest bardzo słabym antyoksydantem. Występując w liposomach, jako składnik błon komórkowych, wykazuje tam lepsze właściwości przeciwutleniające niż inne karotenoidy (9).
W piśmiennictwie można znaleźć również informacje o profilu karotenoidowym winogron (21). 85% wszystkich zawartych w winogronach karotenoidów to β-karoten i luteina (ich zawartość wyrażana jest w mg/kg). Pozostałe karotenoidy, tj. neochrom, neoksantyna, wiolaksantyna, luteoksantyna, flawoksantyna, 5,6-epoksyd luteiny, zeaksantyna, cis-izomery luteiny i β-karotenu, występują na poziomie μg/kg. Podejrzewa się, że β-karoten, neoksantyna, luteina i zeaksantyna odpowiadają za aromat winogron, jak również prawdopodobnie są one substratami dla reakcji otrzymywania norizoprenoidów. Na profil karotenoidowy w winogronach, podobnie jak u innych roślin, ma wpływ wiele czynników zewnętrznych; odmiana, warunki klimatyczne, skład gleby, stadium rozwoju, czy nawet sposób uprawy. Najwyższą zawartość tej grupy związków obserwuje się w winogronach rosnących w gorących regionach świata, a najwyższe ich stężenie znajduje się w skórce (2-3 razy wyższe niż w miąższu owoców).
Wysokie stężenie wiolaksantyny, 5,6-epoksydu luteiny i luteoksantyny obserwuje się w owocach zawierających w 1 kg 160 g cukru, natomiast neochrom jest charakterystyczną substancją dla niedojrzałych owoców. Prowadzono wiele badań nad karotenoidami w różnych stadiach rozwoju owoców. Karotenoidy są intensywnie syntetyzowane w pierwszych etapach tworzenia się owoców, a po dojrzaniu ich stężenie wyraźnie spada. Liczne badania potwierdzają drastyczny spadek zawartości β-karotenu, luteiny, flawoksantyny i neoksantyny. Prawdopodobnie jest to związane z degradacją enzymatyczną lub procesami biokonwersji tych związków, np. w wiolaksantynę podczas aktywacji cyklu ksantofilowego pod koniec dojrzewania owocu (21).
Skład poszczególnych karotenoidów w roślinach zależy od gatunku, odmiany, miejsca wzrostu, nasłonecznienia i okresu, w którym zostały zebrane owoce (3, 21). Do roślin bogatych w karotenoidy należą jarmuż, szpinak, czerwona papryka, pomidory, marchew. Najczęściej w roślinach dominującym związkiem jest luteina, a więc ksantofil. Papryka czerwona bogata jest w kapsantynę, kapsorubinę, kapsoluteinę i β-karoten. Natomiast pomidory są źródłem likopenu, który wykryto również w małych ilościach w marchwi i czerwonej papryce. 95% likopenu zawartego w pomidorach występuje jako izomer trans, natomiast zawartość izomeru cis nie przekracza 10%. Najpowszechniejszymi ksantofilami w roślinach są: wiolaksantyna, neoksantyna, β-kryptoksantyna. W szpinaku, czerwonej papryce, ziemniakach i białej kapuście można znaleźć zeaksantynę.
Na zawartość karotenoidów w spożywanych owocach i warzywach ma też wpływ ich przyrządzenie, czyli usuwanie zewnętrznych liści czy skóry. Usunięcie zewnętrznej warstwy liści z białej kapusty pozbawia ją dużej ilości luteiny i β-karotenu (liście zewnętrzne bowiem zawierają ok. 150-razy więcej luteiny i ok. 200 razy więcej β-karotenu niż wewnętrzne liście). Natomiast skóra pomidora zawiera ok. 5 razy więcej likopenu niż miąższ. Na zawartość likopenu w pomidorach ma wpływ temperatura wzrostu owoców. Przyjmuje się, że optymalna temperatura wzrostu owoców to 16-26°C, natomiast w temperaturze powyżej 35°C likopen przekształcany jest w β-karoten (3).
W tabeli 1 umieszczono zawartość poszczególnych karotenoidów w popularnych warzywach, a w tabeli 2 w popularnych owocach i innych produktach spożywczych.
Tabela 1. Zestawienie zawartości karotenoidów w jadalnych częściach popularnych warzyw (wg 3).
| Warzywo |
Zawartość (mg/100 g części jadalnych) |
| α-karoten |
β-karoten |
likopen |
luteina +zeaksantyna |
| Brokuły | 0,001-0,073 |
0,28-2,42 |
– |
0,78-3,50 |
| Brukselka | 0,004-0,011 |
0,43-1,02 |
– |
0,92-1,59 |
| Kapusta biała | 0-0,002 |
0,01-0,41 |
– |
0,084-0,45 |
| Kapusta czerwona | ilości śladowe |
0,015-0,05 |
– |
0,026-0,15 |
| Jarmuż | 0-0,15 |
2,84-43,80 |
– |
3,04-39,55 |
| Kalafior | – |
0,002-0,08 |
– |
0,015-0,033 |
| Szpinak | 0-0,09 |
3,25-5,60 |
– |
4,40-11,94 |
| Sałata | 0,04 |
0,98-1,55 |
|
1,35-2,92 |
| Marchew | 0,53-4,96 |
6,15-9,02 |
0,015 |
0,30-0,51 |
| Seler | – |
0,15-2,90 |
– |
0,23-7,20 |
| Cebula żółta | – |
0,002-0,007 |
– |
0,015-0,016 |
| Por | – |
1,00-3,19 |
– |
1,90-3,68 |
| Ogórek | ilości śladowe |
0,13-0,27 |
– |
0,47-0,84 |
| Pomidory | 0,11-0,15 |
0,21-0,89 |
3,10-11,44 |
0,076-0,43 |
| Pomidory cherry | – |
0,92-1,05 |
7,20-10,80 |
– |
| Papryka czerwona | 0,059-0,51 |
2,38-3,25 |
0,13 |
2,20 |
| Papryka żółta | 0,092 |
0,12-0,27 |
– |
0,77 |
| Papryka zielona | 0,010-0,022 |
0,10-0,25 |
– |
0,41-0,77 |
| Ziemniaki | – |
0,003-0,006 |
– |
0,013-0,116 |
Tabela 2. Zestawienie zawartości witaminy A i β-karotenu w popularnych produktach spożywczych (wg 16).
| Produkt |
Zawartość witaminy A (mg/100 g części jadalnych) |
Zawartość β-karotenu (mg/100 g części jadalnych) |
| Tran | 60,000 |
|
| Wątroba wołowa | 14,400 |
0,950 |
| Wątroba wieprzowa | 13,000 |
0,011 |
| Masło ekstra | 0,814 |
0,380 |
| Ser twarogowy tłusty | 0,083 |
0,062 |
| Jajka kurze całe | 0,375 |
0,281 |
| Makrela wędzona | 0,054 |
– |
| Mleko spożywcze (2%) | 0,025 |
0,012 |
| Jabłka | 0,004 |
0,024 |
| Ser gouda tłusty | 0,276 |
0,207 |
Śliwki suszone
z pestką | 0,154 |
0,925 |
| Dynia | 0,496 |
2,974 |
| Kurki | – |
0,800 |
| Brzoskwinie | 0,099 |
0,595 |
| Morele | 0,254 |
1,523 |
| Fasola szparagowa | 0,063 |
0,378 |
| Śliwki | 0,049 |
0,295 |
| Jeżyny | – |
0,300 |
| Groszek zielony | 0,068 |
0,408 |
Witamina A
Jedną z substancji, z których może powstać prowitamina A jest β-karoten (2, 17). Cecha ta jest bezpośrednio związana ze strukturą danej cząsteczki karotenoidu. Podstawowym warunkiem, by dana substancja mogła być prekursorem witaminy A (retinolu), jest obecność niepodstawionego pierścienia β. Inne karotenoidy, które nie mają takiego pierścienia, bądź jest on podstawiony przez grupę hydroksylową, epoksydową lub karbonylową, nie mogą być substratami do syntezy prowitaminy A (2).
Odkrycie retinolu datuje się na 1915 rok, choć objawy hipowitaminozy i awitaminozy znane były już w starożytnym Egipcie. Prawidłowe stężenie witaminy A w organizmie chroni przed wieloma poważnymi chorobami, choć do dnia dzisiejszego nie odkryto jej funkcji biologicznej. Ze względu na budowę retinolu, w składzie którego znajdują się liczne wiązania podwójne, czego konsekwencją są różnego rodzaju izomery geometryczne, można mówić o ponad 1000 związkach, z czego biologicznie czynnych jest jedynie 50. Najważniejszym z nich jest β-karoten.
Witamina A odpowiedzialna jest za widzenie, bierze udział w procesach zachodzących w siatkówce za sprawą rodopsyny, czyli purpury wzrokowej. Odgrywa również bardzo ważną rolę w procesie rozrostu tkanki kostnej oraz komórek nabłonkowych, w szczególności błony śluzowej jamy ustnej, przewodu pokarmowego, układu moczowego, dróg oddechowych, jak również narządu wzroku. Awitaminoza prowadzi do zaburzenia wzrostu u dzieci, wysychania i rogowacenia naskórka, rogowacenia części nerek i powstawania kamieni, kurzej ślepoty, wysychania rogówki i jej rozmiękczania, czego konsekwencją może być całkowita ślepota. Szczególnie wrażliwe są tkanki płucne wcześniaków. Najczęściej niedobór witaminy A diagnozuje się u dzieci poniżej 5. roku życia. Objawia się on biegunką oraz chorobami układu oddechowego. Inne badania donoszą, że awitaminoza prowadzi do niedrożności przewodów gruczołowych i atrofii gruczołów, zaburzenia spermatogenezy, zapłodnienia i rozwoju płodu.
Witamina A jest magazynowana w wątrobie (96%) w postaci estrów, w szczególności kwasu palmitynowego. Pozostałe 4% to retinol. Należy podkreślić, że nadmierne spożywanie witaminy A działa toksycznie na organizm, a nadmierna, niezwiązana przez białka ilość retinolu występująca w postaci wolnej we krwi, tkankach, jak również w innych narządach, prowadzi do hiperwitaminozy. Jedynie 80% spożywanego retinolu ulega wchłanianiu, natomiast pozostałe 20% wydalane jest z organizmu w przeciągu 24-48 godzin. Karotenoidy wchłaniane są dużo gorzej niż witamina A, bo zaledwie w 30%. Proces ten uzależniony jest od diety, źródła i rodzaju białka, żelaza, cynku, tłuszczów, jak również procesów metabolizmu pożywienia (16). Pochodna witaminy A – kwas retinowy – odgrywa bardzo ważną rolę w organizmie. Aktywuje on receptory jądrowe czynników transkrypcyjnych aktywowanych przez ligandy. Około 500 genów w sposób pośredni lub bezpośredni regulowanych jest przez ten kwas (3).
Inne karotenoidy
Liao i wsp. (3) prowadzili badania nad karotenoidami, w szczególności nad β-karotenem oraz innymi substancjami pochodzenia roślinnego, wykazującymi silne właściwości antyoksydacyjne, tj. (+)-katechina, (-)-epikatechina. Z badań wynika, że połączenie tych grup związków wzmaga ochronę przed peroksydacją lipidów błon erytrocytalnych katalizowanych jonami Fe+2. Natomiast z badań nad samymi karotenoidami można wywnioskować zwiększenie ochronnego działania na błony lipidowe za sprawą likopenu i luteiny (3).
Ren i Zhang (19) prowadzili badania nad izolacją i identyfikacją żółtych barwników z rdestnicy kędzierzawej (Potamogeton cripuds L.). Ekstrakcję z surowca prowadzono za pomocą mieszaniny acetonu i eteru naftowego (1:1). Tak uzyskany ekstrakt poddawano kolejnym procesom mającym na celu izolację karotenoidów. Identyfikację poszczególnych związków potwierdzono za pomocą chromatografii cieczowej (TLC, HPLC) i spektrometrii mas. Dzięki temu potwierdzono obecność 231 μg/g karotenoidów w przeliczeniu na wysuszoną substancję roślinną. Zidentyfikowano w ten sposób neoksantynę, wiolaksantynę, luteinę, rodoksantynę oraz β-karoten (19).
Simkin i wsp. (14) prowadzili badania nad wyjaśnieniem genetycznych procesów prowadzących do powstania karotenoidów w popularnych gatunkach kawy. Przebadali oni młode liście, gałęzie i kwiaty Coffea canephora i Coffea arabica. Badania koncentrowały się na 8 genach kodujących biosyntezę karotenoidów: PSY, PDS, ZDS, PTOX, LCY-E, CRTR-B, ZEP, VDE oraz 2 genach odpowiedzialnych za formowanie różnych apokarotenoidów: CCD1 oraz NCED3. Dla każdego genu określone zostały filogenetyczne powiązania sekwencji cDNA kawy, opierając się na blisko spokrewnionych genetycznie gatunkach roślin (pomidorach, ziemniakach, tytoniu oraz pieprzu). Sekwencja aminokwasów CcCRTR-B, a w szczególności gen CRTR-B, obecna jest we wszystkich gatunkach roślin. Gen ten odpowiedzialny jest za przekształcanie β-karotenu w zeaksantynę poprzez dwukrotną hydroksylację kryptoksantyny. Umieszczenie białka rekombinującego CcCRTR-B w komórkach odpowiadających produkcji zeaksantyny, nie spowodowało żadnych zmian w ich zabarwieniu. Jednakże gromadzenie β-karotenu indukowane CcCRTR-B spowodowało zmianę zabarwienia z pomarańczowo-żółtego na jasno żółte, powodując powstanie β-kryptoksantyny oraz zeaksantyny.
Badania nad CcCRTR-B potwierdziły aktywność genu CRTR-B w przemianach biochemicznych β-karotenu. W liściach większości gatunków roślin występuje β-karoten oraz luteina, ale nie α-karoten. α-Karoten jest substancją charakterystyczną dla marchwi. W badaniach prowadzonych nad liśćmi Coffea canephora i Coffea arabica wykryto wysoką zawartość tej postaci karotenu, w szczególności w C. arabica. Natomiast w drugim gatunku zaobserwowano wysoką zawartość luteiny, co pozwala wysunąć hipotezę o dwóch różnych procesach syntezy tych związków. Liście kawy zawierały 12-13% β-karotenu, w przeciwieństwie do pomidorów, tytoniu czy rzodkiewnika (26-28%). Wysunięto więc hipotezę, że niska zawartość β-karotenu jest ściśle powiązana z odpowiednimi warunkami panującymi podczas przekształcenia α-karotenu w β-karoten w obecności kompleksu PSII. Biosynteza karotenoidów może również być ściśle powiązana ze stresem wywołanym brakiem wody. Wyżej wymienione geny badano również w stanie stresu. Poziom transkrypcji tych genów w stanie stresu był wyższy niż w liściach roślin próby odniesienia. I tak np. poziom transkrypcji genu PSY był 10-krotnie wyższy. Prawdopodobnie odpowiada on za kontrolę pierwszego etapu przemiany, dlatego też jego poziom może być wyższy w szybko rozwijających się liściach. PTOX odpowiada za desaturację fitoenów oraz może być powiązany z poziomem PDS. Poziom tych 2 genów po trzytygodniowym pozbawieniu rośliny wody wzrósł 3-krotnie, choć ich poziom spadł nieznacznie w trakcie eksperymentu. Poziom transkrypcji LCY-E jest niższy przy braku wody. Zachowanie to wskazywać by mogło na udział tego genu w metabolizmie luteiny do ksantofili.
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
24 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
59 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
119 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 28 zł
Piśmiennictwo
1. Tobias AV, Arnold FH. Biosynthesis of novel carotenoid families based on unnatural carbon backbones: A model for diversification of natural product pathways. BBA 2006; 1761:235-46. 2. Andersson SC. Carotenoids, tocochromanols and chlorophylls in sea buckthorn berries (Hippophae rhamnoides) and rose hips (Rosa sp.). Doctoral Thesis Swedish University of Agricultural Sciences, Alnarp 2009; 15-20. 3. Grajek W. Przeciwutleniacze w żywności. Aspekty zdrowotne, technologiczne, molekularne i analityczne. Wyd Nauk-Techn, Warszawa 2007; 97:172-176,344,431. 4. Fratianni A, Cinquanta L, Panfili G. Degradation of carotenoids in orange juice during microwave heating. LWT-Food Sci Technol 2010; 43:867-71. 5. Juola FA, McGraw K. Dearborn DC. Carotenoids and throat pouch coloration in the great frigatebird (Fregata minor). Comp Biochem Physiol 2008; 149:370-7. 6. Graça-Dias M, Cam?es MFGFC, Oliveria L. Carotenoids in traditional Portuguese fruits and vegetables. Food Chem 2009; 113:808-15. 7. Geens A, Dauwe T, Eens M. Does anthropogenic metal pollution affect carotenoid colouration, antioxidative capacity and physiological condition of great tits (Parus major)? Comp Biochem Physiol Pt C 2009; 150:155-63. 8. Meléndez-Martínez AJ, Escudero-Gilete ML, Vicario IM i wsp. Study of the influence of carotenoid structure and individual carotenoids in the qualitative and quantitative attributes of orange juice color. Food Res Int 2010; 43:1289-96. 9. Liang J, Tian YX, Yang F i wsp. Antioxidant synergism between carotenoids in membranes. Astaxanthin as a radical transfer bridge. Food Chem 2009; 115:1437-42. 10. Scarno S, Cartmel B, Lin H i wsp. Significant correlations of dermal total carotenoids and dermal lycopene with their respective plasma levels in healthy adults. Arch Biochem Biophys 2010; 504:34-9. 11. Widomska J, Kostecka-Gugała A, Latowski D i wsp. Calorimetric studies of the effect of cis-carotenoids on the thermotropic phase behavior of phosphatidylcholine bilayers. Biophys Chem 2009; 140:108-14. 12. Odriozola-Serrano I, Soliva-Fortuny R, Hernández-Jover T i wsp. Carotenoid and phenolic profile of tomato juices processed by high intensity pulsed electric fields compared with conventional thermal treatments. Food Chem 2009; 112:258-66. 13. Rodríguez-Bernaldo, de Quirós A, Costa HS. Analysis of carotenoids in vegetable and plasma samples: a review. J Food Compos Anal 2006; 19:97-111. 14. Simkin AJ, Moreau H, Kuntz M i wsp. An investigation of carotenoids biosynthesis in Coffea canephora and Coffea arabica. J Plant Physiol 2008; 165:1087-106. 15. Maoka T. Recent progress in structural studies of carotenoids in animals and plants. Arch Biochem Biophys 2009; 483:191-5. 16. Ziemlański Ś. Normy żywienia człowieka. Fizjologiczne podstawy. Wyd Lek PZWL, Warszawa 2001; 141-6, 301-2. 17. Luo M, Estívariz CF, Schleicher RL i wsp. Prospective analysis of serum carotenoids, vitamin A and tocopherols in adults with short bowel syndrome undergoing intestinal rehabilitation. Nutr J 2009; 25:400-7. 18. Kiokias S, Dimakou C, Oreopoulou V. Activity of natural carotenoid preparations against the autoxidative deterioration of sunflower oil-in-water emulsions. Food Chem 2009; 114:1278-84. 19. Ren D, Zhang S. Separation and identification of the yellow carotenoids in Potamogeton cripuds L. Food Chem 2008; 106:410-14. 20. Murray RK, Granner DK, Mayes PA i wsp. Biochemia Harpera. Wyd Lek PZWL, Warszawa 1994; 928. 21. Mendes-Pinto MM. Carotenoid breakdown products the – norisoprenoids – in wine aroma. Arch Biochem Biophys 2009; 483:236-45. 22. Larsson SC, Bergkvist L, Wolk A. Dietary carotenoids and risk of hormone receptor-defined breast cancer in a prospective cohort of Swedish women. Eur J Cancer 2010; 46:1079-85. 23. Nkodjock A, Ghadrian P. Intake of specific carotenoids and essential fatty acids and breast cancer risk in Montreal, Canada. Am J Clin Nutr 2004; 79:857-64. 24. Mignone LI, Giovannuci E, Newcomb PA i wsp. Dietary carotenoids and risk of invasive breast cancer. Int J Cancer 2009; 124:2929-37. 25. Cho E, Spiegelman D, Hunter DJ i wsp. Premenopausal intakes of vitamins A, C, and E, folate, and carotenoids, and risk of breast cancer. Cancer Epidemiol Biomarkers Prev 2003; 12:713-20. 26. Zhang S, Hunter DJ, Forman MR i wsp. Dietary carotenoids and vitamins A, C and E and risk of breast cancer. J Natl Cancer Inst 1999; 91:547-56. 27. Nagel G, Linseisen J, van Gils CH i wsp. Dietary beta-carotene, vitamin C and E intake and breast cancer risk in the European Prospective Investigation into Cancer and Nutrition (EPIC). Breast Canc Res Treat 2010; 119:753-65. 28. Bord B. Organic sales in Ireland exceed €100 million. http://www.bordbia.ie/eventsnews/press/2008/Pages/OrganicsalesinIrelandexceed-100million.aspx. 29. Jiwan MA, Duane P, O’Sullivan L i wsp. Content and bioaccessibility of carotenoids from organic and non-organic baby foods. J Food Comp Anal 2010; 23:346-52. 30. Rao AV, Rao LG. Carotenoids and human health. Pharm Res 2007; 55:207-16. 31. Majchrzak D, Frank U, Elmadfa I. Carotenoid profile and retinol content of baby food products. Eur Food Res Technol 2000; 210:407-13. 32. Garrett DA, Failla MI, Sarama RJ. Development of an in vitro digestion method to assess carotenoid bioavailability from meals. J Agr Food Chem 1999; 47:4301-9 33. Caris-Veyrat C, Amiot MJ, Tyssandier V i wsp. Influence of organic versus conventional agricultural practice on the antioxidant microconstituent content of tomatoes and derived purees; consequences on antioxidant plasma status in human. J Agr Food Chem 2004; 52:6503-9.




