© Borgis - Postępy Nauk Medycznych 3/2014, s. 172-177
*Agnieszka Wegner, Maciej Dądalski, Józef Ryżko, Jarosław Kierkuś
Terapia w chorobie Leśniowskiego-Crohna u dziecka. Opis przypadku
Methods of treatment in child with Crohn’s disease. Case report
Klinika Gastrologii, Hepatologii i Zaburzeń Odżywiania, Instytut „Pomnik-Centrum Zdrowia Dziecka”, Warszawa
Kierownik Kliniki: prof. dr hab. med. Józef Ryżko
Streszczenie
Choroba Leśniowskiego-Crohna należy wraz z wrzodziejącym zapaleniem jelita grubego do nieswoistych chorób zapalnych jelit. Dzieci są szczególną grupą pacjentów z nieswoistym zapaleniem jelita, ze względu na większe ryzyko wystąpienia ciężkiej postaci choroby oraz jej wieloletni przebieg. Zmiany zapalne w tej chorobie mają charakter nieswoisty i obejmują całą ścianę jelita. Mogą wystąpić w każdym odcinku przewodu pokarmowego od jamy ustnej do odbytu. Najczęstszą lokalizacją jest końcowy odcinek jelita krętego i początkowy jelita grubego.
Obecnie do powszechnie stosowanych leków w terapii tej choroby należą glikokortykosteroidy, leki immunomodulujące (azatiopryna, 6-merkaptopuryna oraz metotreksat), mesalazyna. Coraz większe zastosowanie w terapii tej choroby znajdują leki biologiczne – infliksimab i adalimumab.
Leczenie operacyjne jest stosowane u dzieci z chorobą Leśniowskiego-Crohna w momencie braku odpowiedzi na zastosowane wcześniej leczenie zachowawcze. U około 75-90% pacjentów z CD zaistnieje konieczność leczenia operacyjnego w ciągu 20 lat trwania choroby.
W artykule przedstawiono opis historii leczenia dziewczynki z chorobą Leśniowskiego-Crohna oraz omówiono główne grupy leków stosowanych w terapii tej choroby.
Summary
Crohn’s disease and ulcerative colitis belong to inflammatory bowel diseases. Children are a specific group of patients with inflammatory bowel disease, due to the increased risk of severe diseases, and its long-term course. Inflammatory changes in this disease are nonspecific and include the entire wall of the intestine. They can occur in any section of the gastrointestinal tract from the mouth to the anus. The most common location is the ileocecal valve.
The glicocorticosteroids, immunomodulator drugs (azathioprine, 6-mercaptopurin, metotrexat), masalamine belong to standard used medicaments in Crohn’s disease. In the recent years biologic agents (infliximab and adalimumab) have played significant role in this disease treatment.
The surgical procedures are used when other methods failed. In approximately 75-90% of patients with CD there is a need surgery within 20 years of disease duration.
In the article we presented a case report of therapy a child with Crohn’s disease. Additionally we discussed main groups of drug used to treat this disease.

Opis przypadku
Siedmioletnia dziewczynka ze zmianami okołoodbytniczymi – pod postacią szczeliny oraz kłykcin odbytu – została przyjęta do Oddziału Gastrologicznego celem diagnostyki oraz zaplanowania dalszego leczenia. Od dwóch lat dziewczynka sporadycznie zgłaszała występowanie bólów brzucha oraz luźnych stolców z domieszką świeżej krwi i śluzu. Obserwowano u niej spowolnienie tempa wzrastania oraz przybierania na masie ciała. W wykonanej rektoskopii stwierdzono zapalenie błony śluzowej odbytnicy, w badaniu histopatologicznym wycinków pobranych w biopsji – nacieki z komórek zapalnych oraz ziarniniak nabłonkowatokomórkowy. Włączono do leczenia doustny preparat mesalazyny.
Ze względu na występujące u dziecka objawy została przekazana do Kliniki Gastrologii IP-CZD. W badaniu fizykalnym z odchyleń stwierdzono niedobór masy ciała i wzrostu (3-10 centyl). W badaniach laboratoryjnych zaobserwowano podwyższone wykładniki stanu zapalnego oraz niedokrwistość. W gastroskopii stwierdzono prawidłowy obraz górnego odcinka przewodu pokarmowego, w kolonoskopii zmiany zapalne w jelicie krętym, poprzecznicy, esicy, odbytnicy. W wykonanym badaniu radiologicznym (pasaż przewodu pokarmowego) końcowy odcinek jelita krętego był wąski, o nierównym świetle. Rozpoznano chorobę Leśniowskiego-Crohna (ryc. 1).
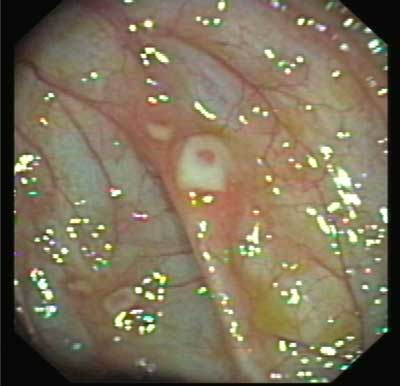
Ryc. 1. Zmiany aftowate na śluzówce jelita.
Włączono do leczenia prednizon (schemat dawkowania: 2 mg na kilogram masy ciała, przez miesiąc, następnie redukcja dawki o 5 mg na tydzień) w celu indukcji remisji choroby oraz azatioprynę (w dawce 2 mg na kilogram masy ciała). W trakcie zmniejszenia dawki sterydu obserwowano u dziewczynki nawrót dolegliwości (luźne stolce, bóle brzucha). W badaniu fizykalnym stwierdzono cechy cushingoidalne, w badaniach laboratoryjnych podwyższone wykładniki stanu zapalnego. W skali PCDAI (Pediatric Crohn’s Disease Activity Index) stwierdzono 50 punktów. Pacjentkę zakwalifikowano do leczenia biologicznego – terapii infliksimabem. Otrzymała dwie dawki leku w odstępie dwóch tygodni (w dawce 5 mg na kilogram masy ciała, w postaci wlewu dożylnego), po których obserwowano poprawę kliniczną. Kontynuowano podaż azatiopryny.
Po miesiącu od otrzymania drugiej dawki infliksimabu dziewczynka zaczęła oddawać liczne luźne stolce z domieszką krwi. W badaniach laboratoryjnych stwierdzono podwyższone wykładniki stanu zapalnego, w skali PCDAI 32,5 punktu. Z tego powodu zwiększono dwukrotnie trzecią dawkę leku (10 mg na kilogram masy ciała we wlewie dożylnym). Jednak objawy nadal się utrzymywały. W kolonoskopii stwierdzono kłykciny wokół odbytu, aktywne zmiany zapalne w jelicie grubym, prawidłową kątnicę oraz ileum terminale. Zadecydowano o zmianie leczenia. Ze względu na dobrą początkowo odpowiedź na infliksimab zadecydowano o zmianie leku biologicznego na inny – wprowadzono adalimumab (pierwsza dawka 80 mg w postaci iniekcji podskórnej, kolejne 40 mg, podawane co dwa tygodnie). Dodatkowo odstąpiono od podaży azatiopryny, jednocześnie wprowadzając metotreksat (w dawce 15 mg na tydzień, w formie doustnej). Przez trzy miesiące w czasie podawania adalimumabu (40 mg w postaci iniekcji podskórnej) oraz metotreksatu dziecko pozostawało w remisji klinicznej.
W czwartym miesiącu stosowanego leczenia u dziewczynki wystąpiły objawy infekcji dróg oddechowych. U pacjentki rozpoznano zapalenie oskrzeli, włączono wtedy antybiotykoterapię oraz odroczono podaż adalimumabu. Po dwóch tygodniach rozpoznano kolejne zaostrzenie choroby Leśniowskiego-Crohna pod postacią bólów brzucha oraz luźnych stolców. W badaniach laboratoryjnych stwierdzono podwyższone wykładniki stanu zapalnego, w skali PCDAI 30 punktów. Ponownie włączono adalimumab. Obserwowano ustąpienie objawów choroby.
Po upływie trzech miesięcy ze względu na nawrót dolegliwości u dziewczynki wykonano badania kontrolne. W kolonoskopii stwierdzono zmiany zapalne o dużym nasileniu obejmujące jelito kręte i grube. W badaniach laboratoryjnych stwierdzono podwyższone wykładniki stanu zapalnego, w skali PCDAI 45 punktów. Ze względu na utratę odpowiedzi na zastosowane leczenie zakwalifikowano pacjentkę do leczenia chirurgicznego – wyłonienia ileostomii dwulufowej. Po operacji włączono azatioprynę w dawce 2 mg na kilogram masy ciała w celu utrzymania remisji choroby.
Po pół roku od leczenia operacyjnego dziewczynka zaczęła oddawać stolec przez odbyt naturalny, pojawiły się u niej bóle brzucha oraz utrata masy ciała. U dziecka podejrzewano powstanie nieprawidłowego połączenia pomiędzy jelitami. Nie zidentyfikowano przetoki w badaniach obrazowych. Przeprowadzono zabieg zamknięcia lufy dystalnej stomii. Jednak nadal obserwowano u dziecka brak przyrostu masy ciała, dodatkowo dziewczynka zgłaszała bóle brzucha.
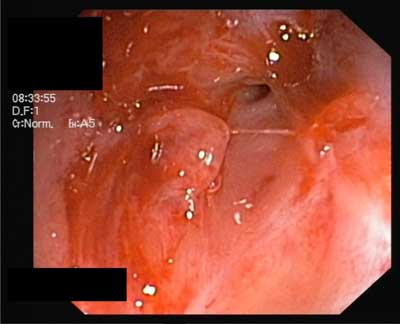
Ze względu na przebieg choroby oraz zastosowane w przeszłości leczenie bez długotrwałej poprawy włączono ponownie sterydoterapię. W trakcie podaży prednizonu obserwowano ustępowanie objawów choroby podstawowej. Jednak w trakcie zmniejszania dawki leku wystąpił kolejny nawrót choroby. W badaniach laboratoryjnych stwierdzono podwyższone wykładniki stanu zapalnego, w skali PCDAI 50 punktów. W przeprowadzonej kolonoskopii zaobserwowano nasilenie zmian zapalnych w obrębie odbytnicy oraz esicy, dodatkowo uwidoczniono owrzodzenia oraz ropną wydzielinę na śluzówce odbytnicy oraz bardzo duże zmiany wokół odbytu w postaci kłykcin (ryc. 2 i 3).
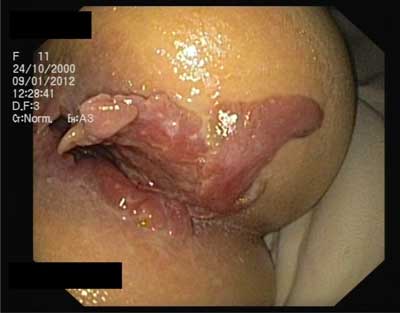
Ryc. 2. Zmiany wokół odbytu.

Ryc. 3. Zmieniona zapalnie śluzówka jelita grubego.
Zmieniono prednizon na budesonid, kontynuowano podawanie azatiopryny, włączono leczenie miejscowe – zastosowano wlewki z hydrokortyzonu. W wykonanych badaniach nie zidentyfikowano defektu receptora dla interleukinu-10 oraz obecności przeciwciał przeciwtkanowych pANCA oraz cANCA.
Po odstawieniu budesonidu u dziewczynki wystąpił rumień guzowaty, włączono cyprofloksacynę oraz maść ichtiolową. Dodatkowo w okolicy odbytu uwidoczniono rozległą szczelinę oraz nadal obecność kłykcin. W skali PCDAI stwierdzono 32,5 punktu. W badaniu kontrolnym przeprowadzonym po odstawieniu sterydoterapii stwierdzono w górnym odcinku przewodu pokarmowego: zapalenie błony śluzowej żołądka oraz dwunastnicy, w dolnym zwężenie pozapalne odbytnicy na głębokości 10 cm, z światłem zwężenia 2-3 mm (ryc. 4). Uwidoczniona przez stomię błona śluzowa jelita cienkiego była prawidłowa.
Ryc. 4. Zwężenie odbytnicy.
Włączono leczenie miejscowe – wlewki z mesalazyny oraz kwasu masłowego. Przez pół roku dziewczynka nie zgłaszała dolegliwości ze strony przewodu pokarmowego.
W kontrolnej kolonoskopii stwierdzono pogorszenie zmian zapalnych w porównaniu z badaniem poprzednim, na głębokości 5 cm uwidoczniono zwężenie o długości 3 cm, powyżej zwężenia pojedyncze zmiany zapalne. Górny odcinek przewodu pokarmowego był prawidłowy. Ze względu na utrzymujące się zmiany w odbytnicy zadecydowano o ponownym leczeniu operacyjnym. Przeprowadzono resekcję dystalnej części jelita grubego, zamknięcie odbytu naturalnego oraz wyłonienie kolostomii w okolicy zagięcia wątrobowego.
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
29 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
69 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
129 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 78 zł
Piśmiennictwo
1. Mendeloff AL: The epidemiology bowel disease. Clin Gastroenterol 1980; 9: 258-270.
2. Kelsen J, Baldassano RN: Inflammatory bowel disease: the difference between children and adults. Inflammatory Bowel Disease 2008 Oct; 14 (suppl. 2): S9-11.
3. Benchimol EI, Fortinsky KJ, Gozdyra P et al.: Epidemiology of pediatric inflammatory bowel disease: a systematic review of international trends. Inflamm Bowel Dis 2011; 17: 423-439.
4. Van Assche G, Dignass A, Reinisch W et al.: The second European evidence-based Consensus on the diagnosis and management of Crohn’s disease: Special situations. Journal of Crohn’s and Colitis 2010; 4: 63-101.
5. Sauer CG, Kugathasan S: Pediatric inflammatory bowel disease: highlighting pediatric differences in IBD. Gastroenterol Clin North Am 2009; 38: 611-628.
6. Beattie RM, Croft NM, Fell JM et al.: Inflammatory bowel disease. Archives of Disease in Childhood 2006; 91(5): 426-432.
7. Rutgeerts P, Vermeire S, Van Asche G: Mucosal healing in inflammatory bowel disease: impossible ideal or therapeutic target? Gut 2007; 56: 453-455.
8. Schnitzler F, Fidder H, Ferrante M et al.: Mucosal healing predicts long-term outcome for maintenance therapy with infliximab in Crohn’s disease. Inflamm Bowel Dis 2009; 15: 1295-1301.
9. Ford AC, Kane SV, Khan KJ et al.: Efficacy of 5-aminosalicylates in Crohn’s disease: systematic review and meta-analysis. Am J Gastroenterol 2011 Apr; 106(4): 617-629. Epub 2011 Mar 15.
10. Travis SP, Stange EF, Lèmann M et al.: European evidence based consensus on the diagnosis and management of Crohn’s disease: current management. Gut 2006; 55 (suppl. 1): i16-i35.
11. Tang J, Sharif O, Pai C et al.: Mesalamine protects against colorectal cancer in inflammatory bowel disease. Dig Dis Sci 2010: 1696-1703.
12. Hyams JS, Markowitz JF: Can we alter the natural history of Crohn disease in children? J Pediatr Gastroenterol Nutr 2005; 40: 262-272.
13. Markowitz J, Hyams J, Mack D et al.: Corticosteroid therapy in the age of infliximab: acute and 1-year outcomes in newly diagnosed children with Crohn’s disease. Clin Gastroenterol Hepatol 2006; 4: 1124-1129.
14. Dziechciarz P, Horvath A, Shamir R et al.: Meta-analysis: enteral nutrition in active Crohn’s disease in children. Aliment Pharmacol Ther 2007; 26: 795-806.
15. Borrelli O, Cordischi L, Cirulli M et al.: Polymeric diet alone versus corticosteroids in the treatment of active pediatric Crohn’s disease: a randomized controlled open-label trial. Clin Gastroenterol Hepatol 2006 Jun; 4(6): 744-753. Epub 2006 May 6.
16. Van Gossum A, Cabre E, Hèbuterne X et al.: ESPEN Guidelines on Parenteral Nutrition: gastroenterology. Clin Nutr 2009 Aug; 28(4): 415-427.
17. Pearson DC, May GR, Fick G et al.: Azathioprine for maintaining remission of Crohn’s disease. Cochrane Database Syst Rev 2000; 2: CD000067.
18. Present DH, Korelitz BI, Wisch N et al.: Treatment of Crohn’s disease with 6-mercaptopurine. A long-term, randomized, double blind study. N Engl J Med 1980; 302: 981-987.
19. Feagan BG, Rochon J, Fedorak RN et al.: Methotrexate for the treatment of Crohn’s disease. The North American Crohn’s Study Group Investigators (comment). N Engl J Med 1995; 332: 292-297.
20. D’Haens G, Geboes K, Ponette E et al.: Healing of severe recurrent ileitis with azathioprine therapy in patients with Crohn’s disease. Gastroenterology 1997; 112: 1475-1481.
21. Kozarek RA, Patterson DJ, Gelfand MD et al.: Methotrexate induces clinical and histologic remission in patients with refractory inflammatory bowel disease. Ann Intern Med 1989; 110: 353-356.
22. Pearson DC, May GR, Fick GH et al.: Azathioprine and 6-mercaptopurin Crohn’s disease: a metaanalysis. Ann Intern Med 1995; 123: 132-142.
23. Danese S, Sans M, Scaldaferri F et al.: TNF-alpha blockade down-regulates the CD40/CD40L pathway in the mucosal microcirculation: a novel anti-inflammatory mechanism of infliximab in Crohn’s disease. J Immunol 2006 Feb 15; 176(4): 2617-2624.
24. Ferkolj I, Ihan A, Markovic S et al.: Infliximab reduces the number of activated mucosal lymphocytes in patients with Crohn’s disease. J Gastrointestin Liver Dis 2006 Sep; 15(3): 231-235.
25. Baldassano R, Braegger CP, Escher JC et al.: Infliximab (Remicade) therapy in the treatment of pediatric Crohn’s disease Am J Gastroenterol 2003; 98: 833-838.
26. Cezard JP, Nouaili N, Talbotec C et al.: A prospective study of the efficacy and tolerance of a chimeric antibody to tumor necrosis factors (remicade) in severe pediatric Crohn’s disease. J Pediatr Gastroenterol Nutr 2003; 36: 632-636.
27. Hyams J, Crandall W, Kugathasan S et al.: Induction and maintenance infliximab therapy for the treatment of moderate to severe Crohn’s disease in children. Gastroenterology 2007; 132: 863-873.
28. Kierkus J, Dadalski M, Szymanska E et al.: The impact of infliximab induction therapy on mucosal healing and clinical remission in Polish pediatric patients with moderate-to-severe Crohn’s disease. J Eur J Gastroenterol Hepatol 2012 May; 24(5): 495-500.
29. Kierkus J, Dądalski M, Szymanska S et al.: Maintenance therapy with infliximab for paediatric Crohn’s disease: impact on clinical remission and mucosal healing in Polish paediatric patients with severe Crohn’s disease. Przegląd Gastroenterologiczny 2012; 7(1): 26-30.
30. Borrelli O, Bascietto C, Viola F: Infliximab heals intestinal inflammatory lesions and restores growth in children with Crohn’s disease. Dig Liver Dis 2004; 36: 342-347.
31. Löwenberg M, Peppelenbosch M, Hommes D: Biological therapy in the management of recent onset Crohn’s disease: why, when and how? Drugs 2006; 66(11): 1431-1439.
32. Pressman AR, Hutfless S, Velayos F et al.: Patterns of infliximab use among Crohn’s disease patients in a community setting. Inflamm Bowel Dis 2008 Sep; 14(9): 1265-1272.
33. Hyams J, Lerer T, Griffiths A et al.: Long-term outcome of maintenance infliximab therapy in children with Crohn’s disease. Inflam Bowel Dis 2009; 15: 816-822.
34. Rosh JR, Lerer T, Markowitz J et al.: Retrospective Evaluation of the Safety and Effect of Adalimumab Therapy (RESEAT) in pediatric Crohn’s disease. Am J Gastroenterol 2009; 104: 3042-3049.
35. Russell RK, Wilson ML, Loganathan S et al.: A British Society of Paediatric Gastroenterology, Hepatology and Nutrition survey of the effectiveness and safety of adalimumab in children with inflammatory bowel disease. Aliment Pharmacol Ther 2011; 33: 946-953.
36. Wyneski MJ, Green A, Kay M et al.: Safety and efficacy of adalimumab in pediatric patients with Crohn disease. J Pediatr Gastroenterol Nutr 2008; 47: 19-25.
37. Rosenbach Y, Hartman C, Shapiro R et al.: Adalimumab treatment in children with refractory Crohn’s disease. Dig Dis Sci 2010; 55: 747-753.
38. Hyams JS, Griffiths A, Markowitz J et al.: Safety and efficacy of adalimumab for moderate to severe Crohn’s disease in children. Gastroenterology 2012 Aug; 143(2): 365-374.




