*Agnieszka Dmowska-Koroblewska, Michał Michalik, Adrianna Podbielska-Kubera, Włodzimierz Jakub Siemianowski
Badanie endoskopowe drożności dróg oddechowych w czasie snu farmakologicznego – wstępne wyniki
Drug-induced sleep endoscopy in assessing airway patency – own experiences
Department of Otolaryngology, MML Medical Center, Warsaw
Head of Department: Michał Michalik, MD, PhD
Streszczenie
Wstęp. Zespół obturacyjnego bezdechu sennego należy do zaburzeń oddychania w czasie snu. Brak poprawy stanu zdrowia po wcześniej wykonanych zabiegach laryngologicznych stanowi wskazanie do badania endoskopowego w czasie snu indukowanego (DISE– ang. drug-induced sleep endoscopy). DISE dostarcza istotnych informacji na temat czynnościowej drożności górnych dróg oddechowych.
Materiał i metody. Badania przeprowadzono na grupie pacjentów, u których wcześniejsze leczenie chrapania i bezdechu sennego było nieskuteczne. U pacjentów przeprowadzono endoskopię w czasie snu indukowanego DISE. Do znieczulenia zastosowano propofol podawany w ciągłym wlewie dożylnym, co zapewniło bezpieczeństwo wykonywanej procedury.
Wyniki. Od 2007 do 2017 roku w Centrum Medycznym MML przeprowadzono 3911 zabiegów leczących chrapanie i bezdechy podczas snu. W tym czasie wykonano 176 procedur DISE. Sposoby leczenia przyczynowego określano na podstawie ankiety, tomografii komputerowej z promieniem stożkowym (CBCT – ang. cone beam computed tomography), badania laryngologicznego i DISE. Subiektywną poprawę z ustąpieniem objawów uzyskano u 80% pacjentów. W 70% przypadków chrapanie zmniejszyło się. U pozostałej części pacjentów wymagane było poszukiwanie przyczyn ogólnoustrojowych: kardiologicznych, neurologicznych gastrologicznych lub endokrynologicznych.
Wnioski. W grupie pacjentów Centrum Medycznego MML zastosowanie techniki DISE przyczyniło się do precyzyjnego określenia miejsca wibrowania i zapadania się dróg oddechowych.
Badanie DISE daje powtarzalne pomiary drożności dróg oddechowych na poziomie gardła dolnego. DISE umożliwia efektywną diagnostykę przyczyn zaburzeń snu w sytuacji, gdy inne metody, takie jak tomografia stożkowa czy cefalometria, nie są wystarczające.
Summary
Introduction. Obstructive sleep apnea is a disorder of breathing during sleep. Lack of clinical improvement after previously performed laryngological procedures is an indication for endoscopic examination during drug – induced sleep. Drug-induced sleep endoscopy (DISE) provides important information about functional upper airways patency.
Material and methods. The study was performed in patients in whom other treatment methods had not been effective. DISE was performed in these patients. Continuous intravenous propofol infusion was given as general anesthetic to ensure the safety of the procedure.
Results. From 2007 to 2017, 2897 procedures for snoring and sleep apnea were performed at the MML Medical Center. At this time, 176 DISE examinations were performed.
Causative treatment methods were determined by the means of questionnaire, CBCT, laryngological examination, and DISE examination. Subjective improvement of apnea symptoms was achieved in 80% of patients. In 70% of cases, snoring decreased. The rest of the patients are required to look for systemic causes of cardiological, neurological gastrological, or endocrine origin.
Conclusions. In our patients, the use of the DISE examination enabled to precisely determine the location of the vibration and of the collapse of the respiratory tract. DISE enables to effectively diagnose the cause of sleep disorders when other methods, such as cone beam computed tomography (CBCT) or cephalometry are not sufficient.
Wstęp
Zespół obturacyjnego bezdechu sennego (OSAS – ang. obstructive sleep apnea syndrome) dotyczy od 2% do 4% populacji, głównie ludzi dorosłych (1). Około 80% - 90% osób z OSAS pozostaje niezdiagnozowanych (2). OSAS występuje także u dzieci, zwłaszcza powyżej 3.-6. roku życia (1).
Zespół obturacyjnego bezdechu sennego charakteryzuje się wysokim wskaźnikiem zachorowalności i śmiertelności i jest uważany za problem zdrowia publicznego. Objawy kliniczne OSAS obejmują chrapanie, niespokojny sen (2). Schorzenie może być także powiązane ze słabą koncentracją, porannymi bólami głowy, nadmierną sennością w ciągu dnia, zmniejszonymi zdolnościami intelektualnymi (3). Dolegliwości prowadzą do niedotlenienia organizmu i znacznie pogarszają jakość życia chorych. Czynniki takie jak otyłość, alergia, deformacja twarzoczaszki mogą nasilać ten problem (4). Jednym z najczęściej występujących czynników ryzyka jest otyłość (5). Szczególne znaczenie ma gromadzenie się nadmiernej ilości tkanki tłuszczowej w okolicy szyi (6). Następstwem bezdechu sennego mogą być powikłania kardiologiczne (zawał serca), neurologiczne (udar mózgu), endokrynologiczne (zaburzenia wzrostu u dzieci), czy też pulmonologiczne (nadciśnienie płucne) (7). Dlatego tak ważna jest diagnostyka tego schorzenia i jego właściwe leczenie.
Obturacyjny bezdech senny jest wynikiem nieprawidłowości w budowie górnych dróg oddechowych, takich jak przerost małżowin nosowych, obecność polipów, skrzywienie przegrody nosa, przerost migdałków podniebiennych, migdałka gardłowego, wiotkie opadające podniebienie, zwłaszcza języczek, przerośnięta nasada języka, czy patologia w obrębie krtani (8). Bezdech definiuje się jako całkowite zablokowanie przepływu powietrza przez drogi oddechowe trwające co najmniej 10 sekund (4). Celem leczenia obturacyjnego bezdechu sennego jest utrzymanie drożności górnych dróg oddechowych.
Nasilenie objawów OSAS jest zmienne i zależy od wiele czynników, które wciąż nie do końca są poznane (9). Potwierdzono, że pozycja podczas snu wpływa na częstotliwość występowania i stopień nasilenia objawów bezdechu sennego. Dolegliwości u pacjentów z OSAS (częstotliwość bezdechu, czas trwania, desaturacja) zwiększają się w czasie pozostawania pacjentów w pozycji leżącej. Zmiany w górnych drogach oddechowych w zależności od pozycji przybieranej podczas snu odpowiadają różnym nasileniom zdarzeń bezdechowych. Mechanizm odpowiedzialny za nasilenie objawów w pozycji na plecach nie jest jasny. Najprawdopodobniej powiązany jest z wpływem grawitacji na ułożenie poszczególnych odcinków górnych dróg oddechowych. W pozycji leżącej skłonność do zapadania dróg oddechowych jest większa. Przy zmianie pozycji z leżącej na boczną niedrożność na poziomie struktur takich jak podstawa języka i krtań jest rzadziej spotykana. Ocena zmian w pozycji elementów anatomicznych górnych dróg oddechowych w zależności od pozycji snu może być stosowana do planowania leczenia celowanego u pacjentów (9).
W diagnostyce chorych z OSAS wykorzystuje się badanie laryngologiczne, badanie endoskopowe, polisomnografię (PSG), tomografię komputerową z promieniem stożkowym (CBCT – ang. cone beam computed tomography), rynomanometrię, jak również badanie endoskopowe w czasie snu indukowanego (DISE – ang. drug-induced sleep endoscopy).
Polisomnografia, opisana po raz pierwszy w 1965 roku przez Gastauta, jest wykorzystywana do diagnozowania i oceny ciężkości OSAS. Ciągłe dodatnie ciśnienie w drogach oddechowych (CPAP – ang. Continuous Positive Airway Pressure) jest uważane za złoty standard leczenia w przypadku chorych z OSAS (10).
Brak poprawy po wcześniej wykonanych zabiegach laryngologicznych (septokonchoplastyka, plastyka podniebienia miękkiego, tonsillotomia lub tonsillektomia) stanowi wskazanie do DISE (11). Sytuacja powyższa dotyczy zarówno dorosłych, jak i dzieci. Badanie DISE należy wykonać u dzieci, które po adenotosillotomii nadal chrapią i wybudzają się w czasie snu (11).
W 1991 roku Croft i Pringle po raz pierwszy zastosowali endoskopię w trakcie snu wywołanego farmakologicznie, podczas którego uwidocznili światło dróg oddechowych w znieczuleniu (12).
Chirurgiczne leczenie zespołu obturacyjnego bezdechu sennego wymaga dokładnej lokalizacji przeszkody. Jedynie badanie górnych dróg oddechowych u śpiącego pacjenta może dostarczyć pełnej informacji o stanie zdrowia (13). Do tej pory nie ma optymalnej metody określania miejsc niedrożności dróg oddechowych (3). Niestety większość technik stosowanych w celu przeprowadzenia badania lokalizacji niedrożności opiera się na badaniu w stanie czuwania i obejmuje obserwacje statyczne, a nie dynamiczne. DISE to unikalne badanie do oceny przyczyny bezdechu i/lub chrapania, dzięki wprowadzeniu pacjenta w lekki sen wywołany podaniem środka farmakologicznego (10).
Badanie przeprowadza się w warunkach pełnego bezpieczeństwa pacjenta, w obecności anestezjologa na bloku operacyjnym lub w odpowiednio wyposażonej sali zabiegowej. Parametry życiowe pacjenta są cały czas monitorowane, w razie konieczności pacjent może zostać zaintubowany i podłączony do respiratora (14).
Różne systemy klasyfikacji, takie jak system klasyfikacji VOTE (ang. velum, oropharynx lateral walls, tongue base, epiglottis – podniebienie, ściany boczne gardła, podstawa języka, nagłośnia) i system NOHL (ang. nose, oropharynx, hypopharynx, larynx – nos, gardło, gardło dolne, krtań) są używane do określenia miejsca i stopnia obturacji górnych dróg oddechowych u pacjentów z OSAS. Klasyfikacja VOTE umożliwia ocenę jakościową (3). Dla każdego z poziomów opisuje się stopień obturacji w skali trzystopniowej: 0 – brak obturacji (brak wibracji), 1 – częściowa obturacja (wibracje), 2 – całkowita obturacja (zapadanie). Opisany jest także sposób, w jaki sposób dochodzi do obturacji: ap (ang. anterior-posterior – przednio-tylny), l (ang. lateral – boczny) (ryc. 1), c (ang. concentric – okrężny). Nie wszystkie wzory obturacji mogą występować na wszystkich ocenianych poziomach (11).
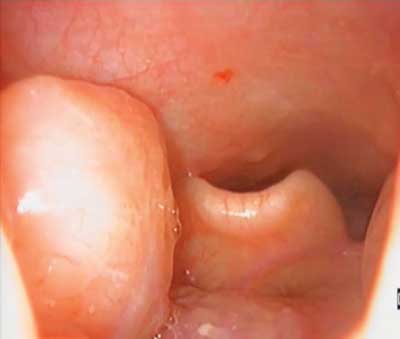
Ryc. 1. Dolny biegun migdałka podniebiennego uciskający nagłośnię
W systemie NOHL na każdym z wymienionych poziomów określa się stopień obturacji w skali pięciostopniowej od 0 do 4 oraz wzór obturacji – dotyczący gardła: ap (ang. anterior-posterior – przednio-tylny), l (ang. lateral – boczny), c (ang. circular – okrężny) i krtani: a (nadgłośniowo), b (na poziomie głośni), p (ang. positive – obecne), n (ang. negative – nieobecne) (ryc. 2, 3) (15).
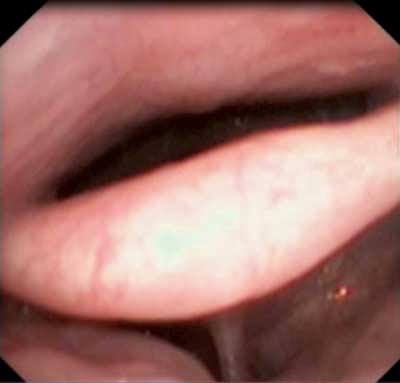
Ryc. 2. Zapadanie się nagłośni

Ryc. 3. Zamknięcie światła dróg oddechowych na poziomie nagłośni
Zdecydowana większość badaczy korzysta z systemu klasyfikacji VOTE (3).
Materiał i metody
Praca ma charakter retrospektywny. Badania przeprowadzono wśród pacjentów z bezdechem sennym. Pacjenci przed wykonaniem badania otrzymali do wypełnienia ankiety: kwestionariusz do diagnostyki przesiewowej zaburzeń oddychania w czasie snu – poszerzona, autorska wersja oparta o kwestionariusz berliński (ryc. 4) – w celu oceny zależności pomiędzy zaburzeniami oddychania w czasie snu a chorobami układu oddechowego i układu krążenia oraz kwestionariusz skali senności Epworth wg British Snoring & Sleep Apnoea Association (ryc. 5) – w celu oceny senności i prawdopodobieństwa zaśnięcia w sytuacjach życia codziennego.



Ryc. 4. Kwestionariusz do diagnostyki przesiewowej zaburzeń oddychania w czasie snu

Ryc. 5. Skala senności dziennej Epworth
U części pacjentów w ramach diagnostyki poszerzonej wyznaczono również wskaźnik bezdechu/spłycenia oddechu (AHI – ang. apnea/hypopnea index). AHI określa nasilenie występowania bezdechów w czasie snu, wyraża się liczbą bezdechów i spłyceń oddychania w przeliczeniu na godzinę snu (tab. 1).
Tab. 1. Wartość indeksu AHI a stopień ciężkości choroby
| AHI | Ciężkość OSAS |
| < 5 | w normie |
| 5-14 | postać lekka bezdechu |
| 15-24 | postać umiarkowana bezdechu |
| > 24 | postać ciężka bezdechu |
Dla każdego pacjenta obliczono również wskaźnik masy ciała (BMI – ang. Body Mass Index) oraz zmierzono obwód szyi.
W badaniu laryngologicznym oceniono nos zewnętrzny (symetrie i ew. deformacje), nozdrza przednie, przegrodę nosową i małżowiny dolne. Oceniono również podniebienie miękkie wg skali Mallampatiego (tab. 2) oraz migdałki podniebienne wg skali Pirqueta (tab. 3).
Tab. 2. Skala Mallampatiego
| Stopień | Opis |
| 1. | widoczne podniebienie miękkie, języczek, gardło i zarys migdałków |
| 2. | widoczne podniebienie miękkie i języczek |
| 3. | widoczne podniebienie miękkie i podstawa języczka |
| 4. | nie widać podniebienia miękkiego |
Tab. 3. Skala Pirqueta
| Stopień | Opis |
| I° | Migdałki są schowane za łukami podniebiennymi |
| II° | Migdałki sięgają do łuków podniebiennych |
| III° | Migdałki przekraczają linię łuków podniebiennych |
| IV° | Migdałki zajmują połowę szerokości gardła |
| V° | Migdałki stykają się ze sobą na tylnej ścianie gardła |
Pacjentów poddano badaniom endoskopowym i CBCT (ryc. 6). Wskazania do leczenia chirurgicznego obejmowały skrzywioną przegrodę nosową, przerost małżowin nosowych dolnych i wiotkie opadające podniebienie miękkie.
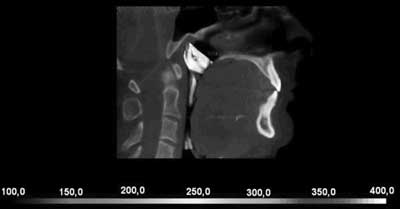
Ryc. 6. Zaburzenie drożności dróg oddechowych na poziomie podniebienia miękkiego i nasady języka
Pacjentów poddawano wówczas plastyce podniebienia, plastyce małżowin nosowych dolnych metodą koblacji, septoplastyce, tonsillotomii lub tonsillektomii. Do leczenia zabiegowego wykorzystano różne techniki, włączając w to metodę Shaver, metodę Celon/koblacji, czy laser diodowy kontaktowy.
Pacjentów kontrolowano w 1. i 4. tygodniu po zabiegu. Wyniki leczenia oceniano 3 miesiące po zabiegu. Pacjenci ponownie wypełniali ankiety, przeprowadzono również badanie laryngologicznie. U każdego pacjenta wykonano ponadto CBCT i rynomanometrię. Jeżeli drożność nosa była zachowana oraz w badaniu podniebienie miękkie było napięte, a objawy utrzymywały się, szukano przyczyn w gardle dolnym i krtani.
Brak poprawy po wcześniej wykonanych zabiegach laryngologicznych stanowił wskazanie do wykonania DISE.
W badaniu DISE wykorzystano następującą aparaturę: procesor wideo Olympus CV-170; wideorynolaryngoskop Olympus ENF-V3 o średnicy 2,6 mm i długości 30 cm; wideorynolaryngoskop Olympus ENF-VH o średnicy 3,9 mm i długości 30 cm.
W dniu badania pacjenci zgłaszali się do szpitala i byli przyjmowani na oddział w trybie hospitalizacji jednodniowej.
Zastosowano standardową procedurę przygotowania do zabiegu ze znieczuleniem ogólnym.
Pacjenci przed przystąpieniem do badania pozostawali na czczo. Nie było potrzeby wykonywania badań dodatkowych z krwi przed znieczuleniem, przeprowadzono natomiast wywiad dotyczący chorób przewlekłych.
Pacjenci podczas badania spoczywali na stole operacyjnym w pozycji na wznak. Standardowe monitorowanie obejmowało monitorowanie EKG, pomiar częstości akcji serca, ciśnienia tętniczego i saturacji krwi tlenem SaO2. Do nosa założono pacjentom tlenowe kaniule donosowe. W trakcie badania kaniule były przyłożone do ust, aby nie kolidować z drogą wprowadzenia endoskopu miękkiego. W trakcie badania podawano tlen w ilości ok. 2-3 l/min. U każdego pacjenta uzyskano dostęp dożylny do żyły przedramienia. Po premedykacji dożylnej midanium w dawce 3 mg, wprowadzono do znieczulenia propofol w dawce indukcyjnej 1-1,5 mg/kg masy ciała. Wlew dożylny propofolu kontynuowany był przez pompę infuzyjną w dawce 3-6 mg/kg masy ciała/godz. przez cały czas badania. Podanie propofolu w pompie dożylnej zapewniło bezpieczną i stabilną sedację (9).
Pacjenci Centrum Medycznego MML na ogół nie wymagali podaży narkotycznych leków przeciwbólowych. Po skończonym badaniu wyłączono dożylny wlew propofolu. Po ok. 5-10 minutach pacjenci wybudzali się ze snu indukowanego i byli przewożeni do sali wybudzeniowej. Po ok. 2-3 godzinach mogli opuścić szpital.
W ocenie obturacji dróg oddechowych posługiwano się skalą punktową VOTE (7).
Metody leczenia, jakie stosuje się w Centrum Medycznym MML zależą od umiejscowienia przyczyny schorzenia. Wykorzystuje się techniki przedstawione wcześniej.
Przedstawione wyniki obejmują odpowiedzi pacjentów na pierwszych 10 pytań zawartych w kwestionariuszu do diagnostyki przesiewowej zaburzeń oddychania w czasie snu. Wyniki całościowe, obecnie w trakcie analizy, zostaną uzyskane na podstawie wyników kwestionariusza, skali senności Epworth, badania rynomanometrycznego oraz tomografii komputerowej. Ze względu na dużą liczbę otrzymanych danych pozostałe wyniki są w trakcie analizy.
Wyniki
Od 2007 do 2017 roku w Centrum Medycznym MML przeprowadzono 2897 zabiegów leczących chrapanie i bezdechy podczas snu. Badania objęły 1053 kobiety i 2844 mężczyzn. Średni wiek pacjentów wynosił 46 lat (mężczyźni) i 35 lat (kobiety). Średni czas trwania choroby wynosił 4 lata. Wykonano 176 zabiegów DISE. Sposoby leczenia przyczynowego określano na podstawie ankiety, CBCT, badania laryngologicznego i endoskopowego. Subiektywną poprawę z ustąpieniem objawów uzyskano u 80% pacjentów. W 70% przypadków chrapanie zmniejszyło się. U pozostałej części pacjentów wymagane było poszukiwanie przyczyn ogólnoustrojowych: kardiologicznych, neurologicznych gastrologicznych lub endokrynologicznych.
Dyskusja
OSAS to rozpowszechnione, ale w dużej części niezdiagnozowane schorzenie (1). Obturacyjny bezdech senny przez wiele lat pozostawał niedocenianym czynnikiem ryzyka chorób sercowo-naczyniowych (6). Dlatego niezbędne są badania oceniające ryzyko wystąpienia zaburzeń oddychania podczas snu, a także opracowanie strategii zapobiegania i leczenia OSAS (12).
Diagnostyka OSAS opiera się na wywiadzie chorobowym oraz badaniu polisomnograficznym, które ocenia rodzaj i nasilenie zaburzeń oddychania w czasie snu.
Pacjenci znajdujący się w grupie ryzyka proszeni są o wypełnienie kwestionariusza do diagnostyki przesiewowej zaburzeń oddychania w czasie snu oraz kwestionariusza skali senności dziennej Epworth. U pacjentów z potwierdzonym bezdechem sennym wskazana jest również konsultacja laryngologiczna w celu oceny zaburzeń drożności górnych dróg oddechowych. W przypadku stwierdzenia nieprawidłowości anatomicznych należy rozważyć leczenie operacyjne.
Pacjenci Centrum Medycznego MML, u których nie stwierdzono poprawy po wcześniej wykonanych zabiegach laryngologicznych, poddawani byli badaniu DISE.
U ponad 80% pacjentów objętych badaniem zaobserwowano zmniejszenie objawów – zniknęły problemy z sennością w ciągu dnia i trudności w zasypianiu wieczorem, a chrapanie zmniejszyło się, co jest zgodne z doniesieniami z literatury (17). W nierandomizowanym badaniu prospektywnym, w którym poddano pacjentów diagnostyce DISE, na podstawie zdjęć cyfrowych wykonanych podczas zabiegu Ryan C. i wsp. (18) określili procentowy stopień zwężenia dróg oddechowych u pacjentów. Największy stopień zwężenia stwierdzono na poziomie podniebienia (84.1 ± 18.7%), a także na poziomie podstawy języka (39.3 ± 37.5%) i nagłośni (44.6 ± 42.8%).
Dane literaturowe pokazują, że DISE jest bezpieczną, skuteczną, powtarzalną i łatwą w zastosowaniu techniką lokalizowania miejsc niedrożności w górnych drogach oddechowych. Wstępne badania wykazały, że sukces terapeutyczny leczenia OSAS u pacjentów, u których zastosowano technikę DISE jest częstszy (75%) niż u pozostałych pacjentów (40%) (3). Hessel i wsp. (13) potwierdzają skuteczność DISE u pacjentów z OSAS w 69% przypadków.
Endoskopia w czasie snu indukowanego okazała się ważną techniką identyfikującą wielopoziomowe zapadnięcia, szczególnie u nasady języka i w okolicach nagłośni. Badania przeprowadzone techniką DISE wykazały również istotną rolę niedrożności krtani w OSAS (2).
W leczeniu chorych z OSAS nadal dominuje CPAP. Pomimo udowodnionej skuteczności techniki CPAP znaczna liczba pacjentów nie może tolerować tej formy leczenia i poszukuje alternatyw, takich jak chirurgia i/lub aparaty czynnościowe doustne (19). Technika CPAP okazuje się nieskuteczna w przypadku leczenie pacjentów, u których dochodzi do zapadania się nagłośni, ponieważ może skutkować przesuwaniem nagłośni w stronę krtani (19).
Chisholm i wsp. (13) donoszą, że pacjenci, u których zastosowanie CPAP nie powiodło się, można poddać zabiegowi DISE. Możliwe jest wówczas zastosowanie skutecznej laserowej operacji podniebienia miękkiego oraz obniżenie indeksu AHI poniżej 20 w 90% przypadków (13).
Metoda inwazyjna, resekcja nagłośni, jest preferowanym rozwiązaniem w przypadkach, gdy nagłośnia zapada się i blokuje drogi oddechowe podczas snu. U pacjentów z OSAS usuniecie nagłośni w połączeniu z innymi procedurami może prowadzić do znacznej poprawy stanu zdrowia pacjenta (19).
Zabieg DISE nie jest przeprowadzany podczas snu fizjologicznego. W naturalnym śnie występuje redukcja napięcia mięśni bródkowo-językowych podczas faz snu NREM (ang. non-rapid eye movement – wolne ruchy gałek ocznych) i REM (ang. rapid eye movement – szybkie ruchy gałek ocznych). Zjawisko to u chorych z OSAS jest bardziej nasilone niż u osób zdrowych. Po farmakologicznym wprowadzeniu pacjenta w sen redukcja napięcia mięśnia bródkowo-językowego może przyczyniać się do zapaści podstawy języka. Dla potwierdzenia skuteczności i celowości przeprowadzenia zabiegu DISE niezbędne jest przeprowadzenie randomizowanych badań na dużej grupie pacjentów (20). Jednocześnie wyniki badań przeglądowych pokazują wiele rozbieżności między lokalizacjami przeszkód u pacjentów pozostających w stanie czuwania i poddanych zabiegowi DISE (13).
DISE jest uważane za integralną część diagnostyki pacjentów z podejrzeniem OSAS w wielu krajach, m.in. w Holandii. Przeciwnicy metody argumentują, że sen farmakologiczny nie jest równoważny ze snem fizjologicznym. Idealnym rozwiązaniem byłoby przeprowadzenie zabiegu DISE podczas snu fizjologicznego, jednakże taka procedura jest bardzo wymagająca i stosowana bardzo rzadko (10).
Zwrócono ponadto uwagę na konieczność stosowania jednolitej metody sedacji (10). Wpływ metod sedacji (propofol i midazolam w dawce początkowej, a następnie dozowany stopniowo w trakcie zabiegu) na wynik badania niedrożności dróg oddechowych może być różny. Rabelo i wsp. podają, że korzystanie z propofolu skraca fazę snu REM, co nieznacznie zmienia architekturę snu, a jednocześnie nie wpływa znacząco na układ oddechowy i wskaźnik AHI (10). Te same wnioski zostały wyciągnięte z badania z zastosowaniem diazepamu. W badaniach przeprowadzonych przez Sadaoka i wsp. dowiedziono, że sen farmakologiczny po podaniu diazepamu nie różni się od snu fizjologicznego, poza długością trwania fazy REM (10). Do chwili obecnej brakuje standardowego protokołu znieczulenia podczas badania DISE, bowiem dawkowanie i czas trwania anestezji zależą od wielu czynników, m.in. różnic międzyosobniczych, podatności na działanie uspokajające leku. Dalsze badania są niezbędne w celu uniknięcia wyników fałszywie dodatnich (10).
W literaturze znajdujemy doniesienia mówiące o zastosowaniu DISE-TCI (ang. Target Controlled Infusion – docelowa infuzja kontrolowana) w celu odtworzenia zachowania się dróg oddechowych podczas chrapania i bezdechu w trakcie DISE (21). W docelowej infuzji kontrolowanej, po zaprogramowaniu żądanego stężenia anestetyku w surowicy lub narządzie efektorowym (mózgu), pompa infuzyjna na podstawie algorytmu uwzględniającego m.in. płeć, wiek, masę ciała, wzrost chorego ustala szybkość wlewu leków. Ten sposób podaży leków znieczulających zapewnia szybkie uzyskanie i utrzymanie odpowiedniej głębokości znieczulenia (22). Według danych literaturowych lepszą kontrolę sedacji umożliwia jednak analiza bispektralna oceniająca czynność mózgu (23). Analiza bispektralna minimalizuje ryzyko przywrócenia świadomości pacjenta podczas zabiegu. Umożliwia ponadto właściwe dawkowanie propofolu podczas zabiegu (24).
W randomizowanym prospektywnym badaniu jednoośrodkowym przeprowadzono badanie porównujące skuteczność DISE i DISE-TCI (13). Objęło ono 40 chorych przydzielonych losowo do grupy DISE lub DISE-TCI. Zaobserwowano istotną statystycznie różnicę w odsetku pacjentów, u których stwierdzono wyleczenie bezdechu (4 chorych – 20% – w grupie DISE vs. 17 chorych – 85% – w grupie DISE-TCI; p < 0,0001). Dwóch pacjentów z grupy DISE wymagało podania tlenu po podaniu pierwszej dawki propofolu. Niestabilność podczas znieczulenia zaobserwowano u 13 pacjentów z grupy DISE (65%) i 1 pacjenta z grupy DISE-TCI (5%) (p = 0,0001). Wyniki sugerują, że technika DISE-TCI powinna być pierwszym wyborem w wykonywaniu endoskopii snu ze względu na zwiększoną dokładność, stabilność i bezpieczeństwo (21). Jednocześnie Witkowska M. i wsp. (18) podają, że nie ma istotnie klinicznych różnic parametrów hemodynamicznych, głębokości snu, czasu budzenia, zużycia środków anestetycznych pomiędzy docelowo kontrolowaną infuzją a wlewem tych środków kontrolowanym manualnie.
Dane uzyskane podczas badania DISE powinny być interpretowane z zachowaniem środków ostrożności. W niektórych przypadkach znalezienie dodatkowych miejsc niedrożności może prowadzić do zastosowania niepotrzebnych procedur. Wysokie dawki leków i długi czas badania stanowią niedogodności metody DISE. Ponadto leczenie wszystkich miejsc niedrożności znalezionych dzięki technice DISE nie jest gwarancją sukcesu (13). DISE może pomóc wyjaśnić patofizjologię bezdechów związanych z przybieraniem różnych pozycji w trakcie spania (25).
Abdullah i wsp. zaobserwowali, że pacjenci z wyższym współczynnikiem BMI cechują się występowaniem większej liczby miejsc niedrożności (4 lub więcej) w porównaniu z pozostałymi pacjentami, u których zazwyczaj stwierdza się jedynie pojedyncze miejsca niedrożności (10).
Dane zawarte w piśmiennictwie wskazują, że sukces chirurgiczny jest zdecydowanie rzadszy u pacjentów ze zwiększonym BMI. U tych pacjentów występuje głównie niedrożność koncentryczna. Iwanaga i wsp. (10) potwierdzili częstsze występowanie niedrożności na poziomie podniebienia oraz obturację u podstawy języka u pacjentów z BMI > 30 oraz z wyższymi wartościami wskaźnika AHI. Przy wyższych wartościach AHI obserwujemy ponadto zapadanie się dróg oddechowych na wielu poziomach (10).
Piśmiennictwo podaje, w jaki sposób badanie DISE, w porównaniu z klasycznym badaniem laryngologicznym, wpływa na kwalifikację do poszczególnych procedur zabiegowych lub aparatu wysuwającego żuchwę. Po przeprowadzeniu DISE rekomendowano zmianę sposobu leczenia. Operacje podniebienia miękkiego proponowano w 93,8% po przeprowadzeniu badania DISE (77,3% – bez tego badania). Modyfikację sposobu leczenia po badaniu DISE u 23 z 38 pacjentów zaproponowali też Gillespie i wsp (14). Planowanie leczenia z zastosowaniem badania DISE pozwoliło na uzyskanie poprawy u 72% pacjentów w dużej grupie obejmującej 2485 chorych analizowanych przez Kotecha i wsp. (14).
Zapadanie się nagłośni u pacjentów z OSAS występuje częściej niż przedstawiały wcześniejsze wyniki badań. Przed wprowadzeniem techniki DISE zapadanie się nagłośni diagnozowano u 12% pacjentów z OSAS w oparciu o badanie w stanie czuwania. Zapadanie się nagłośni można zaobserwować podczas badania DISE, nawet gdy wcześniejsze badania laryngologiczne nie wykazują nieprawidłowości (19).
W grupie pacjentów Centrum Medycznego MML głównym celem przeprowadzonych badań było precyzyjne określenie miejsca wibrowania i zapadania się dróg oddechowych. Technika DISE w pełni umożliwiła nam osiągnięcie tego celu. Należy podkreślić, że DISE jako procedura diagnostyczna ma swoje wady, do których zaliczają się przede wszystkim wysokie koszty i ryzyko powikłań (m.in. reakcja alergiczna, niedrożność dróg oddechowych) (26). Ponadto metoda ta jest zależna od doświadczenia operatorów, sposobu podania znieczulenia i jego dawki. Ogromnym ograniczeniem w stosowaniu DISE do diagnostyki OSAS jest mnogość i złożoność systemów klasyfikacji, co w znacznym stopniu utrudnia porównywanie wyników między ośrodkami (27).
Kluczem do sukcesu terapeutycznego jest indywidualne podejście do pacjenta i zwrócenie uwagi na przyjmowaną w czasie snu pozycję oraz cechy osobnicze pacjenta (10).
Należy zwrócić uwagę również na doświadczenie zawodowe lekarzy przeprowadzających badanie.
Doniesienia literaturowe potwierdzają, że doświadczenie w wykonywaniu techniki DISE jest konieczne, aby uzyskać wiarygodne obserwacje (28).
Powyższe zagadnienia stanowią nadal przedmiot badań.
Wnioski
W grupie pacjentów Centrum Medycznego MML zastosowanie techniki DISE przyczyniło się do precyzyjnego określenia miejsca wibrowania i zapadania się dróg oddechowych.
Badanie DISE daje powtarzalne pomiary drożności dróg oddechowych na poziomie gardła dolnego.
DISE umożliwia efektywną diagnostykę przyczyn zaburzeń snu w sytuacji, gdy inne metody, takie jak tomografia stożkowa czy cefalometria, nie są wystarczające. Zwrócono szczególną uwagę na badanie czynnościowe dróg oddechowych z jednoczasowym wykonaniem zabiegu.
Pomimo braku standaryzacji badań klinicznych, rodzaju leków stosowanych w sedacji oraz zastosowanego systemu klasyfikacji wyniki badań opisane w literaturze sugerują włączenie techniki DISE do diagnostyki miejsc niedrożności u pacjentów z OSAS. Zastosowanie uniwersalnego systemu oceny DISE może ułatwić porównywanie wyników badań pomiędzy ośrodkami.
Podczas badania DISE możliwe jest zobrazowanie, w jaki sposób dochodzi do zapadania się górnych dróg oddechowych oraz na jakim poziomie. Możliwa jest ocena nawet kilku miejsc obturacji, co oznacza przewagę tego badania nad klasyczną endoskopią. Klasyczna endoskopia, w odróżnieniu od techniki DISE, może drażnić górne drogi oddechowe i zakłócać sen pacjenta.
Odpowiednia ocena wszystkich miejsc niedrożności z wykorzystaniem zarówno DISE jak i klasyfikacji VOTE ma na celu poprawę skuteczności leczenia pacjentów z OSAS. Tylko chirurgiczna ablacja wszystkich przeszkód znalezionych podczas wykonywania badania DISE może dać odpowiedź na pytanie, czy znalezione niedrożności były przyczyną zespołu bezdechu sennego.
Technika DISE jest bezpieczna i łatwa do wykonania, umożliwia indywidualne opracowanie planu leczenia. Endoskopia wykonywana w czasie snu farmakologicznego jest cennym uzupełnieniem diagnostyki zaburzeń oddychania w czasie snu. Nowoczesne środki anestezjologiczne zmniejszają ryzyko badania. Zastosowane systemy klasyfikacji są subiektywne i wymagają zobiektywizowania.
Piśmiennictwo
1. Young T, Finn L: Epidemiological insights into the public health burden of sleep disordered breathing: sex differences in survival among sleep clinical patients. Thorax 1998; 53 suppl. 3: 516-519.
2. Viana Ada C Jr, Thuler LC, Araújo-Melo MH: Drug-induced sleep endoscopy in the identification of obstruction sites in patients with obstructive sleep apnea: a systematic review. Braz J Otorhinolaryngol. 2015; 81: 439-446.
3. Altintaş A, Olgun B, Yegin Y et al.: Interobserver Consistency of Drug-Induced Sleep Endoscopy in Diagnosing Obstructive Sleep Apnea Using a VOTE Classification System. J Craniofac Surg. 2017; 1: 1-10.
4. Hasiec A, Szumowski Ł, Walcza F: Obturacyjny bezdech – senny zabójca. For Med Rodz 2012; 6 (3), 103-114.
5. Schwartz AR, Patil SP, Laffan AM et al.: Obesity and obstructive sleep apnea: pathogenic mechanisms and therapeutic approaches. Proc Am Thor Soc 2008; 5(2); 185-192.
6. Ciuba I: Obturacyjny bezdech senny. Zam St Mat; 2011; 13(1): 109-115.
7. Jagannathan R, Seixas A, St-Jules D et al.: Systems Biology Genetic Approach Identifies Serotonin Pathway as a Possible Target for Obstructive Sleep Apnea: Results from a Literature Search Review. Sleep Disord 2017; 2017: 6768323.
8. Atulkumar Shah J, George A, Chauhan N, Francis S: Obstructive Sleep Apnea.Role of an Otorhinolaryngologist; Indian J Otolaryngol Head Neck Surg 2016; 68(1): 71-74.
9. Lee CH, Kim DK, Kim SY et al.: Changes in Site of Obstruction in Obstructive Sleep Apnea Patients According to Sleep Position: A DISE Study. Laryngoscope 2015; 125: 248-254.
10. Ravesloot MJ, de Vries N: One hundred consecutive patients undergoing drug-induced sleep endoscopy: results and evaluation. Laryngoscope 2011; 121(12): 2710-2716.
11. Kezirian EJ, Hohenhorst W, de Vries N: Drug-induced sleep endoscopy: the VOTE classification. Eur Arch Otorhinolaryngol 2011; 268(8): 1233-1236.
12. Croft CB, Pringle M: Sleep nasendoscopy: a technique of assessment in snoring and obstructive sleep apnoea. Clin Otolaryngol Allied Sci 1991; 16: 504-509.
13. Blumen MB, Latournerie V, Bequignon E et al.: Are the obstruction sites visualized on drug-induced sleep endoscopy reliable? Sleep Breath 2015; 19: 1021-1026.
14. Grochowski T, Kukwa W, Krzeski A et al.: Badanie endoskopowe gardła dolnego we śnie farmakologicznym. Mag Otolar 2014; 50(13): 57-61.
15. Vicini C, De Vito A, Benazzo M et al.: The nose oropharynx hypopharynx and larynx (NOHL) classification: A new system of diagnostic standardized examination for OSAHS patients. Eur Arch Otorhinolaryngol 2012; 269(4): 1297-1300.
16. Roblin G, Williams AR, Whittet H: Target-controlled infusion in sleep endoscopy. Laryngoscope 2001; 111: 175-176.
17. Kotecha BT, Hannan SA, Khalil HM et al.: Sleep nasendoscopy: A 10-year retrospective audit study. Eur Arch Otorhinolaryngol 2007; 264(11): 1361-1367.
18. Ryan C, Borek BS, Erica R at al.: Quantitative Airway Analysis During Drug-Induced Sleep Endoscopy for Evaluation of Sleep Apnea. Laryngoscope 2012; 122(11): 2592-2599.
19. Torre C, Camacho M, Liu SY et al.: Epiglottis collapse in adult obstructive sleep apnea: a systematic review. Laryngoscope 2016; 126(2): 515-523.
20. Yegïn Y, Çelik M, Kaya KH et al.: Comparison of drug-induced sleep endoscopy and Müller’s maneuver in diagnosing obstructive sleep apnea using the VOTE classification system. Braz J Otorhinolaryngol. 2017; 83(4): 445-450.
21. De Vito A, Agnoletti V, Berrettini S et al.: Drug-induced sleep endoscopy: conventional versus target controlled infusion techniques – a randomized controlled study. Eur Arch Otorhinolaryngol 2011; 268: 457-462.
22. Witkowska M, Karwacki Z, Rzaska M et al.: Porównanie docelowej infuzji kontrolowanej i anestezji całkowicie dożylnej z użyciem propofolu i remifentanylu do operacji mikrodyskoidektomii w odcinku lędźwiowym kręgosłupa; Anest Int Ter 2012, 44:(3), 156-163.
23. Lo YL, Ni YL, Wang TY et al.: Bispectral Index in Evaluating Effects of Sedation Depth on Drug-Induced Sleep Endoscopy. JCSM 2015; 11(9): 1011-1020.
24. Myles PS, Leslie K, McNeil J et al.: Bispectral index monitoring to prevent awareness during anaesthesia: the B-Aware randomised controlled trial. Lancet 2004; 363(9423): 1757-1763.
25. Safiruddin F, Koutsourelakis I, de Vries N: Analysis of the influence of head rotation during drug-induced sleep endoscopy in obstructive sleep apnea. Laryngoscope 2014; 124: 2195-2199.
26. Carrasco-Llatas M, Agostini-Porras G, Cuesta-González MT, Rodrigo-Sanbartolomè A et al.: Drug-induced sleep endoscopy: a two drug comparison and simultaneous polysomnography. Eur Arch Otorhinolaryngol 2014; 271(1): 181-187.
27. Dijemeni E, Kotecha B: Drug-Induced Sedation Endoscopy (DISE) DATA FUSION system: clinical feasibility study. Eur Arch Otorhinolaryngol 2017; 1: 1-14.
28. Vroegop AV, Vanderveken OM, Wouters K et al.: Observer variation in drug-induced sleep endoscopy: experienced versus nonexperienced ear, nose, and throat surgeons. Sleep 2013; 36(6): 947-953.







