© Borgis - Postępy Fitoterapii 1/2016, s. 20-32
*Tadeusz Wolski1, Tomasz Baj1, Katarzyna Wolska2, Wanda Zwolan1
Badania anatomiczne części nadziemnych i podziemnych rzepienia pospolitego Xanthium strumarium L. oraz analiza chromatograficzna frakcji garbnikowej
The anatomical investigations of aerial and underground parts of rough cocklebur (Xanthium strumarium L.) and chromatographic analysis of tannin fraction
1Katedra i Zakład Farmakognozji z Pracownią Roślin Leczniczych, Uniwersytet Medyczny w Lublinie
Kierownik Zakładu: dr hab. n. farm. Grażyna Zgórka
2Studia Doktoranckie, I Wydział Lekarski z Oddziałem Stomatologicznym, Uniwersytet Medyczny w Lublinie
Kierownik Studiów Doktoranckich: prof. dr hab. n. med. Grzegorz Dzida
Summary
The present work is a continuation of research on species Xanthium strumarium L. In the previous sections describe its pharmacological properties, phytochemical analysis of phenolic compounds, sterols and triterpenes and analyze the content and composition of essential oil. The first time the raw material was carried out systematic anatomical studies stems, leaves and roots. It has been shown that in all the examined organs are secreted structure in the form of channels, vascular tissue and hair. In the present discharge channels. The stem was a small secretory channels that form two rings external and internal. The root canals are secreted in the cortex secondary. The results of analysis of tannins in the examined organs Xanthium strumarium L. are as follows: the highest percentage shows the herb 10.54%, fruits 7.14% and the lowest roots 3.35%. TLC analysis allowed to identify the presence of phenolic acids: caffeic, gallic and ferulic in all the tested extracts, and in addition to identify the chlorogenic acid from extracts of the herb, fruit and roots following acid hydrolysis. HPLC analysis of tannin fractions after hydrolysis of extracts from the herb, fruit and roots revealed the presence of the following phenolic acids in the herb: gallic, caffeic, protocatechuic, syringic, chlorogenic, ferulic and vanilic; in fruits gallic, caffeic, protocatechuic, chlorogenic, ferulic and vanillic; and in the roots of gallic, caffeic, chlorogenic, ferulic and vanilic acids.

Wstęp
Prezentowana praca stanowi kontynuację badań nad gatunkiem Xanthium strumarium L. W poprzednich częściach opisano jego właściwości farmakologiczne, analizę fitochemiczną związków fenolowych, steroli i triterpenów oraz analizę zawartości i składu olejku eterycznego (1-3).
Gatunek Xanthium strumarium L. występuje w różnych siedliskach: na polach uprawnych, pastwiskach, nieużytkach, poboczach, przydrożach, torfowiskach, brzegach jezior, rzek, stawów i strumieni, jak też w miejscach wilgotnych zalewanych przez powodzie (1, 4-9). Rodzaj Xanthium najbardziej rozpowszechniony jest w strefie umiarkowanej. Spotkać go można niemal na całym świecie. Rozmieszczenie Xanthium strumarium L. przedstawiono na rycinie 1. Jednym z powodów znacznego rozprzestrzeniania się tej rośliny jest zdolność do samozapylania. Rzepień najczęściej rośnie w małych skupiskach, na glebach brunatnych i pseudobielicowych, wytworzonych z piasków luźnych i słabo gliniastych o odczynie słabo kwaśnym i obojętnym (10, 11). W niedogodnych warunkach, na suchych słabych ziemiach, może urosnąć zaledwie kilka centymetrów, potrafi też przetrwać suszę, a następnie wydać nasiona. Jak podaje piśmiennictwo, Xanthium strumarium L. można spotkać także na Lubelszczyźnie, zwłaszcza w północno- i południowo-zachodniej jej części (ryc. 2) (11). Obraz całej rośliny Xanthium strumarium L. przedstawia rycina 3.
Ryc. 1. Rozmieszczenie Xanthium strumarium L. na świecie (opracowanie własne)
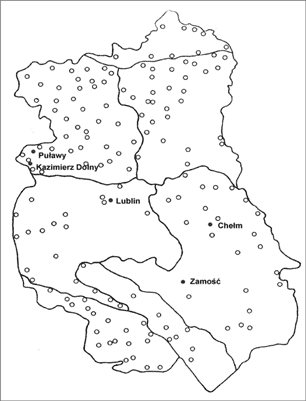
Ryc. 2. Występowanie Xanthium strumarium L. na Lubelszczyźnie (wg 11)

Ryc. 3. Xanthium strumarium L. (11)
Cel pracy
Celem pracy były badania anatomiczno-morfologiczne oraz analiza chromatograficzna frakcji garbnikowej.
Materiał i metody
Surowiec do badań stanowiły organy nadziemne – ziele (liście i łodygi), owoce oraz korzenie rzepienia pospolitego Xanthium strumarium L. Surowiec w pierwszym roku badań pochodził ze stanu naturalnego i zebrano go w okolicach Kazimierza Dolnego nad Wisłą, a w dalszych latach z upraw w Ogrodzie Roślin Leczniczych Katedry i Zakładu Farmakognozji z Pracownią Roślin Leczniczych Uniwersytetu Medycznego w Lublinie (ryc. 4).

Ryc. 4. Poletka doświadczalne rzepienia pospolitego Xanthium strumarium L. w Ogrodzie Roślin Leczniczych Katedry i Zakładu Farmakognozji z Pracownią Roślin Leczniczych UM w Lublinie
Surowiec do badań pozyskiwano z roślin jednorocznych, które zbierano w drugiej połowie września, następnie suszono go w cieniu i przewiewie oraz rozdrabniano w zależności od potrzeb i przygotowywano do badań. Prowadzone analizy trwały trzy lata.
Badania anatomiczne
Badania obejmowały części nadziemne rzepienia pospolitego – łodygę i liść, oraz podziemne – korzeń. Tkanki roślinne badano na przekrojach poprzecznych wykonanych ze świeżego materiału roślinnego utrwalonego w FFA (etanol 50% + kwas octowy + formalina 40% (990:5:5)) (12). W celu zabarwienia struktur komórkowych i eksudatów wydzielniczych, w preparatach sporządzonych ze świeżych łodyg i liści zastosowano testy histochemiczne: płyn Lugola, Sudan III oraz błękit toluidynowy (13).
Mikroskopia świetlna
Fragmenty łodyg i liści utrwalano w 2,5% aldehydzie glutarowym w 0,1 m buforze kokodylanowym (pH = 7,4). Po dehydratacji próbki przenoszono do tlenku propylenu i zatapiano w żywicy SPURR. Skrawki tkanek roślinnych o grubości 0,5-0,7 μm uzyskiwano przy użyciu ultramikrotomu Reichert Ultracut S (13).
Skaningowa mikroskopia elektronowa (SEM)
Po utrwaleniu w aldehydzie glutarowym i odwodnieniu część próbek przenoszono do acetonu. Następnie suszono je w ciekłym CO2 i napylano złotem przy użyciu CS 100 Sputter Coater. Obserwacje wykonywano przy użyciu mikroskopu BS-340 Tesla. Do barwienia stosowano 1% roztwór błękitu metylenowego z azurem II w wodnym roztworze czteroboranu sodu (13).
Oznaczenie ilościowe garbników
W celu wyizolowania frakcji garbników z ziela, owoców i korzeni rzepienia pospolitego sporządzono wyciągi wodne stosując klasyczną ekstrakcję typu ciecz-ciało stałe. Oznaczenie ilościowe zawartości garbników prowadzono zgodnie z metodyką opisaną w FP IV (15).
Izolacja frakcji garbnikowej
Wyciągi wodne otrzymane według procedury (15) ekstrahowano w układzie ciecz-ciecz porcjami octanu etylu (10 x 10 ml). Następnie zebrane frakcje octanowe osuszano bezwodnym siarczanem sodu. Po przesączeniu oddestylowano rozpuszczalnik na wyparce obrotowej. Suchą pozostałość rozpuszczano w 10 ml metanolu. Tak uzyskane próbki poddano badaniom chromatograficznym TLC i HPLC (14).
Hydroliza frakcji garbników
W celu wyodrębnienia związków fenolowych – podstawowych składników garbników hydrolizujących – przeprowadzono hydrolizę kwasową surowca. Odważano po 10 g każdego z organów rzepienia pospolitego i umieszczano je w kolbach okrągłodennych, do których dodawano po 200 ml 4% roztworu kwasu siarkowego (VI), po czym ogrzewano przez 4 godziny na wrzącej łaźni wodnej pod chłodnicą zwrotną. Otrzymane hydrolizaty ostudzono, przesączono i ekstrahowano eterem dietylowym (10 x 10 ml). Połączone wyciągi eterowe osuszono bezwodnym siarczanem sodu, przesączono, po czym oddestylowano rozpuszczalnik do sucha. Suchą pozostałość rozpuszczono w 10 ml metanolu i poddano analizie TLC (14, 16-18).
Analiza TLC garbników
Analizę jakościową TLC frakcji wyodrębnionych zgodnie z metodyką opisaną powyżej, a zawierającą związki garbnikowe oraz kwasy fenolowe uwolnione z połączeń garbnikowych w wyniku hydrolizy kwasowej, wykonano na płytkach pokrytych żelem krzemionkowym Si60F254, celulozą oraz poliamidem. Podczas rozwijania stosowano technikę jednokierunkową. Identyfikację prowadzono przez porównanie wartości Rf związków występujących w badanych frakcjach z wartościami Rf wzorców.
Chromatogramy rozwijano w następujących układach elucyjnych:
1. dla fazy stacjonarnej z żelem krzemionkowym:
– toluen-mrówczan etylu-kwas mrówkowy, 5 + 4 + 1 (v/v) (19),
– octan etylu-kwas mrówkowy-kwas octowy-woda, 100 + 11 + 11 + 27 (v/v) (20),
– eter diizopropylowy-kwas mrówkowy 98%, 9 + 1 (v/v) (układ własny),
– chloroform-octan etylu-kwas mrówkowy 98%, 5 + 4 + 1 (v/v) (21),
– n-butanol-kwas octowy-woda, 4 + 1 + 5 (v/v) (22),
2. dla fazy stacjonarnej z celulozy:
– dioksan-woda, 10 + 1 (v/v) (układ własny),
– kwas octowy-woda, 15 + 85 (v/v) (układ własny),
– chloroform-kwas octowy-woda, 90 + 45 + 6 (v/v) (23),
3. dla fazy stacjonarnej z poliamidem:
– metanol-woda-lodowaty kwas octowy, 20 + 12,5 + 1 (v/v) (21),
– metanol-woda-dioksan-kwas mrówkowy 98%, 20 + 12,5 + 1 + 1 (v/v) (22).
Rozwinięte chromatogramy wizualizowano pod lampą UV przy długościach fali λ = 254 nm i λ = 366 nm oraz przy użyciu Videostore (Camag, Szwajcaria). Płytki chromatograficzne wywołano przez spryskanie zdiazowanym kwasem sulfanilowym.
Wysokosprawna chromatografia HPLC ekstraktów garbnikowych
Przed przeprowadzeniem analizy HPLC próbki poddano oczyszczeniu metodą ekstrakcji do fazy stałej (SPE) na kolumienkach z fazą oktadecylową RP C18 zgodnie z wcześniej opisaną metodyką (24).
Analiza frakcji garbnikowej po hydrolizie kwasowej metodą HPLC
Analizę chromatograficzną HPLC wykonano w układzie faz odwróconych stosując chromatograf cieczowy typu LaChrom firmy Merck z detektorem diodowym DAD (L-7450), pompą dozującą (L-7100), degazerem (L-7612), pętlą dozującą 20 μl, termostatem (L-7360), dozownikiem Rheodyne, kolumną stalową LiChrospher 100 RPClS o wymiarach 250 mm x 4 mm wypełnioną fazą stacjonarną o średnicy ziarna 5 μm. Analizę prowadzono w temp. 25°C. Jako fazę rozwijającą stosowano układ metanol-woda (25 + 75, v/v) z dodatkiem 1% (v/v) kwasu octowego. Szybkość przepływu wynosiła 0,8 ml/min, a wielkość nastrzyku – 20 μl. Identyfikację kwasów fenolowych przeprowadzono porównując ich czasy retencji tR z wzorcami oraz spektroskopowo, wyznaczając ich widma w zakresie UV (219-400 nm) (25, 26). Pełną analizę frakcji garbnikowej wykonano po hydrolizie kwasowej.
Budowa anatomiczna łodygi, liścia i korzenia rzepienia pospolitego
Anatomia łodygi
Łodyga rzepienia na przekroju poprzecznym ma kształt lekko spłaszczony. Okryta jest jednowarstwową epidermą, wytwarzającą włoski mechaniczne. Komórki epidermy mają silnie zgrubiałe ściany zewnętrzne z wyraźnie wyodrębnioną warstwą kutykuli. Włoski mechaniczne są masywne, wielokomórkowe, jednorzędowe.
Warstwę wzmacniającą łodygi tworzy kolenchymatyczna hypoderma. Komórki kolenchymy kątowej obejmują 7-8 warstw. W kolenchymie widoczne są liczne chloroplasty. W parenchymie kory pierwotnej rozmieszczone są niewielkie kanały wydzielnicze, które tworzą dwa pierścienie. Zewnętrzny położony jest bliżej kolenchymy, wewnętrzny w sąsiedztwie endodermy. Kanał wydzielniczy ograniczony jest jedną warstwą epitelu wydzielniczego, a wokół otaczają go komórki miękiszu różnej wielkości. Endoderma w łodydze rzepienia wyraźnie się wyodrębnia z powodu zgrubiałych ścian komórkowych. Falistą linią opasuje od zewnątrz wiązki przewodzące.
Położone w walcu osiowym pasma wiązek przewodzących są oddzielone od siebie miękiszem i tworzą pojedynczy pierścień. Kolateralne, otwarte wiązki przewodzące mają różne rozmiary. W czasie rozrastania się łodygi na grubość, pomiędzy dużymi wiązkami powstają wiązki waskularne mniejszych rozmiarów.
Centralną część łodygi zajmuje duży rdzeń, utworzony z komórek miękiszowych o wielkości podobnej do komórek miękiszu kory pierwotnej.
Omawiana powyżej budowa anatomiczna łodygi rzepienia pospolitego została przedstawiona na rycinach 5-9.
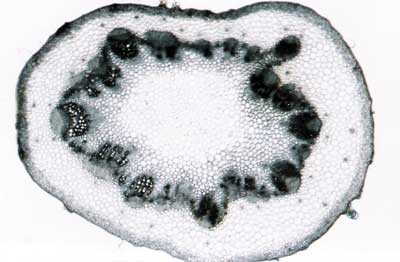
Ryc. 5. Przekrój poprzeczny łodygi rzepienia pospolitego (x 20)
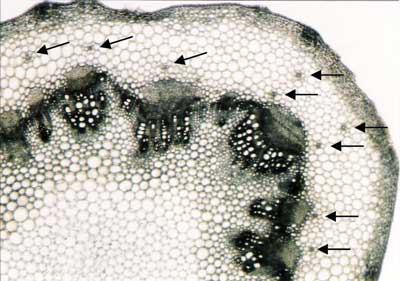
Ryc. 6. Fragment przekroju poprzecznego łodygi rzepienia pospolitego z widocznymi kanałami wydzielniczymi (strzałki) (x 35)

Ryc. 7. Fragment przekroju poprzecznego kory pierwotnej łodygi rzepienia pospolitego z widoczną epidermą (e), kolenchymą kątową (k), parenchymą (p) i kanałami wydzielniczymi (strzałki) (lewe zdjęcie x 190, prawe zdjęcie x 17)

Ryc. 8. Kanał wydzielniczy w korze pierwotnej łodygi (gwiazdka) rzepienia pospolitego z pojedynczą warstwą epitelu wydzielniczego (strzałka) (x 650)
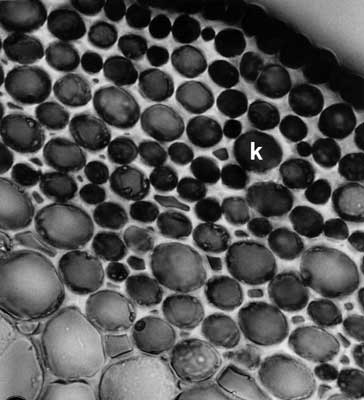
Ryc. 9. Wielowarstwowa kolenchyma kątowa (k) tworząca warstwę hypodermalną w łodydze rzepienia pospolitego (x 350)
Anatomia liścia
Nerw główny liścia rzepienia pospolitego otoczony jest jednowarstwową epidermą, pod którą od strony doosiowej (górnej) i odosiowej (dolnej) występują 2-4 warstwy kolenchymy. Epiderma wytwarza wielokomórkowe włoski mechaniczne. Centralną część nerwu zajmuje duża wiązka przewodząca kolateralna otwarta. Powyżej tej wiązki położone są 3 wiązki o znacznie mniejszych rozmiarach. Blaszka liściowa okryta jest epidermą wytwarzającą liczne, duże włoski mechaniczne. Podobnie jak na łodydze, są one wielokomórkowe, jednorzędowe. Aparaty szparkowe występują w skórce dolnej. Warstwę miękiszu palisadowego rozdzielają duże komórki miękiszu wodonośnego tworzące jasne trójkątne strefy w górnej części liścia. Miękisz gąbczasty składa się z drobnych komórek o luźnym układzie, z wyraźnie zaznaczonymi, jaśniejszymi przestrzeniami międzykomórkowymi.
Budowa anatomiczna liścia rzepienia pospolitego została przedstawiona na rycinach 10-12.

Ryc. 10. Fragmenty przekroju poprzecznego liścia rzepienia pospolitego z widocznym nerwem głównym. Widoczne wiązki przewodzące (strzałki), włoski mechaniczne (t) i warstwy miękiszu wodonośnego (w) rozdzielające miękisz palisadowy (p) (x 87)

Ryc. 11. Fragment przekroju poprzecznego blaszki liściowej rzepienia pospolitego z masywnymi włoskami mechanicznymi (t), miękiszem palisadowym (p), gąbczastym (g) i wodonośnym (w) (x 87)
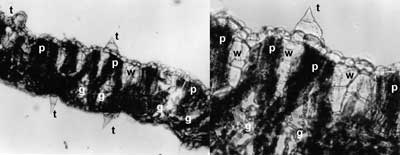
Ryc. 12. Fragment przekroju poprzecznego liścia rzepienia pospolitego z widocznym miękiszem wodonośnym (w) rozdzielającym warstwę miękiszu palisadowego (p) oraz miękiszem gąbczastym (g) (lewe zdjęcie x 80, prawe zdjęcie x 180)
Anatomia korzeni
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
29 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
69 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
129 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 78 zł
Piśmiennictwo
1. Wolski T, Zwolan W, Lewandowska A. Rzepień pospolity (Xanthium strumarium L.) – surowiec zielarski o wielokierunkowym działaniu farmakologicznym. Analiza fitochemiczna związków fenolowych. Post Fitoter 2006; 3:118-30. 2. Wolski T, Zwolan W, Baj T i wsp. Rzepień pospolity (Xanthium strumarium L.) – analiza fitochemiczna steroli i triterpenów. Post Fitoter 2006; 4:170-82. 3. Wolski T, Baj T, Głowniak K i wsp. Rzepień pospolity (Xanthium strumarium L.) – analiza i skład olejku eterycznego. Post Fitoter 2009; 3:152-67. 4. Tymrakiewicz W. Atlas chwastów. PWRiL, Warszawa 1962; 33. 5. Tacik T. Flora polska. Rośliny naczyniowe Polski i ziem ościennych. Tom 12. PWN, Warszawa 1971. 6. Szafer W. Opisy i klucze do oznaczania wszystkich gatunków roślin naczyniowych rosnących w Polsce. PWN, Warszawa 1988; 674-5. 7. Broda B. Zarys botaniki farmaceutycznej. PZWL, Warszawa 1998. 8. Rutkowski L. Klucz do oznaczania roślin naczyniowych Polski niżowej. PWN, Warszawa 1998. 9. Pitcher D. Element stewardship abstract for Xanthium spinosum spiny cocklebur. 2001, http://www.conserveonline.org/2001/05/d/en/xantspi.pdf. 10. Fijałkowski D. Flora roślin naczyniowych Lubelszczyzny. Tom 1. LTN, Lublin 1994; 227. 11. Fijałkowski D. Flora roślin naczyniowych Lubelszczyzny. Tom 2. LTN, Lublin 1995; 612. 12. Broda B. Metody histochemii roślinnej. PZWL, Warszawa 1971; 245. 13. Wolski T, Baj T. Biologia wzrostu i rozwoju dwu odmian dyptamu jesionolistnego (Dictamnus albus L. cv. Albiflores i cv. Rosa Purple) oraz budowa anatomiczno-morfologiczna struktur wydzielniczych, skład olejku eterycznego i analiza ekstraktu. Post Fitoter 2015; 1:21-36. 14. Jerzmanowska Z. Substancje roślinne, metody wyodrębniania. Tom 1. PWN, Warszawa, 1970; 43-71. 15. Farmakopea Polska IV. PZWL, Warszawa 1970. 16. Borkowski B, Miłkowska K. Garbniki, tanoidy i związki pokrewne. III. Elagotaniny. Herba Pol 1996; 43(2):118-26. 17. Borkowski B, Miłkowska K. Garbniki, tanoidy i związki pokrewne. IV. Kawolidy. Herba Pol 1996; 42(3):174-82. 18. Borkowski B, Miłkowska K. Garbniki skondensowane. Herba Pol 1997; 43(1):73-97. 19. Borkowski B (red.). Zarys farmakognozji. PZWL, Warszawa 1970. 20. Farmakopea Polska VI. PTFarm, Warszawa 2002. 21. Strzelecka H, Kamińska J, Kowalski J, Walewska E. Chemiczne metody badań roślinnych surowców leczniczych. PZWL, Warszawa 1987. 22. Borkowski B (red.). Chromatografia cienkowarstwowa w analizie farmaceutycznej. PZWL, Warszawa 1973; 234. 23. Lewandowska A. Analiza związków fenolowych występujących w rzepieniu pospolitym (Xanthium strumarium L.) ze szczególnym uwzględnieniem flawonoidów i garbników. Praca magisterska, AM w Lublinie 2006. 24. Głowniak K, Zgórka G, Dragan T. Zastosowanie metody SPE-HPLC do rozdziału i oznaczenia fenolokwasów w wyciągach i preparatach jeżówki (Echinacea sp.). Farm Pol 1993; 20:28-33. 25. Nollet LML (ed.). Food Analysis by HPLC. Marcel Dekker, New York 2002. 26. Brandsteterova E, Ziakova-Caniova A. Phenolic acids in natural plants: Analysis by HPLC. Encyclopedia of Chromatography, CRC Press 2005. 27. Davis WE. The development of dormancy in seed of cocklebur (Xanthium). Am J Bot 1930; 2:56-9. 28. Zjemlińskij SE. Liekarstwiennyje Rastienija. MOIP, Moskwa 1949. 29. Lersten NR, Curtis JD. Secretory reservoirs (duct) development in Ambrosia trifida (Asteraceae) staminate flowers. Am J Bot 1988; 76(7):1313-23. 30. Maksymowych R, Ledbetter MC. Fine structure of epithelial canal cell in petioles of Xanthium pensylvanicum. Am J Bot 1987; 74:65-73. 31. Polit F, Sacchetti G, Bruni A. Distribution of internal secretory structures in Tagets patula (Asteraceae). Nord J Bot 1995; 15:197-205. 32. Lersten NR, Curtis JD. Polyacetylene reservoir (duct) development in Ambrosia trifida (Asteraceae) staminate flowers. Am J Bot 1989; 74:65-73. 33. Seaman FC. Sesquiterpene lactones as taxonomic characters in Asteraceae. Bot Rev 1982; 48:121-595. 34. Kohlműnzer S. Farmakognozja. PZWL, Warszawa 2000. 35. Dasgupta J, Kundu BC. Pharmacognostic studies of Xanthium strumarium Linn. root. Planta Med 1963; 11:470-8. 36. Śliwiński E, Salisbury FB. Cross-section through an internodium of a Xanthium strumarium (Burweed) shoot. 2003, http://www.biologie.uni-hamburg.de/b-online/e06/rastxant.htm. 37. Khafagy SM, Sabry NN, Metwally AM, el-Naggar SF. Phytochemical investigation of Xanthium strumarium. Planta Med 1974; 26(1):75-8. 38. Pitcher D. The Nature Conservancy Element Stewardship Abstract For Xanthium strumarium. 1989, http://www.conserveonline.org/2001/05/d/en/xantstr.pdf>. 39. Mowszowicz J. Przewodnik do oznaczania krajowych roślin zielarskich. PWRiL, Warszawa 1983; 397-8. 40. Mowszowicz J. Krajowe chwasty polne i ogrodowe. Przewodnik do oznaczania. PWRiL, Warszawa 1986. 41. Świejkowski L. Rośliny lecznicze i przemysłowe. Klucz do oznaczania. WRW, Libra, Warszawa 1990; 439. 42. Lee JM. Common Cocklebur. Xanthium strumarium. Iowa State University, Agronomy Department – Weed Species reports. 1996, http://www.agron.iastate.edu/weed/WeedBiolLibrary/u4cocklel.html. 43. Broda B, Mowszowicz J. Przewodnik do oznaczania roślin leczniczych, trujących i użytkowych. PZWL, Warszawa 2000; 693-4. 44. Lloyd S. Bathurst burr. Farmnote. Department of Agriculture, Western Australia 2000, http://www.agric.wa.gov.au/agency/Pubns/farmnote/2000/fo4100.html. 45. Sarwa AJ. Wielki leksykon roślin leczniczych. Wyd. Książka i Wiedza, Warszawa 2001; 386-7. 46. Smith AH, Zoetendal E, Mackie RI. Bacterial mechanisms to overcome inhibitory effects of dietary tannins. Microb Ecol 2005; 50:197-205. 47. Ma YT, Huang MC, Hsu F, Chang H. Thianezidione from Xanthium strumarium. Phytochem 1998; 48(6):1083-5. 48. Pashchenko MM, Pivenko GP. Polyphenol substances in Xanthium riparium and Xanthium strumarium. Farm Zh 1970; 25(6):41-3.












