© Borgis - Postępy Nauk Medycznych 5/2012, s. 406-412
*Tomasz Jargiełło1, Michał Sojka1, Andrzej Wolski2, Radosław Krupiński2, Michał Przyszlak1, Paweł Poluha1, Małgorzata Szczerbo-Trojanowska1
Implantacja stentgraftów u chorych z zagiętymi szyjami tętniaków aorty brzusznej – planowanie zabiegów, wyniki i powikłania
Stentgraft implantations in patients with angulated neck of AAA – procedure planning, outcomes and complications
1Zakład Radiologii Zabiegowej i Neuroradiologii Uniwersytetu Medycznego w Lublinie
Kierownik Zakładu: prof. dr hab. med. Małgorzata Szczerbo-Trojanowska
2Oddział Chirurgii Naczyń Samodzielnego Publicznego Szpitala Klinicznego nr 4 w Lublinie
Ordynator Oddziału: dr hab. med. Andrzej Wolski
Streszczenie
Wstęp. Już od początku stosowania stentgraftów zauważono, że szyja tętniaka aorty brzusznej (TAB) zbyt szeroka lub zbyt krótka, szyja z obecnością skrzeplin lub o nadmiernie uwapnionych ścianach czy w końcu mocno zagięta stanowi główny czynnik ryzyka niepowodzenia leczenia, czyli nieszczelności stentgraftu.
Materiał i metody. W latach 2006-2011 wykonano 405 zabiegów implantacji stentgraftów aortalno-biodrowych chorych z TAB, w tym u 92 chorych (23%), u których stwierdzono zagięcie szyi pod kątem > 60°. Wszystkie leczone TAB miały średnicę > 50 mm (średnio 59 mm). Średnica szyi tętniaków wynosiła od 23 do 30 mm (średnio 27 mm), zaś długość od 10 do 45 mm (średnio 23 mm). Pod względem pomiarów zagięcia szyi tętniaka chorych podzielono na dwie grupy: z zagięciami mniejszego stopnia (60-80°) i z zagięciami większego stopnia (> 80°). Stosowano trzy typu stentgraftów: Aorfix, Excluder i Zenith.
Wyniki. U wszystkich 92 chorych implantacja zaprojektowanych wcześniej stentgraftów powiodła się. Nie doszło do konieczności tzw. konwersji chirurgicznej. W okresie około zabiegowym (30 dni) doszło do reinterwencji u 2 chorych, skutecznie leczono zagięcie ramienia biodrowego i aortalnego stentgraftów. W dalszej obserwacji 12 i 24-miesięcznej nie stwierdzono zgonów z powodu pęknięcia TAB, zacieki typu I-go odnotowano u 3 chorych.
Wnioski. Zgięcie szyi TAB > 60° nie stanowi przeciwwskazania w kwalifikacji chorego do zabiegów implantacji stentgraftów. Właściwe dobranie typu i rozmiarów stentgraftu pozwala uzyskać podobne wyniki powodzenia technicznego i trwałości wyłączenia TAB, jak u chorych bez zagięć szyi.
Summary
Introduction. It was noticed from the beginning of the use of stentgrafts for AAA treatment, that aneurysms’ neck is the main risk factor for unsuccessful procedure (endoleaks), especially when too broad, too short, calcified, with extensive trombi or finally significantly angulated.
Material and methods. In the years 2006-2011, 405 EVAR procedures were performer, including 92 patients (23%), in whom aortic neck angulation u > 60° was found. All treated AAAs were > 50 mm in diameter (mean 59 mm). Diameter of aortic neck was from 23 to 30 mm (mean 27 mm), and its length was from 10 to 45 mm (mean 23 mm). According to neck angulation patients were divided into two groups: with lower grade angulation (60-80°) and with higher grade angulation (> 80°). We used three different types of stentgrfats: Aorfix, Excluder and Zenith.
Results. In all 92 patients stentgraft implantations were as planned. There were no surgical conversions. In peri operational period (30 days) reinterventions were needed in 2 patients, we successfully treated endovascularly kinkings of aortic arm and iliac arm respectively. In a long-term (12 and 24 months) follow-up there were no deaths due to AAA rupture but type I endoleaks were noticed in 3 patients.
Conclusions. AAA neck angulation > 60° is not a contraindication in qualifying patients for endovascular stentgrafting procedures. Proper selection of stentgraft type and size allows to obtain similar technical and clinical results when compared with straight neck AAAs.

Wstęp
Wprowadzenie małoinwazyjnych technik wewnątrznaczyniowej implantacji stentgraftów znacząco rozszerzyło możliwości i poprawiło wyniki leczenia chorych z tętniakami aorty brzusznej (TAB) w porównaniu do typowego leczenia chirurgicznego. Obecnie, większość chorych obciążonych innymi schorzeniami stanowiącymi istotne utrudnienia lub nawet przeciwwskazania do operacji chirurgicznej mogą być z powodzeniem leczeni metodami wewnątrznaczyniowymi. Doświadczenia ostatnich lat wykazały, że sukces metod wewnątrznaczyniowych w leczeniu TAB wiąże się głównie z prawidłową kwalifikacją chorych pod względem anatomicznym oraz właściwym doborem stentgraftu (1, 2). Jednak, oprócz ewidentnych zalet opisywana metoda ma także swoje ograniczenia. Głównym przeciwwskazaniem do implantacji stentgraftu są niekorzystne warunki anatomiczne, a wśród nich szczególne miejsce zajmuje tzw. szyja tętniaka, czyli odcinek aorty brzusznej pomiędzy tętnicami nerkowymi a workiem tętniaka. Już od początku stosowania stentgraftów zauważono, że szyja TAB zbyt szeroka lub zbyt krótka, szyja z obecnością skrzeplin lub o nadmiernie uwapnionych ścianach, czy w końcu mocno zagięta stanowi główny czynnik ryzyka niepowodzenia leczenia, czyli nieszczelności stentgraftu. Nieszczelność w części proksymalnej stentgraftu określana jako zaciek typu Ia jest najpoważniejszym z możliwych niepowodzeń zabiegu wewnątrznaczyniowego. Zaciekanie krwi do worka tętniaka może powodować jego powiększanie się i w rezultacie pęknięcie tętniaka. Zaciek typu Ia może powstać już w trakcie zabiegu lub bezpośrednio w okresie około zabiegowym, jest wówczas wynikiem nieprawidłowej kwalifikacji anatomicznej lub złego doboru stentgraftu. Zacieki Ia pojawiające się w dalszej obserwacji mogą być wynikiem rozwoju tętniaka w postaci poszerzania się szyi; taki mechanizm nie jest możliwy do przewidzenia i na szczęście zdarza się stosunkowo rzadko. Inny mechanizm powstawania odległych zacieków typu Ia to migracja źle dobranego stentgraftu (typ, średnica) lub implantacja stentgraftu do szyi ze skrzeplinami lub zwapnieniami (3-5). Wraz ze wzrostem doświadczenia operatorów oraz rozwojem technologii stosowanych przy produkcji stentgraftów, leczenie wewnątrznaczyniowe TAB można dziś proponować większej niż kiedyś grupie chorych. Wymaga to jednak ciągłych obserwacji i badań naukowych, w celu określenia nowoczesnych kryteriów kwalifikacji chorych i tętniaków do małoinwazyjnego leczenia wewnątrznaczyniowego (6-8).
Dlatego, celem przedstawianej pracy jest ocena powodzenia technicznego oraz ocena wyników i powikłań w obserwacji rocznej pod kątem szczelności implantowanych stentgraftów aortalno-biodrowych u chorych z tętniakami aorty brzusznej i zagiętą szyją tętniaka pod kątem > 60°.
Materiał i metody
W okresie 5 lat (2006-2011) wykonano 405 wewnątrznaczyniowych zabiegów implantacji stentgraftów aortalno-biodrowych chorych z tętniakami aorty brzusznej, w tym u 92 chorych (23%), u których stwierdzono zagięcie szyi TAB pod kątem > 60°. W badanej grupie 92 chorych było 35 kobiet i 57 mężczyzn w wieku od 58 do 83 lat (średni wiek 71 lat). Wszyscy leczeni chorzy mieli wykonane przed zabiegiem badanie arteriograficzne z cewnikiem kalibrowanym oraz tomografię komputerową. Wszystkie leczone tętniaki brzuszne miały średnicę > 50 mm – od 52 do 87 mm (średnio 59 mm). Średnica szyi tętniaków wynosiła od 23 do 30 mm (średnio 27 mm), zaś długość – od 10 do 45 mm (średnio 23 mm). Pomiary długości szyi pochodziły z arteriografii, a pomiary średnicy oraz ocena zwapnień i skrzeplin w obrębie szyi TAB z obrazów tomografii komputerowej. Pod względem pomiarów zagięcia szyi tętniaka, chorych podzielono na dwie grupy: z zagięciami mniejszego stopnia (60-80°) i z zagięciami większego stopnia (> 80°) – (ryc. 1A, B, C; ryc. 2A, B, C, D; ryc. 3A, B, C, D). Szczegółowe dane dotyczące morfologii szyi tętniaków w badanej grupie chorych zawarto w tabeli 1.
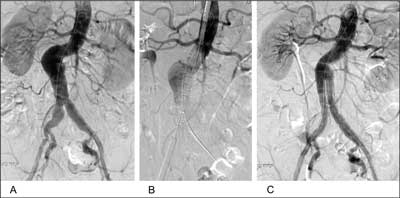
Ryc. 1. Mężczyzna, lat 68, z podwójnie zagiętą, długą szyją tętniaka (największe zagięcie około 90°) – implantowano stentgraft z umocowaniem nadnerkowym typu Zenith. A – arteriografia wyjściowa; B – arteriografia kontrolna, celowanie położenia stentgraftu tuż poniżej tętnic nerkowych; C – arteriografia kontrolna po implantacji stentgraftu, dokładne wymiarowanie pozwoliło na umieszczenie ramion biodrowych stentgraftu tuż powyżej odejść tętnic biodrowych wewnętrznych przy wyraźnym poszerzeniu tętnic biodrowych wspólnych.
Tabela 1. Morfologia szyi TAB w grupie badanej.
inne cechy
morfologii
szyi TAB | wszyscy chorzy
92 (100%) | zagięcie szyi
60-80°
51 (55,4%) | zagięcie szyi
> 80°
41 (44,6%) |
długość szyi
< 20 mm | 23 (25,0%) | 14 (15,2%) | 9 (9,8%) |
długość szyi
> 20 mm | 69 (75,0%) | 37 (40,2%) | 32 (34,8%) |
| zwapnienia w szyi* | 21 (22,8%) | 16 (17,4%) | 5 (5,4%) |
| skrzepliny w szyi** | 18 (19,6%) | 11 (12,0%) | 7 (6,0%) |
*zwapnienia obejmujące 20-50% obwodu szyi
**skrzepliny obejmujące do 30% obwodu szyi
Rozmiary i typy stentgraftów dobierano po przeanalizowaniu obrazów angiografii kalibrowanej i skanów tomografii komputerowej. Stosowano trzy typy stentgraftów: Aorfix (Lombard Medical), Excluder (W.L. Gore) i Zenith (Cook Inc.) – tabela 2. Wszystkie zabiegi były wykonane po chirurgicznym wyłonieniu tętnic udowych wspólnych w pachwinach. Większość implantacji – 88 (95,6%) wykonano w znieczuleniu nadoponowym, pozostałe 4 (4,4%) zabiegi wykonano w znieczuleniu ogólnym. W każdym zabiegu podawano 5000 IU heparyny dożylnie. Do wszystkich zabiegów stosowano niejonowy środek cieniujący Visipaque 320 (GE Healthcare), średnie zużycie środka cieniującego w jednym zabiegu wyniosło około 100 ml.
Tabela 2. Typy stosowanych stentgraftów.
| typ stentgraftu | wszyscy chorzy
92 (100%) | zagięcie szyi
60-80°
51 (55,4%) | zagięcie szyi
> 80°
41 (44,6%) |
| Aorfix (Lombard Medical) | 22 (24,0%) | 4 (4,4%) | 18 (19,6%) |
| Excluder (W.L. Gore) | 12 (13,0%) | 10 (10,8%) | 2 (2,2%) |
| Zenith (Cook Inc.) | 58 (63,0%) | 37 (40,2%) | 21 (22,8%) |
Przed opuszczeniem szpitala wszyscy chorzy mieli wykonane badanie usg metodą Dopplera. Gdy nie stwierdzano nieprawidłowości, kolejne badanie dopplerowskie zalecono po 6 miesiącach, a tomografia komputerowa była wykonywana w przypadkach, gdy stwierdzano cechy nieszczelności (zacieki), objawy chromania kończyn dolnych (zwężenia/niedrożności stentgraftu) oraz w przypadkach powiększania się lub braku zmniejszania worka tętniaka, odpowiednio do wykrycia tych nieprawidłowości lub po 12 miesiącach. W okresie pooperacyjnym chorzy otrzymywali ASA w jednorazowej dawce dziennej 75-100 mg (do końca życia) i clopidogrel – 75 mg jeden raz dziennie (przez trzy miesiące). Nie stosowano preparatów heparyny po zabiegach.
Wyniki
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
29 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
69 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
129 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 78 zł
Piśmiennictwo
1. Marin ML, Hollier LH, Ellozy SH et al.: Endovascular stent graft repair of abdominal and thoracic aortic aneurysms a ten-year experience with 817 patients. Ann Surg 2003; 238: 586-595.
2. Chaikof EL, Blankensteijn JD, Harris PL et al.: Reporting standards for endovascular aortic aneurysm repair. J Vasc Surg 2002; 35: 1048-1060.
3. Choke E, Munneke G, Morgan R et al.: Outcomes of endovascular abdominal aortic aneurysm repair in patients with hostile neck anatomy. Cardiovasc Intervent Radiol 2006; 29: 975-980.
4. Faries PL, Dayal R, Lin S et al.: Endovascular stent graft selection for the treatment of abdominal aortic aneurysms. J Cardiovasc Surg 2005; 46: 9-17.
5. Albertini JN, DeMasi MA, Macierewicz J et al.: Aorfix stent graft for abdominal aortic aneurysms reduces the risk of proximal type 1 endoleak in angulated necks: bench-test study. Vascular 2005; 13: 321-326.
6. Veith FJ, Baum RA, Ohki T et al.: Nature and significance of endoleaks and endotension: summary of opinions expressed at international conference. J Vasc Surg 2002; 35: 1029-1035.
7. Brener BJ, Faries P, Connelly T et al.: An in situ adjustable endovascular graft for the treatment of abdominal aortic aneurysms. J Vasc Surg 2002; 35: 114-119.
8. Carroccio A, Faries PL, Morrissey NJ et al.: Predicting iliac limb occlusions after bifurcated aortic stent grafting: anatomic and device related causes. J Vasc Surg 2002; 36: 679-684.
9. Albertini JN, Perdikides T, Soong CV et al.: Endovascular repair of abdominal aortic aneurysms in patients with severe angulation of the proximal neck using a flexible stent-graft: European Multicenter Experience. J Cardiovasc Surg 2006; 47: 245-250.
10. Jacobs TS, Won J, Gravereaux EC et al.: Mechanical failure of human implants: a 10-year experience with aortic stent grafts. J Vasc Surg 2003; 37: 16-26.
11. Cao P, Verzini F, Zannetti S et al.: Device migration after endoluminal abdominal aortic aneuerysm repair: analysis of 113 cases with a minimum follow up period of 2 years. J Vasc Surg 2002; 35: 229-235.
12. Robbins M, Kritpracha B, Beebe HG et al.: Suprarenal endograft fixation avoids adverse outcomes associated with aortic neck angulation. Ann Vasc Surg 2005; 19: 172-177.
13. Chaikof EL, Fillinger MF, Matsumura JS et al.: Identifying and grading factors that modify the outcome of endovascular aortic aneurysm repair. J Vasc Surg 2002; 35: 1061-1066.
14. Nevala T, Perälä J, Aho P et al.: Outcome of symptomatic, unruptured abdominal aortic aneurysms after endovascular repair with the Zenith stent-graft system. Scand Cardiovasc J 2008; 42: 178-181.
15. Balasubramaniam K, Hardman J, Horrocks M et al.: The advantages of Aorfix for endovascular repair of abdominal aortic aneurysm. J Cardiovasc Surg 2009; 50: 139-143.
16. Pintoux D, Chaillou P, Azema L et al.: Long-term influence of suprarenal or infrarenal fixation on proximal neck dilatation and stentgraft migration after EVAR. Ann Vasc Surg 2011; 25: 1012-1019.
17. Bastos Gonçalves F, de Vries JP, van Keulen JW et al.: Severe proximal aneurysm neck angulation: early results using the Endurant stentgraft system. Eur J Vasc Endovasc Surg 2011; 41: 193-200.
18. Pitoulias GA, Donas KP, Schulte S et al.: Two-dimensional versus three-dimensional CT angiography in analysis of anatomical suitability for stentgraft repair of abdominal aortic aneurysms. Acta Radiol 2011; 52: 317-323.
19. Kaladji A, Lucas A, Kervio G et al.: Sizing for endovascular aneurysm repair: clinical evaluation of a new automated three-dimensional software Ann Vasc Surg 2010; 24: 912-920.
20. Neri E, Bargellini I, Rieger M et al. Abdominal aortic aneurysms: virtual imaging and analysis through a remote web server. Eur Radiol 2005; 15: 348-352.

