© Borgis - Postępy Nauk Medycznych 12/2010, s. 923-927
*Ewa Makowska
Implantowane kardiowertery-defibrylatory
Implantable cardioverter-defibrillator
Klinika Kardiologii Centrum Medycznego Kształcenia Podyplomowego, Szpital Grochowski, Warszawa
Kierownik Kliniki: prof. dr hab. med. Andrzej Budaj
Streszczenie
Pierwszą implantację automatycznego kardiowertera-defibrylatora (ICD) wykonano 30 lat temu. Od 1993 roku używa się elektrod przezżylnych. Obecne urządzenia posiadają udoskonalone algorytmy rozpoznawania arytmii. Implantacja ICD to podstawowa metoda leczenia chorych zagrożonych nagłym zgonem sercowym. Wykazano korzyść z profilaktycznego stosowania ICD u chorych po zawale serca z istotną dysfunkcją lewej komory. Poszukuje się wskaźników, które pozwolą na wyłonienie spośród nich grupy chorych szczególnie zagrożonych nagłym zgonem.
Problemy kliniczne związane z ICD to burze elektryczne, nieadekwatne interwencje, szybkie zużywanie się elektrod, konieczność usuwania elektrod, częste wymiany urządzenia, powikłania infekcyjne, a także zaburzenia lękowe. Burze elektryczne wymagają hospitalizacji w warunkach intensywnego nadzoru kardiologicznego i niekiedy doraźnego wyłączenia ICD. Najczęstszymi przyczynami nieadekwatnych interwencji są tachyarytmie nadkomorowe, zaburzenia sterowania oraz uszkodzenie elektrody. Zbędne defibrylacje mogą wywołać groźne arytmie, ponadto stanowią stres dla pacjenta i wywołują lęk. Elektrody defibrylujące stosunkowo często ulęgają uszkodzeniom, stwarzając konieczność ich usuwania lub doszczepiania nowych z pozostawieniem starych. Nieczynne elektrody to większe ryzyko infekcji oraz zakrzepicy żylnej. Usuwanie elektrod przez wyspecjalizowane ośrodki jest bezpieczną procedurą. Infekcyjne zapalenie wsierdzia związane z ICD wymaga usunięcia całego układu. Całkowicie podskórny defibrylator nie wymaga stosowania elektrod ani wewnątrzsercowych, ani nasierdziowych. We wszystkich ośrodkach pracownie kontrolujące ICD są niewydolne z powodu stale rosnącej liczby pacjentów. Rozwiązaniem mogą być zdalne kontrole, wykorzystujące do przesyłania danych sieci telefoniczne. Wykazano, że taka metoda kontroli jest bezpieczna i w istotny sposób skraca czas od wystąpienia arytmii do podjęcia koniecznych działań. Zdalna kontrola ICD nie jest uznawana za procedurę i nie jest refundowana przez NFZ.
Summary
The first automatic cardiovereter-defibrillator was implanted 30 years ago. Since 1993 transvenous leads have been used. Current devices have improved algorithm for differentiation of arrhythmias. ICD is the main method of treating patients who are at risk of sudden cardiac death. In patients with a prior myocardial infarction and advanced left ventricular dysfunction prophylactic implantation of ICD improves survival. New methods of prediction of sudden cardiac death are needed to identity a group at the highest risk.
The main clinical problems associated with ICD are electrical storm, inappropriate interventions, short lifetime of leads, necessity of leads removing, frequent device replacement, infective complications and anxiety disorders. Patients with electrical storm need hospitalization in CCU and sometimes switching off ICD. Most frequent causes of inappriopriate interventions are supraventricular tachyarrhythmias, oversensing and lead damage. Unnecessary defibrillations may cause serious arrhythmias, are stressful for patients and evoke anxiety. Defibrillating lead failure occurs relatively often, causing necessity of removing lead or implantation a new one beside an old. Inactive leads enhance a risk of infection and vein thrombosis. Removing of leads in specialized centers is a safe procedure. Infective endocarditis associated with ICD is an indication for removing ICD with leads. Because of growing number of patients with ICD follow-up is one of the main problem in all centers. Remote home monitoring using phone net for data transmission may be a resolution of this problem This method of follow-up is safe and allows more rapid detection of actionable events compared with conventional monitoring. Remote monitoring is not acknowledged as a procedure in Poland and is not refunded.

Historia
W lutym b.r. minęła 30. rocznica wszczepienia pierwszego kardiowertera-defibrylatora ( implantable cardioverter-defibrillator – ICD), choć sama koncepcja automatycznego defibrylatora narodziła się 20 lat wcześniej. Jej autorem był Michael Mirowski, absolwent Akademii Medycznej w Gdańsku, wówczas mieszkający w Izraelu. To on w kilka lat później, w 1969 r. w Baltimore wraz z Mortonem Mowerem skonstruował pierwszy zewnętrzny automatyczny defibrylator. Ich dzieło spotkało się z szeroką krytyką i wątpliwością, czy takie urządzenie można będzie kiedykolwiek zastosować u ludzi.
Początkowo implantacja ICD była zabiegiem chirurgicznym, wymagającym torakotomii i naszycia elektrod nasierdziowych. Samo urządzenie wszczepiano w powłoki brzuszne. W 1993 r. po raz pierwszy zastosowano elektrodę przezżylną. Dalsze lata to okres udoskonalania zarówno elektrod (coraz cieńsze, wyposażone w górne zwoje defibrylujące, wreszcie elektrody dwubiegunowe), jak i samych urządzeń (również coraz mniejsze, wszczepiane w okolice podobojczykową, z coraz lepszymi algorytmami rozpoznawania arytmii).
Obecne zastosowanie ICD to podstawowa metoda leczenia chorych zagrożonych nagłym zgonem sercowym (1). Przerwanie migotania komór wewnętrzną defibrylacją z ICD ilustruje rycina 1.
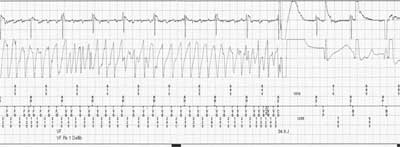
Ryc. 1. Wydruk z pamięci ICD w czasie migotania komór. Górna krzywa – zapis z elektrody przedsionkowej, dolna – z elektrody komorowej. Poniżej markery ułatwiające interpretację zapisu i liczby określające długość cyklu (odstęp pomiędzy kolejnymi pobudzeniami). Elektroda przedsionkowa rejestruje spontaniczną miarową aktywację przedsionków o częstości rytmu 75/min (rytm zatokowy). W tym samym czasie elektroda komorowa rejestruje nieregularne fale migotania komór o częstości rytmu 280-500/min. Defibrylacja wewnętrzna 34,9 J przerywa arytmię.
Korzyści
Dziś nikt już nie ma wątpliwości, że w prewencji wtórnej po nagłym zatrzymaniu krążenia oraz przy udokumentowanym utrwalonym lub niestabilnym hemodynamicznie częstoskurczu komorowym każdemu choremu należy bezwzględnie implantować ICD. Korzyści z takiego postępowania dowiodły badania kliniczne prowadzone w latach dziewięćdziesiątych ubiegłego wieku (AVID, CASH, CIDS), które wykazały istotną redukcję ryzyka śmiertelności po wszczepieniu ICD w porównaniu z leczeniem farmakologicznym (2-5). Wyniki badań MADIT oraz MUSTT rozszerzyły wskazania do ICD na ich profilaktyczne wszczepianie u chorych po zawale serca, z obniżoną frakcją wyrzutową, udokumentowanymi bezobjawowymi nieutrwalonymi częstoskurczami komorowymi oraz indukowanym badaniem elektrofizjologicznym częstoskurczem utrwalonym (6, 7).
Opublikowane w 2002 roku wyniki badania MADIT II wywołały pewną konsternację. Wykazały one, że profilaktyczne wszczepianie kardiowerterów może obejmować jeszcze szerszą populację chorych, mianowicie osoby z pozawałową istotną dysfunkcją lewej komory bez innych czynników ryzyka, gdyż w tej grupie pacjentów implantacja ICD redukuje o ponad 30% ryzyko zgonu, głównie nagłego (8). Ten korzystny efekt utrzymuje się w kilkuletniej obserwacji (9). Zatem u każdego chorego z niską frakcją wyrzutową (≤ 30%) po zawale serca powinno się rozważyć implantację ICD. Wobec tak szerokich wskazań do stosowania kosztownej i obciążonej ryzykiem procedury aktualnie poszukuje się wskaźników, które mogłyby spośród tzw. „populacji osób MADIT II” wyłonić grupę chorych szczególnie zagrożonych nagłym zgonem, którzy muszą otrzymać ICD lub też takich, którzy mimo niskiej frakcji wyrzutowej mają stosunkowo niskie ryzyko zgonu i być może nie potrzebują tego urządzenia. Takimi wskaźnikami mogą być wyznaczniki uszkodzenia układu autonomicznego jak zmienność (HRV) oraz turbulencje (HRT) rytmu serca, a także mikrowoltowa zmienność załamka T (TWA). Ich prognostyczne znaczenie u osób po zawale serca potwierdzono w badaniach (10). Wykazano również istotną wartość prognostyczną scyntygrafii z wykorzystaniem znakowanej jodem-123 metajodobenzylguanidyny u osób z niewydolnością serca w klasie NYHA II i III (11).
Problemy kliniczne
Burze elektryczne
Rosnąca z roku na rok liczba chorych z wszczepionymi ICD powoduje, że coraz częściej stają się oni pacjentami oddziałów kardiologicznych. Główną przyczyną ich hospitalizacji w trybie pilnym są burze elektryczne, czyli powtarzające się (3 lub więcej w ciągu doby) epizody arytmii komorowych z następowymi interwencjami ICD. Chorzy ci wymagają intensywnego nadzoru kardiologicznego, doraźnego stosowania dożylnych leków antyarytmicznych i niekiedy pełnej sedacji, ale też często przeprogramowania czy wyłączenia urządzenia. Lekarze dyżurni oddziałów intensywnej opieki kardiologicznej z konieczności muszą więc opanować podstawowe zasady obsługi programatorów.
Nieadekwatne wyładowania
Jednym z największych problemów u chorych z ICD są nieuzasadnione interwencje urządzenia. Dotyczą one aż 15-20% chorych (12, 13). Najczęstszą ich przyczyną są tachyarytmie nadkomorowe, w dalszej kolejności nieprawidłowe zliczanie arytmii spowodowane m.in. sterowaniem załamkiem T oraz uszkodzenia elektrod. Zbędne defibrylacje mogą działać proarytmicznie, wywołując groźne arytmie komorowe. Jednak nawet jeśli nie dochodzi do tak niebezpiecznych następstw, niepotrzebne wyładowania defibrylatora wywołują stres, lęk i nieufność pacjentów wobec urządzenia. W konsekwencji chorzy próbując unikać sytuacji sprzyjających defibrylacjom, ograniczają swoją zwykłą aktywność.
Z naszego ośrodka najbardziej spektakularnym przykładem niefortunnego ciągu zdarzeń związanych z niepotrzebną interwencją jest historia młodego pacjenta, który wyładowanie ICD spowodowane tachykardią zatokową miał w chwili podbiegania do pociągu. W czasie defibrylacji upadł, doznając urazu i złamania ręki, co stało się powodem przedłużonej absencji chorobowej i w konsekwencji utraty pracy. Uważne programowanie urządzenia, dostosowane indywidualnie do pacjenta oraz nastawianie wysokiego punktu odcięcia dla detekcji arytmii, szczególnie u osób młodych, mogą zmniejszyć częstość nieuzasadnionych defibrylacji. Istnieją doniesienia wskazujące na rzadsze interwencje w przypadku stosowania urządzeń dwujamowych (14), co wiąże się z ich większymi możliwościami rozróżniania arytmii. Jednak dane z subanalizy badania MADIT II pokazują trend w kierunku zwiększonej śmiertelności i częstości występowania niewydolności serca w grupie pacjentów z dwujamowymi ICD w porównaniu z grupą z urządzeniami jednojamowymi (15).
Elektrody
Najsłabszymi elementami układów ICD, ulegającym najczęstszym uszkodzeniom są elektrody. Uszkodzenie elektrody równa się zaburzeniom sterowania i, co za tym idzie, nieadekwatnym interwencjom, a w przypadku zaburzeń rytmu – groźbie nieskutecznych defibrylacji. Stosunkowo krótki czas pracy elektrod defibrylujących wiąże się z koniecznością usuwania starych bądź implantacji nowych obok starych, co stwarza szczególnie w układach wieloelektrodowych (resynchronizujących) większe ryzyko wzajemnego przecierania się osłonek i w konsekwencji zakażenia elektrod, a także zwiększa ryzyko zakrzepicy żylnej. Z roku na rok rośnie liczba usuwanych przezżylnie elektrod. Procedurę taką wykonują wyłącznie wysoko wyspecjalizowane ośrodki, mające zaplecze kardiochirurgiczne; wówczas jest to procedura bezpieczna (16). W przypadku usuwania elektrod defibrylujących istnienie górnego zwoju defibrylującego w żyle głównej górnej stanowi istotne utrudnienie dla operatora.
Stałe udoskonalanie techniczne doprowadziło m.in. do wyprodukowania bardzo cienkich elektrod defibrylujących. Dziś wiemy, że mniejszy przekrój elektrody nie oznacza samych korzyści, gdyż może wiązać się ze zwiększonym ryzykiem perforacji mięśnia serca i w skrajnych wypadkach – tamponady (17), a także powoduje mniejszą trwałość elektrod.
Powikłania infekcyjne
Zakażenia układu ICD szacuje się na 0,5-3,8%. Ryzyko ich wystąpienia jest zwiększone w przypadku ponownych zabiegów (wymiany), a także w przypadku pozostawienia starych, nieczynnych elektrod, które z czasem ulęgają uszkodzeniu. Niestety – wymienione sytuacje będą zdarzać się coraz częściej. Należy odróżnić lokalne zakażenie urządzenia, ograniczone do loży od infekcyjnego zapalenia wsierdzia związanego (IZW) z urządzeniem. W tym ostatnim konieczna jest przedłużona antybiotykoterapia i usunięcie całego układu wraz z elektrodami. Najnowsze wytyczne leczenia IZW zalecają u większości pacjentów usunięcie przezskórne nawet w przypadku obecności dużych (>10 mm) wegetacji (18).
Zaburzenia lękowe
Nieodłącznym towarzyszem wielu osób z implantowanym ICD jest lęk. Rozwija się on u ponad 15% pacjentów po zabiegu i zdecydowanie częściej dotyka tych, którzy doświadczają wyładowań ICD (19), zarówno adekwatnych, jak i nieadekwatnych. Wykazano, że u połowy chorych zaburzenia lękowe utrzymują się nadal po upływie roku (20). Rozpoznanie ich oraz wdrożenie odpowiedniej terapii daje korzystne efekty (21), jednak w naszych warunkach rzadko zdarza się, by ośrodki implantujące i kontrolujące ICD miały zapewnioną możliwość ścisłej współpracy z psychologiem lub/i psychiatrą.
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
29 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
69 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
129 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 78 zł
Piśmiennictwo
1. Zipes DP, Camm AJ, Borggrefe M et al.: American College of Cardiology/American Heart Association Task Force; European Society of Cardiology Committee for Practice Guidelines; European Heart Rhythm Association and the Heart Rhythm Society. ACC/AHA/ESC 2006 guidelines for management of patients with ventricular arrhythmias and the prevention of sudden cardiac death - executive summary: A report of the American College of Cardiology/American Heart Association Task Force and the European Society of Cardiology Committee for Practice Guidelines (Writing Committee to Develop Guidelines for Management of Patients with Ventricular Arrhythmias and the Prevention of Sudden Cardiac Death) Developed in collaboration with the European Heart Rhythm Association and the Heart Rhythm Society. Eur Heart J 2006; 17: 2099-140.
2. A comparison of antiarrhythmic-drug therapy with implantable defibrillators in patients resuscitated from near-fatal ventricular arrhythmias. The Antiarrhythmics versus Implantable Defibrillators (AVID) Investigators. N Engl J Med 1997; 337: 1576-83.
3. Connolly SJ, Gent M, Roberts RS et al.: Canadian implantable defibrillator study (CIDS): a randomized trial of the implantable cardioverter defibrillator against amiodarone. Circulation 2000; 101: 1297-302.
4. Kuck KH, Cappato R, Siebels J et al.: Randomized comparison of antiarrhythmic drug therapy with implantable defibrillators in patients resuscitated from cardiac arrest: the Cardiac Arrest Study Hamburg (CASH). Circulation 2000; 102: 748-54.
5. Connolly SJ, Hallstrom AP, Cappato R et al.: Meta-analysis of the implantable cardioverter defibrillator secondary prevention trials. AVID, CASH and CIDS studies. Antiarrhythmics vs Implantable Defibrillator study. Cardiac Arrest Study Hamburg. Canadian Implantable Defibrillator Study. Eur Heart J 2000; 21: 2071-8.
6. Moss AJ, Hall WJ, Cannom DS et al.: Improved survival with an implanted defibrillator in patients with coronary disease at high risk for ventricular arrhythmia. Multicenter Automatic Defibrillator Implantation Trial Investigators. N Engl J Med 1996; 335: 1933-40.
7. Buxton AE, Lee KL, Fisher JD et al.: A randomized study of the prevention of sudden death in patients with coronary artery disease. Multicenter Unsustained Tachycardia Trial Investigators. N Engl J Med 1999; 341: 1882-90.
8. Moss AJ, Zareba W, Hall WJ et al.: Multicenter Automatic Defibrillator Implantation Trial II Investigators. Prophylactic implantation of a defibrillator in patients with myocardial infarction and reduced ejection fraction. N Engl J Med 2002; 346: 877-83.
9. Goldenberg I, Gillespie J, Moss AJ et al.: Executive Committee of the Multicenter Automatic Defibrillator Implantation Trial II. Long-term benefit of primary prevention with an implantable cardioverter-defibrillator: an extended 8-year follow-up study of the Multicenter Automatic Defibrillator Implantation Trial II. Circulation 2010; 122: 1265-71.
10. Huikuri HV, Exner DV, Kavanagh KM et al.: CARISMA and REFINE Investigators. Attenuated recovery of heart rate turbulence early after myocardial infarction identifies patients at high risk for fatal or near-fatal arrhythmic events. Heart Rhythm 2010; 7: 229-35.
11. Jacobson AF, Senior R, Cerqueira MD et al.: ADMIRE-HF Investigators. Myocardial iodine-123 meta-iodobenzylguanidine imaging and cardiac events in heart failure. Results of the prospective ADMIRE-HF (AdreView Myocardial Imaging for Risk Evaluation in Heart Failure) study. J Am Coll Cardiol 2010; 55: 2212-21.
12. Gradaus R, Block M, Brachmann J et al.: German EURID Registry. Mortality, morbidity, and complications in 3344 patients with implantable cardioverter defibrillators: results from the German ICD Registry EURID. Pacing Clin Electrophysiol 2003; 26: 1511-8.
13. Van der Velden LB, Huybrechts W, Adriaensens B et al.: Appropriate and inappropriate implantable cardioverter defibrillator interventions during secondary prevention. Acta Cardiol 2008; 63: 39-45.
14. Almendral J, Arribas F, Wolpert C et al.: DATAS Steering Committee; DATAS Writing Committee; DATAS Investigators. Dual-chamber defibrillators reduce clinically significant adverse events compared with single-chamber devices: results from the DATAS (Dual chamber and Atrial Tachyarrhythmias Adverse events Study) trial. Europace 2008; 10: 528-35.
15. Berenbom LD, Weiford BC, Vacek JL et al.: Differences in outcomes between patients treated with single- versus dual-chamber implantable cardioverter defibrillators: a substudy of the Multicenter Automatic Defibrillator Implantation Trial II. Ann Noninvasive Electrocardiol 2005; 10: 429-35.
16. Borek PP, Wilkoff BL: Pacemaker and ICD leads: strategies for long-term management. J Interv Card Electrophysiol 2008; 23: 59-72.
17. Danik SB, Mansour M, Singh J et al.: Increased incidence of subacute lead perforation noted with one implantable cardioverter-defibrillator. Heart Rhythm 2007; 4: 439-42.
18. Habib G, Hoen B, Tornos P et al.: ESC Committee for Practice Guidelines. Guidelines on the prevention, diagnosis, and treatment of infective endocarditis (new version 2009): the Task Force on the Prevention, Diagnosis, and Treatment of Infective Endocarditis of the European Society of Cardiology (ESC). Endorsed by the European Society of Clinical Microbiology and Infectious Diseases (ESCMID) and the International Society of Chemotherapy (ISC) for Infection and Cancer. Eur Heart J 2009; 30: 2369-413.
19. Godemann F, Butter C, Lampe F et al.: Panic disorders and agoraphobia: side effects of treatment with an implantable cardioverter/defibrillator. Clin Cardiol 2004; 27: 321-6.
20. Pedersen SS, den Broek KC, Theuns DA et al.: Risk of chronic anxiety in implantable defibrillator patients: A multi-center study. Int J Cardiol 2009 Nov 5. (Epub ahead of print).
21. Salmoirago-Blotcher E, Ockene IS: Methodological limitations of psychosocial interventions in patients with an implantable cardioverter-defibrillator (ICD) A systematic review. BMC Cardiovasc Disord 2009; 9: 56.
22. Duru F, Dorian P, Favale S et al.: PAtient NOtifier Feature for Reduction of Anxiety: A Multicenter ICD Study investigators. Effects of an alert system on implantable cardioverter defibrillator-related anxiety: rationale, design, and endpoints of the PANORAMIC multicentre trial. Europace 2010; 12: 726-30.
23. Halshtok O, Goitein O, Abu Sham'a R et al.: Pacemakers and magnetic resonance imaging: no longer an absolute contraindication when scanned correctly. Isr Med Assoc J 2010; 12: 391-5.
24. Wilkoff BL, Bello D, Taborsky M et al.: EnRhythm MRI SureScan Pacing System Study Investigators. Magnetic Resonance Imaging in Patients with a Pacemaker System Designed for the MR Environment. Heart Rhythm 2010 Oct 5. (Epub ahead of print).
25. Bardy GH, Smith WM, Hood MA et al.: An entirely subcutaneous implantable cardioverter-defibrillator. N Engl J Med 2010; 363: 36-44.
26. Varma N, Epstein AE, Irimpen A et al.: TRUST Investigators. Efficacy and safety of automatic remote monitoring for implantable cardioverter-defibrillator follow-up: the Lumos-T Safely Reduces Routine Office Device Follow-up (TRUST) trial. Circulation. 2010; 122: 325-32.
27. Marzegalli M, Landolina M, Lunati M et al.: Design of the evolution of management strategies of heart failure patients with implantable defibrillators (EVOLVO) study to assess the ability of remote monitoring to treat and triage patients more effectively. Trials 2009; 10: 42.

