© Borgis - Postępy Nauk Medycznych 12/2010, s. 956-962
*Michał Ambroziak, Andrzej Budaj
Choroba wieńcowa w młodym wieku jako efekt współdziałania czynników genetycznych i środowiskowych
Coronary artery disease in young age as the effect of cooperation between genetic and environmental factors
Klinika Kardiologii Centrum Medycznego Kształcenia Podyplomowego, Szpital Grochowski, Warszawa
Kierownik Kliniki: prof. dr hab. med. Andrzej Budaj
Streszczenie
Zawał serca w młodym wieku należy w ostatnich latach do najpoważniejszych problemów medycznych i społecznych. Poznanie czynników genetycznych, leżących u podłoża tego zjawiska wciąż pozostaje dużym wyzwaniem.
W poszukiwaniach polimorfizmów genów kandydatów zidentyfikowano kilka najważniejszych związanych z rozwojem choroby wieńcowej w młodym wieku, wśród nich polimorfizm w genie LDLR receptora LDL, w genie białka przenoszącego estry cholesterolu CETP czy w genie czynnika V Leiden.
Badania asocjacji, koncentrujące się na ocenie związku występowania choroby wieńcowej z określonymi regionami chromosomalnymi, wskazują na obszar 9p21, który w chwili obecnej wydaje się mieć w tym procesie największe znaczenie. Zmienność w tym regionie stanowi niezależny czynnik ryzyka choroby wieńcowej przed 45. rokiem życia, na poziomie zbliżonym do ryzyka związanego z podwyższonym BMI czy hipercholesterolemią. U młodych osób koreluje ona ze stopniem zaawansowania zmian w tętnicach wieńcowych oraz może wpływać na rokowanie po ostrym zespole wieńcowym. Inne regiony chromosomalne, np.: 1p13.3 czy 6p24, wiązane są ze zwiększonym ryzykiem choroby wieńcowej poprzez nasilanie działania takich czynników jak hiperlipidemia. Zidentyfikowano także polimorfizmy, np.: w genie receptora aktywowanego proliferatorami peroksysomów typu alfa PPARalfa lub w genie receptora nikotynowego CHRN3, które modyfikują wpływ środowiskowych czynników ryzyka (poziom aktywności fizycznej, palenie tytoniu) na ryzyko choroby wieńcowej.
Tak więc wydaje się, że najważniejsze dla rozwoju choroby wieńcowej w młodym wieku ma współdziałanie różnych czynników ryzyka, w tym w szczególności modyfikacja wpływów środowiskowych przez określone uwarunkowania genetyczne.
Summary
Myocardial infarction in young age is a growing medical and social problem in last decades. The explanation of the genetic background of this phenomenon remains still a serious challenge.
Several single nucleotide polimorphisms realted to the risk of coronary artery disease development as polimorphisms in LDL receptor, cholesterol ester transfer protein CETP or factor V Leiden genes have been identified in many studies.
Association studies focusing on the searching of genetic loci associated with the incidence of coronary artery disease, indicate the 9p21 locus as the most important in this process. A variant at chromosome 9p21 is thought to be an independent risk factor of coronary artery disease in young age with odds ratio level close to BMI and hypercholesterolemia. Moreover, there is a correlation between polymorphism in this loci and the severity of changes in coronary arteries in young age as well as prognosis after acute coronary syndrome.
The other chromosomal loci variants, as 1p13.3 and 6p24, are involved in the coronary artery disease risk incidence by leading to the development of other disorders related to the atherothrombosis, as hyperlipidemia. Moreover, some identified genetic polimorphisms (for example: within peroxisome proliferator-activated receptor-alpha PPARalfa or nicotine receptor CHRN3genes) modify the influence of environmental factors, as physical activity intensivity or tobacco smoking, on the coronary artery disease.
Thus, a cooperation between different risk factors as well as the influence of the genetic ground on the environmental factors seem to be crucial for the development of coronary artery disease in young age.

Epidemiologia choroby wieńcowej w XXI wieku. Zawał serca w młodym wieku jako problem medyczny i społeczny
Mimo burzliwego rozwoju kardiologii w dziedzinie rozpoznawania i leczenia choroby wieńcowej w ostatnich latach, aterotromboza tętnic wieńcowych pozostaje jednym z największych „zabójców” ludzi we współczesnym świecie. Według szacunków Światowej Organizacji Zdrowia choroby układu krążenia są w 2010 roku, podobnie jak w latach poprzednich, najczęstszą przyczyną zgonów na Ziemi (1). Niepokojącą tendencją, jaka rysuje się w globalnych statystykach, jest zwiększająca się liczba osób, które zaczynają chorować w młodym wieku. W latach 70-tych i 80-tych XX stulecia odsetek chorych przechodzących zawał serca przed 45. rokiem życia utrzymywał się na poziomie 2-6%, w latach 90. wzrósł natomiast do 10%. Polskie dane z 2004 roku mówią o 5,2% chorych z zawałem serca przed 50. rokiem życia (2). Dzieje się tak mimo wzrastającej świadomości na temat zdrowego stylu życiu, roli aktywności fizycznej czy właściwego sposobu odżywiania się.
Fakty te wskazują na konieczność lepszego poznania patogenezy choroby wieńcowej, ze zwróceniem szczególnej uwagi na te czynniki, które decydują o jej rozwoju u ludzi młodych. Niewątpliwie istotne znaczenie mają uwarunkowania genetyczne, których zbadanie wciąż pozostaje dużym wyzwaniem. Zidentyfikowanie ich ma na celu określenie z większą precyzją grupy osób, obciążonych zwiększonym ryzykiem zawału serca w młodym wieku i wyprzedzenie wystąpienie tego zdarzenia odpowiednimi działaniami medycznymi, zgodnie z zasadą: lepiej zapobiegać niż leczyć. Ma to także swoje przełożenie na względy ekonomiczne i społeczne, związane z ograniczeniem kosztów leczenia zawału serca, absencji w pracy oraz wieloletniej opieki medycznej i rent zdrowotnych, co szczególnie w dobie światowych kryzysów nie może pozostać niezauważone.
Choroby dziedziczne związane z rozwojem choroby wieńcowej w młodym wieku
Wśród uwarunkowań genetycznych, prowadzących do rozwoju choroby wieńcowej w młodym wieku szczególną, choć nie najliczniejszą grupę stanowią przyczyny o charakterze jednogenowym, związane z występowaniem znanych mutacji leżących u podłoża różnych chorób dziedzicznych.
Najczęściej spotykaną spośród nich jest hipercholesterolemia rodzinna. Zidentyfikowano ponad 700 mutacji w genach kodujących białka kluczowe dla metabolizmu lipidów. Ich nieprawidłowości prowadzą m.in. do upośledzenia wiązania LDL do jego receptora (mutacja w genie LDLR), zwiększonej degradacji receptora LDL (mutacja w genie PSK9– ang. proprotein-convertase subtilisin-kexin type 9) czy upośledzenia endocytozy receptora (mutacja w genie białka adaptorowego receptora LDL typu 1 LDLRAP1) (3). Dziedziczenie tych zaburzeń ma charakter autosomalny dominujący, częstość występowania homozygot ocenia się na 1:1 mln, heterozygot – 1:500 tys.
Znacznie rzadziej stwierdza się rodzinną hiperlipidemię (mutacja w genie cytochromu 450 CYP7A1, prowadząca do zaburzeń rozkładu cholesterolu), rodzinny defekt ApoB (związany z zaburzeniem wiązania lipoproteiny B do LDLr), homocystynurię (dziedziczone autosomalnie recesywnie zaburzenia ekspresji enzymu syntazy β-cystationionowej, występujące średnio na 1:335 000 z dużym zróżnicowaniem geograficznym, np.: Katar 1:3000, Norwegia 1:6400, Japonia 1:900 000) lub zupełnie kazuistycznie spotykane: chorobę Tangierską czy sitosterolemię. Choroba tangierska, stwierdzona po raz pierwszy na wyspie Tangier, jest rodzinnym niedoborem HDL, dziedziczonym autosomalnie recesywnie. Spowodowana jest mutacją w położonym na chromosomie 9 genie ABC1 (ATP-binding cassette-1), kodującym białko transportujące cholesterol i fosfolipidy. Do tej pory na całym świecie opisano zaledwie około 50 przypadków. Sitosterolemia to równie rzadka (opisanych 45 przypadków) dziedziczona autosomalnie recesywnie choroba, charakteryzująca się nadmierną absorpcją jelitową i zmniejszonym wydzielaniem z żółcią steroli zawartych w pokarmach.
Uwarunkowania genetyczne jako niezależny czynnik ryzyka choroby wieńcowej
Największą, a jednocześnie najtrudniejszą do zbadania grupę uwarunkowań genetycznych aterotrombozy stanowią przyczyny o charakterze wielogenowym. Badania, mające na celu ocenę podłoża genetycznego aterotrombozy tętnic wieńcowych, obejmują obecnie dwa podstawowe kierunki. Pierwszy z nich opiera się na typowaniu tzw. genów kandydatów, kodujących białka zaangażowane w podstawowe procesy prowadzące do rozwoju choroby wieńcowej – zapalne, krzepnięcia, metabolizmu lipidów czy funkcji śródbłonka. Drugi nurt to badania asocjacji, polegające na określeniu lokalizacji chromosomalnych związanych z częstszym występowaniem choroby. W obu przypadkach uwaga badaczy skupia się na identyfikacji polimorfizmów pojedynczych nukleotydów (SNP – ang. single nucleotide polymorphism), związanych ze zwiększonym ryzykiem zachorowania.
Badania polimorfizmów genów kandydatów, odpowiedzialnych za rozwój choroby wieńcowej w młodym wieku, przynoszą wiele, niekiedy sprzecznych danych. Ważnych obserwacji dostarczyła część genetyczna badania INTERHEART, w którym w grupie 8759 osób, pochodzących z Europy, Azji i krajów Bliskiego Wschodu analizowano 1536 polimorfizmów zlokalizowanych w 103 genach (4). Znamienność statystyczną wykazano w przypadku 13 SNP, wykazując ich związek z ryzykiem zawału serca (rs7412 w genie Kapo E, rs429358 w genie apolipoproteiny E Apo E, rs6511720, rs6511721, rs2228671, rs5927 i rs1433099 w genie LDLR receptora LDL, rs1532624, rs1532625 i rs1800775 w genie białka przenoszącego estry cholesterolu CETP oraz rs693 w genie apolipoproteiny B ApoB).
W innej pracy, opublikowanej w 2010 roku wykazano, że polimorfizm G1691A genu czynnika V Leiden może mieć znaczenie w rozwoju choroby wieńcowej u młodych ludzi przed 5. rokiem życia (5). Pozostałe polimorfizmy, które wedle najnowszych opracowań mogą sprzyjać rozwojowi choroby wieńcowej w młodym wieku to: ε2/ε3/ε4 genu apolipoproteiny E oraz G20210A genu protrombiny (6, 7).
Badania związku określonych regionów chromosomalnych z występowaniem choroby wieńcowej mają charakter dużych wieloośrodkowych projektów GWAS (ang. genom wide association studies) i prowadzone są w ramach międzynarodowych konsorcjów, m.in.: Wellcome Trust Case Control Consortium (1926 chorych, 2938 zdrowych osób), Myocardial Infarction Genetics Consortium (MIGen – 2967 chorych, 3075 zdrowych) czy Ottawa Heart Genomics Study (3323 chorych, 2319 zdrowych), czy wreszcie ogromne konsorcjum CARDIoGRAM, skupiające w swoich ramach 13 GWAS, w którym analizie poddaje się DNA, pochodzące od 20 000 chorych z chorobą wieńcową oraz 60 000 osób zdrowych.
Regionem, który w chwili obecnej wydaje się mieć największy związek z rozwojem choroby wieńcowej jest fragment chromosomu 9 na jego krótkim ramieniu – 9p21.3 (ryc. 1). W obszarze tym zidentyfikowano dotychczas blisko 60 polimorfizmów, z których część wykazuje związek z występowaniem choroby wieńcowej w młodym wieku. Jednym z tych, które mogą mieć szczególnie duże znaczenie jest polimorfizm rs1333049[G/C]. Wykazano, że allel C (cytozyna) stanowi allel ryzyka, stwierdzany istotnie częściej u młodych osób z chorobą wieńcową. Ryzyko choroby wieńcowej dla tego polimorfizmu określono na 1,6-krotne dla homozygot i 1,3-krotne dla heterozygot (8). Co więcej, u młodych osób z chorobą wieńcową forma tego polimorfizmu koreluje ze stopniem zaawansowania zmian w tętnicach wieńcowych (9). Z kolei w badaniu przeprowadzonym wśród chorych z rejestru GRACE, wykazano, że polimorfizm rs1333049 w regionie 9p21.3 wiąże się ze zwiększonym ryzykiem ponownego zawału oraz zgonu z przyczyn sercowych w obserwacji 6-miesięcznej po ostrym zespole wieńcowym, wskazując także na allel C jako allel ryzyka (10).
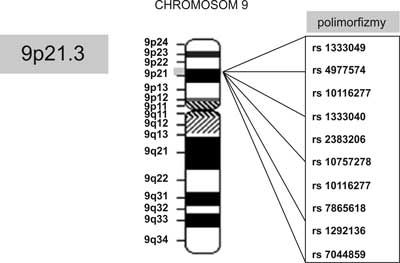
Ryc. 1. Lokalizacja regionu związanego ze zwiększonym ryzykiem choroby wieńcowej na chromosomie 9 oraz niektóre z opisanych w tym obszarze polimorfizmów.
Mechanizm, który leży u podłoża związku zmienności chromosomalnej w regionie 9p21.3 z występowaniem choroby wieńcowej nie jest do końca jasny. Obszar ten jest regionem niekodującym, dlatego oddziaływanie to wiązane jest z zaburzeniami ekspresji najbliżej zlokalizowanych genów: inhibitorów kinaz zależnych od cykliny typu 1 i 2 ( CDKN2B i CDKN2A) oraz genu 5' fosforylazy metyltioadenozyny MTPA (11, 12). Inni badacze wskazują na wtórne do obecności polimorfizmu w regionie 9p21 zaburzenia funkcji zlokalizowanej tam sekwencji regulatorowej ANRIL (ang. antisense noncoding RNA), jako na zjawisko prowadzące do zmiany ekspresji genów regulatorowych cyklu komórkowego (13). W konsekwencji tego dochodzi do zaburzeń przejścia komórek do fazy S cyklu i tym samym do nasilenia ich proliferacji. Zjawisko to może dotyczyć bardzo różnych komórek, co może tłumaczyć związek zmienności chromosomalnej w regionie 9p21 z występowaniem nie tylko choroby wieńcowej, ale także cukrzycy typu 2, tętniaków aorty brzusznej i ośrodkowego układu nerwowego, nowotworów, takich jak: glejak, czerniak czy rak podstawnokomórkowy, a także choroby Alzheimera. Rozpowszechnienie zmienności chromosomalnej w regionie 9p21 jest bardzo duże. Ocenia się, że w Europie odsetek osób, posiadających 1 allel ryzyka choroby wieńcowej wynosi 50%, dwóch alleli – 25% (8).
We włoskim badaniu, które obejmowało 1508 chorych z zawałem serca przed 45. rokiem życia, wartość OR dla polimorfizmu rs1333040 w regionie 9p21 w odniesieniu do ryzyka wystąpienia zawału serca u młodego człowieka określono na 1,43 (CI 1,22-1,66, p=0,0000093), co plasuje ten czynnik na poziomie zbliżonym do ryzyka związanego z podwyższonym BMI i hipercholesterolemią (14).
W ramach dużego międzynarodowego konsorcjum Myocardial Infarction Genetic Consortium przeanalizowano 554 różnych wariantów genetycznych w grupie 2976 chorych z zawałem w młodym wieku oraz w grupie kontrolnej, liczącej 3075 osób (15). Zidentyfikowano kilka innych regionów chromosomalnych, których zmienność związana może być ze zwiększonym ryzykiem choroby wieńcowej w młodym wieku, choć nie jest on tak wyraźny jak w przypadku 9p21. Są to obszary: 3q22.3, 2q33, 12q24, 10q11.21 i 21q22 (ryc. 2). Stwierdzono, że 8 SNP w tych obszarach, w tym dwa dotychczas nieopisywane, mają najsilniejszy związek z rozwojem choroby wieńcowej przed 45. rokiem życia.

Ryc. 2. Najważniejsze lokalizacje chromosomalne regionów związanych ze zwiększonym ryzykiem choroby wieńcowej.
Uwarunkowania genetyczne jako czynnik ryzyka choroby wieńcowej związany z chorobami sprzyjającymi aterotrombozie
Opisanych zostało wiele innych polimorfizmów pojedynczego nukleotydu w genach odpowiedzialnych za podstawowe procesy prowadzące do rozwoju aterotrombozy i przez to związanych ze zwiększonym ryzykiem choroby wieńcowej. Jednym z nich jest polimorfizm we wspomnianym już wcześniej genie PCSK9, którego jeden z alleli wiąże się z obniżeniem poziomu LDL i tym samym jest określany jako czynnik zabezpieczający przed rozwojem aterotrombozy (16).
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
24 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
59 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
119 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 28 zł
Piśmiennictwo
1. Cardiovascular disease – key facts: http://www.who.int/cardiovascular_diseases/en.
2. Stan zdrowia ludności Polski w 2004 roku: http://www.stat.gov.pl/gus.
3. Alves AC, Medeiros AM, Francisco V et al.: Molecular diagnosis of familial hypercholesterolemia: an important tool for cardiovascular risk stratification. Rev Port Cardiol 2010; 29: 907-21.
4. Anand SS, Xie C, Paré G et al.: Genetic variants associated with myocardial infarction risk factors in over 8000 individuals from five ethnic groups: The INTERHEART Genetics Study. Circ Cardiovasc Genet 2009; 2: 16-25.
5. Mannucci PM, Asselta R, Duga S et al.: The association of factor V Leiden with myocardial infarction is replicated in 1880 patients with premature disease. J Thromb Haemost 2010; 8: 2116-2121.
6. Bennet AM, Di Angelantonio E, Ye Z et al.: Association of apolipoprotein E genotypes with lipid levels and coronary risk. JAMA 2007; 298: 1300-11.
7. Ye Z, Liu EH, Higgins JP et al.: Seven haemostatic gene polymorphisms in coronary disease: meta-analysis of 66,155 cases and 91,307 controls. Lancet 2006; 367: 651-8.
8. Schunkert H, Götz A, Braund P et al.: Repeated replication and a prospective meta-analysis of the association between chromosome 9p21.3 and coronary artery disease. Circulation 2008; 117: 1675-84.
9. Dandona S, Stewart AF, Chen L et al.: Gene dosage of the common variant 9p21 predicts severity of coronary artery disease. J Am Coll Cardiol 2010; 56: 479-86.
10. Buysschaert I, Carruthers KF, Dunbar DR et al.: A variant at chromosome 9p21 is associated with recurrent myocardial infarction and cardiac death after acute coronary syndrome: the GRACE Genetics Study. Eur Heart J 2010; 31: 1132-41.
11. Holdt LM, Sass K, Gäbel G et al.: Expression of Chr9p21 genes CDKN2B (p15(INK4b)), CDKN2A (p16(INK4a)), p14(ARF) and MTAP in human atherosclerotic plaque. Atherosclerosis 2010 (in press).
12. Musunuru K, Post WS, Herzog W et al.: Association of single nucleotide polymorphisms on chromosome 9p21.3 with platelet reactivity: a potential mechanism for increased vascular disease. Circ Cardiovasc Genet 2010; 3: 445-53.
13. Holdt LM, Beutner F, Scholz M et al.: ANRIL expression is associated with atherosclerosis risk at chromosome 9p21. Arterioscler Thromb Vasc Biol 2010; 30: 620-7.
14. Ardissino D, Merlini PA, Mannucci PM et al.: (Atherosclerosis, Thrombosis, and Vascular Biology Italian Investigators): Influence of 9p21.3 genetic variants on clinical and angiographic outcomes in early-onset myocardial infarction. American College of Cardiology 58th Annual Scientific Session 2009.
15. Kathiresan S, Voight BF, Purcell S et al.: Myocardial Infarction Genetics Consortium. Genome-wide association of early-onset myocardial infarction with single nucleotide polymorphisms and copy number variants. Nat Genet 2009; 41: 334-41.
16. Guella I, Asselta R, Ardissino D et al.: Effects of PCSK9 genetic variants on plasma LDL cholesterol levels and risk of premature myocardial infarction in the Italian population. J Lipid Res 2010; 51: 3342-9.
17. Linsel-Nitschke P, Heeren J, Aherrahrou Z et al.: Genetic variation at chromosome 1p13.3 affects sortilin mRNA expression, cellular LDL-uptake and serum LDL levels which translates to the risk of coronary artery disease. Atherosclerosis 2010; 208: 183-9.
18. Lluís-Ganella C, Lucas G, Subirana I et al.: Additive effect of multiple genetic variants on the risk of coronary artery disease. Rev Esp Cardiol 2010; 63: 925-33.
19. Anderson JL, Horne BD, Camp NJ et al.: Joint effects of common genetic variants from multiple genes and pathways on the risk of premature coronary artery disease. Am Heart J 2010; 160: 250-256.
20. Davies RW, Dandona S, Stewart AF et al.: Improved prediction of cardiovascular disease based on a panel of single nucleotide polymorphisms identified through genome-wide association studies. Circ Cardiovasc Genet 2010; 3: 468-74.
21. Hancer VS, Diz-Kucukkaya R, Bilge AK et al.: The association between factor XIII Val34Leu polymorphism and early myocardial infarction. Circ J 2006; 70: 239-42.
22. Nazarov IB, Woods DR, Montgomery HE et al.: The angiotensin converting enzyme I/D polymorphism in Russian athletes. Eur J Hum Genet 2001; 9: 797-801.
23. Thompson J, Raitt J, Hutchings L et al.: Angiotensin-converting enzyme genotype and successful ascent to extreme high altitude. High Alt Med Biol 2007; 8: 278-85.
24. Oh SD: The distribution of I/D polymorphism in the ACE gene among Korean male elite athletes. J Sports Med Phys Fitness 2007; 47: 250-4.
25. Feitosa MF, Rice T, Rankinen T et al.: Common genetic and environmental effects on lipid phenotypes: the HERITAGE family study. Hum Hered 2005; 59: 34-40.
26. Naito H, Kamijima M, Yamanoshita O et al.: Differential effects of aging, drinking and exercise on serum cholesterol levels dependent on the PPARA-V227A polymorphism. J Occup Health 2007; 49: 353-62.
27. Furberg H, Kim Y, Dackor J et al.: Genome-wide meta-analyses identify multiple loci associated with smoking behavior. Nat Genet 2010; 42: 441-7.


